
题目列表(包括答案和解析)
|
甲组 |
Na+ |
Ba2+ |
Mg2+ |
Fe3+ |
|
乙组 |
Cl- |
OH- |
CO |
SO |
A,B,C,D,E五种化合物都是由这两组中的各一种离子组成(离子可重复使用),这五种化合物的性质如下:
(1)A既不溶于水,也不溶于酸.
(2)B溶于水形成的溶液显碱性,要向B中加入Na2SO4溶液则产生A.
(3)C溶于水得无色溶液,向C中加入B的溶液产生白色沉淀,再加盐酸沉淀仅部分溶解.
(4)D溶于水后得无色溶液,加入
(5)E物质是红褐色固体,不溶于水但溶于酸.
根据以上性质,试推断A为(写化学式,以下同)____________、B为____________、C为____________、D为____________、E为____________,写出有关的化学反应方程式:
________________________、________________________、________________________、________________________、________________________.
下图所示为实验室常用的实验装置。

据此回答下列问题:
⑴写出带标号仪器的名称:① ② ;
⑵实验室通常用稀盐酸和石灰石反应制取CO2,该反应的化学方程式为 ,发生装置为 ;装置F可用来测量生成的CO2气体的体积,其中在水面上放一层植物油的目的是 ,植物油上方原有的空气对实验的结果 (填“有”或“没有”)明显影响。
⑶小丫在探究CO2与NaOH溶液反应的实验中,先用铝制易拉罐收集满一罐CO2气体,然后迅速向其中加入一定量的NaOH浓溶液,立即将易拉罐口封闭(不漏气),轻轻摇动易拉罐,发现易拉罐很快变瘪,但过一段时间后,易拉罐又重新鼓起来(反应过程中温度的变化忽略不计)。
【讨论】小丫认为易拉罐变瘪,说明CO2与NaOH溶液发生反应;小敏认为此结论不合理,还需进一步验证,验证方法是 ;易拉罐为什么又后鼓起来?是不是反应又产生了气体,该气体的成分?
【提出猜想】a.可能是CO2 b.可能是 。
【查阅资料】①Na2CO3具有较强的热稳定性,只有在高温条件下才会分解;
②铝不仅与酸反应,还能与碱溶液反应2Al+2NaOH+2H2O==2NaAlO2+3X↑
【实验验证】
①将易拉罐口打开,迅速用燃着的木条伸入罐口,发出“噗”的一声,产生淡蓝色火焰,片刻后熄灭。证明猜想 成立;
②取少量铝片于试管中,先加入适量的水,无明显变化。片刻后再加入少量的氢氧化钠浓溶液,产生气泡。该步实验的目的是 ;
【结论】CO2与NaOH反应的化学方程式是 ;
【反思与应用】在生活中铝制容器不能用来盛装酸性物质,也不能盛装 性物质。
【解析】(1)熟知实验常用仪器的名称(2) (2)实验室通常用稀盐酸和石灰石反应制取CO2,反应原理是:CaCO3+2HCl=CaCl2+CO2↑+H2O,属于“固液不加热型”.二氧化碳气体密度比空气大,易溶于水.据此来选择发生装置和收集装置即可.由于实验测得的气体为F装置内的CO2气体的体积,而空气中也有CO2,又因为CO2既不溶于植物油,也不和植物油反应,所以在水面上放一层植物油的目的是防止CO2溶于水、防止CO2与水反应、防止CO2与水接触;所以植物油上方原有的空气对实验的结果就不会有明显影响.
(3)【讨论】根据碳酸离子与钙离子反应生成沉淀碳酸钙;
【提出猜想】根据质量守恒定律进行猜想,可能是氢气;
【实验验证】①根据燃烧的现象进行分析;
②根据实验内容和过程进行分析;
【结论】根据CO2与NaOH的反应写出反应的方程式;
【反思与应用】根据铝的性质分析铝制容器使用注意的事项.
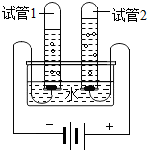 水是生命之源,人类的生活生产离不开水.
水是生命之源,人类的生活生产离不开水.| 通电 |
| 通电 |
 33、随着人们生活水平的提高,人们对于食品不但要求营养,更要求健康.市场上出现了一些不添加防腐剂的绿色食品,这种食品中有一个单独包装的保鲜剂,不会危害食品安全.某同学找来一种在空气中放置一段时间的食品保鲜剂,对它进行探究.
33、随着人们生活水平的提高,人们对于食品不但要求营养,更要求健康.市场上出现了一些不添加防腐剂的绿色食品,这种食品中有一个单独包装的保鲜剂,不会危害食品安全.某同学找来一种在空气中放置一段时间的食品保鲜剂,对它进行探究.| 实验 | 操作 | 主要现象 | 结论与解释 |
| 实验1 初步判断 |
打开这种保鲜剂的包装袋,取少量样品于试管中,进行观察. | 该样品为白色固体. | 该保鲜剂一定不是 铁粉和硅胶 . |
| 实验2 对该保鲜剂的有效性进行探究 |
向实验1的试管中加入适量的水,震荡. | 形成白色浑浊液体,试管壁发热. | 结论与相关反应方程式 该保鲜剂仍有效,CaO+H2O=Ca(OH)2 . |
| 实验3 对该保鲜剂的成分进行探究 |
过滤实验2所的液体,向滤液中通入二氧化碳. | 溶液变浑浊. | 该保鲜剂中一定含有的物质是 氧化钙 ,对于实验3不能确定的物质是氢氧化钙和碳酸钙 . |
| 将滤渣放入另一试管中,加入足量稀盐酸. | 有气泡产生. |
 2Cu+CO2↑②C+CuO
2Cu+CO2↑②C+CuO Cu+CO↑
Cu+CO↑| 检验方案 | 不可行的原因 | |
| 小杰 | 把小动物放在收集的气体中,观察能否存活 | ③_____________ |
| 小燕 | 点燃生成的气体,观察能否燃烧 | ④______________ |

| 实验现象 | 检验方案 |
| A中固体由黑色变成红色 | 有Cu生成 |
| B中黄色试纸变蓝 | 有⑤_____生成 |
| C中⑥___________ | 有CO2生成 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com