
题目列表(包括答案和解析)

金属材料市现代生活和工业生产中应用极为普遍的一类物质。
(l)铁是一种最主要的金属材料,实验室里用一氧化碳还原氧化铁得到铁,实验过程中先通入一氧化碳的目的是 。
炼铁厂常以焦炭、赤铁矿、空气等主要原料炼铁,反应过程如下:
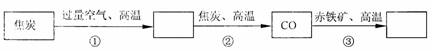
写出②③两步的化学方程式 、 。
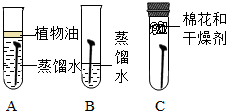
(2)在学习了金属资源保护内容以后,兴趣小组同学对金属的锈蚀做了观察,发现残留水的铁锅在与水面接触的部位最易生锈;家用的铜质水龙头也生了一层绿色的铜锈。为了弄清铁锅生锈的原因,兴趣小组同学用相同的铁钉设计了如下安验。经过一周观察:试管A和C中的铁钉无明显变化,试管B中的铁钉明显锈蚀。

①通过探究发现:铁生锈是铁与 和 共同存在时发生化学反应的过程。
②A中加入的蒸馏水要事先煮沸,其目的是 。
③铜生锈的原因是什么?查阅有关资料:铜锈的主要成份是Cu2(OH)2CO3。他们除依照铁钉锈蚀条件的探究方法进行实验外,还补充做了铜锈蚀与 有关系的实验。请写出一种防止铁或铜等金属制品生锈的具体方法 。
“家事国事天下事事事关心”.作为新时代的中学生,我们不仅要学习文化知识,而且要关注社会,关注生活.
(1)2013年4月20日8点02分四川省雅安市芦山县发生7.0级地震.地震发生后,全国人民抗震救灾,众志成城,彰显了中华民族巨大的凝聚力.
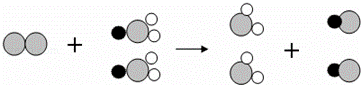
①救灾需要大量的消毒剂,我国研制出比漂白粉更高效的饮用水消毒剂“ClO2”,其反应的微观过程图如下:
(其中 表示氯原子,
表示氯原子, 表示钠原子,
表示钠原子, 表示氧原子)
表示氧原子)
试回答:ClO2叫做 ,其中氯的化合价为 价.
根据反应的微观过程图写出反应的化学方程式为 .
②国家药监局公布的抗震救灾急需药械目录中包括:一次性防护服、活性炭防护口罩、骨科内外固定材料等.其中防护口罩主要是利用活性炭的 性.
③地震发生后,全国各地为灾区紧急提供包括方便面在内的各种救灾物品.据下表回答:
| 方便面营养成分表(每100g中含量) |
| ||||||||
| 糖类 (g) | 脂肪 (g) | 蛋白质 (g) | 水分 (g) | 钠 (mg) | 钾 (mg) | 磷 (mg) | 钙 (mg) | 维生素C (mg) | 其他 |
| 61.6 | 21.1 | 9.5 | 3.6 | 1144 | 134 | 80 | 25 | 0 | … |
方便面所含的营养素主要有蛋白质、 、油脂、无机盐和水.
(2)有机高分子材料、金属材料和无机非金属材料是人类使用的三大类基础材料,它们以各自的特点满足着人类多方面的需要.
①有机高分子材料“玉米塑料”因其可降解被广泛用来替代一次性泡沫塑料,“玉米塑料”的使用可减少“ 污染”.
②金属材料中,有一类贮氢合金能够结合氢气形成金属化合物,并在一定条件下分解释放出氢气,该贮运原理属于 变化(选填“物理”或“化学”).
③无机非金属材料中,用于电子工业的高纯碳酸钙和高纯氧化钙生产流程如下:

实验室常采用 操作进行沉淀分离,生产高纯碳酸钙时,选择“220℃恒温干燥”,而不选择“高温”条件下完成此操作的原因是 (用化学方程式说明).
(3)创新利用CO2,倡导低碳生活,发展低碳经济已成为一种环保时尚.现在许多城市倡导“135”出行,即1公里以内步行,3公里以内骑自行车,5公里乘坐公共交通工具,提倡“低碳城市”、“绿色出行”.
①为减少CO2排放,人们积极寻找不含碳元素的燃料.经研究发现NH3燃烧的产物没有污染,且释放大量能量,有一定应用前景.请将NH3燃烧反应的化学方程式补充完整:4NH3+3O2 6H2O+ 2N2 .
6H2O+ 2N2 .
②法国化学家PaulSabatier采用“组合转化”技术使CO2和H2在催化剂作用下生成CH4和H2O.试写出该反应的化学方程式 CO2+4H2 CH4+2H2O .
CH4+2H2O .
“家事国事天下事事事关心”。作为新时代的中学生,我们不仅要学习文化知识,而且要关注社会,关注生活。
(1)2013年4月20日8点02分四川省雅安市芦山县发生7.0级地震。地震发生后,全国人民抗震救灾,众志成城,彰显了中华民族巨大的凝聚力。
 ①救灾需要大量的消毒剂,我国研制出比漂白粉更高效的饮用水消毒剂“ClO2”,其反应的微观过程图如下:
①救灾需要大量的消毒剂,我国研制出比漂白粉更高效的饮用水消毒剂“ClO2”,其反应的微观过程图如下:

(其中 表示氯原子,●表示钠原子, 表示氧原子)
表示氧原子)
试回答:ClO2叫做 ,其中氯的化合价为 。
根据反应的微观过程图写出反应的化学方程式为 。
②国家药监局公布的抗震救灾急需药械目录中包括:一次性防护服、活性炭防护口罩、骨科内外固定材料等。其中防护口罩主要是利用活性炭的 性。
③地震发生后,全国各地为灾区紧急提供包括方便面在内的各种救灾物品。据下表回答:
| 方便面营养成分表(每100g中含量) | |||||||||
| 糖类 | 脂肪 | 蛋白质 | 水分 | 钠 | 钾 | 磷 | 钙 | 维生素C | 其他 |
| 61.6 | 21.1 | 9.5 | 3.6 | 1144 | 134 | 80 | 25 | 0 | … |
方便面所含的营养素主要有蛋白质、 、油脂、无机盐和水。
(2)有机高分子材料、金属材料和无机非金属材料是人类使用的三大类基础材料,它们以各自的特点满足着人类多方面的需要。
①有机高分子材料“玉米塑料”因其可降解被广泛用来替代一次性泡沫塑料,“玉米塑料”的使用可减少“ 污染”。
②金属材料中,有一类贮氢合金能够结合氢气形成金属化合物,并在一定条件下分解释放出氢气,该贮运原理属于 变化(选填“物理”或“化学”)。
③无机非金属材料中,用于电子工业的高纯碳酸钙和高纯氧化钙生产流程如下:

实验室常采用 操作进行沉淀分离,生产高纯碳酸钙时,选择“220℃恒温干燥”,而不选择“高温”条件下完成此操作的原因是 (用化学方程式说明)。
(3)创新利用CO2,倡导低碳生活,发展低碳经济已成为一种环保时尚。现在许多城市倡导“135”出行,即1公里以内步行,3公里以内骑自行车,5公里乘坐公共交通工具,提倡“低碳城市”、“绿色出行”。
①为减少CO2排放,人们积极寻找不含碳元素的燃料。经研究发现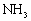 燃烧的产物没有污染,且释放大量能量,有一定应用前景。请将
燃烧的产物没有污染,且释放大量能量,有一定应用前景。请将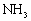 燃烧反应的化学方程式补充完整:
燃烧反应的化学方程式补充完整: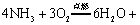 。
。
②法国化学家PaulSabatier采用“组合转化”技术使CO2和H2在催化剂作用下生成CH4和H2O。试写出该反应的化学方程式 。
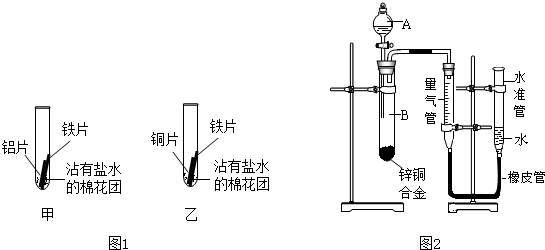
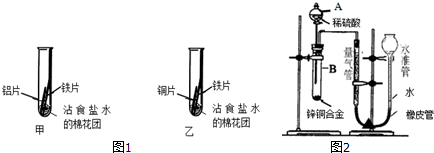
| 现象 | 分析 |
| 甲中:铝片表面出现灰白色物质,铁片表面几乎没有明显现象. | 铝与铁在潮湿的环境中接触,______首先被腐蚀. |
| 乙中:铁片表面出现______,铜片表面几乎没有明显现象. | 铁与铜在潮湿的环境中接触,铁首先被腐蚀. |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com