
题目列表(包括答案和解析)
在农业生产中,常用溶质质量分数为10%―20%的氯化钠溶液来选种。
(1)实验室现要配制16%的氯化钠溶液100g,需要氯化钠 g,水 ml。
(2)现有下列仪器:①药匙,②集气瓶,③烧杯,④试管,⑤玻璃棒,⑥量筒,⑦铁架台,⑧托盘天平,必须使用的仪器有 (填序号)。
(3)在配制过程中有下列操作步骤:①称量氯化钠,②量取水,③计算氯化钠质量和水的体积,④溶解并搅拌。其正确的操作顺序是 (填写序号)
(1)烧碱在工业上通常用电解饱和NaCl水溶液的方法制取,产物除烧碱外,还有H2和Cl2,请写出电解他和NaCl水溶液的化学方程式:________
(2)烧碱放在空气中会变质生成碳酸钠。现有14.6 g暴露在空气中的烧碱样品,全部溶于水,然后滴加足量Ca(OH)2溶液,充分反应后,过滤,烘干得10 g沉淀,则样品的组成为 ( )
A.全部为Na2CO3 B.4gNa2CO3和10.6gNaOH
C.全部为NaOH D.4g NaOH和10.6g Na2CO3
(3)酸碱中和反应在工农业生产和科研上具有很大用途,但氢氧化钠溶液和盐酸反应时看不到现象,请你设计一个实验,通过观察到的明显现象,说明氢氧化钠溶液与盐酸发生了反应。
______ __
(4)若中和反应需要60g 10%的NaOH溶液,现提供50g 20%的NaOH溶液、40g 5%的NaOH溶液以及足够的NaOH固体和水,请选用以上提供的药品涉及两种配制方案(只要说明配制所需的各种药品的用量)填入下表中
|
序号 |
配制方案 |
|
举例 |
6gNaOH固体和54g水 |
|
方案1 |
|
|
方案2 |
|
(5)下图是某学生用氢氧化钠固体和水配制60g10%的NaOH溶液的部分操作过程,该同学在称量氢氧化钠时,先在两个托盘上各放一张质量相同的纸,然后把药品直接放在纸上称量。

①操作中的错误是_______;
②下列操作中导致溶质质量分数偏低的是_______。(填字母)
A.a操作中砝码和氢氧化钠放错盘
B.b中烧杯用水洗涤后未干燥就使用
C.c操作中平视量筒凹液面最低处读数为50mL
D.d操作中有少量水溅出
水和溶液在生命活动和生产、生活中起着十分重要的作用.
(1)“生命吸管”(如下图)是一种可以随身携带的小型水净化器,里面装有网丝、注入了活性炭和碘的树脂等.其中活性炭起到________和过滤作用.

(2)水常用来配制各种溶液,硝酸钾溶液中的溶质为________.
(3)农业生产常用溶质的质量分数为10%~20%的NaCl溶液来选种.现将300 g 25%的NaCl溶液稀释为15%的NaCl溶液,需要加水的质量为________g.
(4)根据下表回答问题.
①60℃时,向两个分别盛有50 g NaCl和NH4Cl的烧杯中,各加入100 g的水,充分溶解后,为饱和溶液的是________溶液.
②采用一种操作方法,将上述烧杯中的剩余固体全部溶解,变为不饱和溶液.下列说法正确的是________(填字母序号)
A.溶质的质量不变
B.溶液中溶质的质量分数一定减小
C.溶液质量可能不变
D.可升高温度或增加溶剂
(7分)中和反应是中学化学中重要的学习内容,其在日常生活和工农业生产中有广泛的应用。
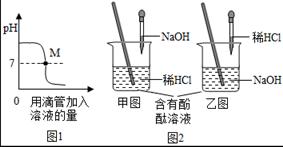
(1)下图表示盐酸和氢氧化钠溶液发生反应过程中溶液的pH的变化曲线。请从曲线图中获取信息,回答下列问题: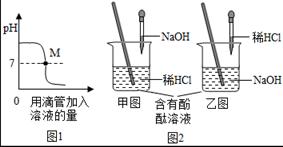
①图1图象表示盐酸和氢氧化钠溶液发生反应过程中溶液的pH变化。进行该反应的实验操作是按照图2中的 (填甲或乙)图所示进行的。
②曲线上M点表示 。
③向烧杯中倾倒20g质量分数为4.00%的氢氧化钠溶液,滴入3滴酚酞试液,振荡,再逐滴滴入质量分数为3.65%的稀盐酸,边滴边振荡,直至溶液刚好变为 色为止,共用去稀盐酸20g,则反应后溶液中溶质质量分数为 (结果精确到0.1%)。
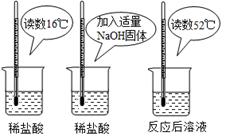
(2)为证明中和反应是放热反应,某小组进行了如图所
示的实验操作: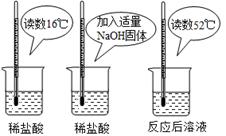
根据上图实验,甲同学认为:NaOH与稀盐酸发生的中和反应是放热反应。乙同学认为:甲同学得出
这个结论的依据不科学,理由是 。
(3)为探究影响中和反应放出热量多少的因素,他们又进行了如下实验:在编号为A、B、C、
D、E的五只烧杯中各装入36.5g 溶质质量分数为5%、10%、15%、20%、25%的盐酸,
再向上述五只烧杯中分别加入40g20% 的氢氧化钠溶液,最后测量其温度,数据记录如下:
| 烧杯编号 | A | B | C | D | E |
| 盐酸的溶质质量分数 | 5% | 10% | 15% | 20% | 25% |
| 反应后溶液温度(℃) | 24℃ | 34℃ | 46℃ | 54℃ | 54℃ |
| 烧杯编号 | A | B | C | D | E |
| 盐酸的溶质质量分数 | 5% | 10% | 15% | 20% | 25% |
| 反应后溶液温度(℃) | 24℃ | 34℃ | 46℃ | 54℃ | 54℃ |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com