
题目列表(包括答案和解析)

氢氧化钠固体及溶液在空气中很容易发生变质生成碳酸钠。
(1)甲同学在实验室里发现一瓶敞口放置的氢氧化钠溶液,对其变质情况进行了如下探究。
【猜想与假设】该氢氧化钠溶液已部分变质。
【实验与结论】
| 实验步骤 | 实验现象 | 实验结论 |
| a.取少量该溶液于一支试管中,加入 |
| 该氢氧化钠溶液已变质 |
| b.将步骤a所得的液体静置,取上层清液于另一支试管中,滴加 |
| 该氢氧化钠溶液已部分变质 |
【拓展探究】甲同学又尝试通过实验除去该氢氧化钠溶液中含有的碳酸钠,方案如下:
向该溶液中加入 ,充分反应后,经 操作,即可除去该氢氧化钠溶液中含有的杂质。
(2)乙同学在实验室里发现少量部分变质的氢氧化钠固体,尝试通过实验测定其中碳酸钠的质量分数。
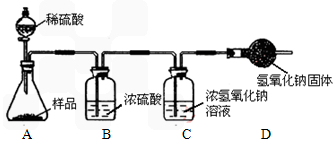
【设计和进行实验】乙同学设计了下图所示的实验装置(铁架台、铁夹等固定用装置已略去,碱石灰是固体氢氧化钠和生石灰的混合物)。取10.0g待测样品,进行实验。

实验步骤如下:
a.连接好装置,并检查气密性;
b.打开弹簧夹,缓缓通入一段时间空气;
c.称量装置D的质量为83.4g;
d.关闭弹簧夹,慢慢滴加Y溶液,至不再产生气泡为止;
e.打开弹簧夹,再次缓缓通入一段时间空气;
f.再次称量装置D的质量为84.5g。
【交流讨论】
①试剂X、Y、Z依次最适宜选用 (选填字母)。
A.氢氧化钠溶液 浓盐酸 浓硫酸 B.澄清石灰水 稀盐酸 稀硫酸
C.氢氧化钠溶液 稀硫酸 浓硫酸 D.浓硫酸 稀硫酸 氢氧化钠溶液
②步骤e中通入空气的作用是 。
③若没有装置C,则会导致测定结果 (选填“偏大”、“偏小”或“无影响”,下同);若没有装置E,则会导致测定结果 。
【数据处理】根据实验中测得的有关数据,计算部分变质的氢氧化钠固体中碳酸钠的质量分数。
氢氧化钠是一种重要的化工原料.
①少量氢氧化钠可用石灰石、水、纯碱(Na2CO3)为原料制取,流程如下:
Ⅰ.用化学方程式表示白色固体加入纯碱溶液后所有发生的化学反应 、 .
Ⅱ.滤液中存在少量的Na2CO3,用适量 试剂可以去除该物质.
②为测定某部分变质的氢氧化钠固体中氢氧化钠的质量分数,设计以下装置进行实验(假设每步实验都完全进行,浓硫酸具有吸水性).
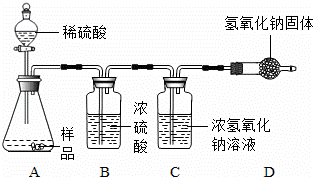
Ⅰ.要确定该样品中氢氧化钠的质量分数,所需要的数据是 .
A.固体样品的质量 B.浓硫酸实验前后质量 C.浓氢氧化钠溶液实验前后质量
D.所用稀硫酸质量 E.仪器D中氢氧化钠固体实验前后质量 F.稀硫酸质量分数
Ⅱ.D装置的作用是 .没有D装置对氢氧化钠质量分数的测定结果影响是 (填“偏大”“偏小”或“不变”).
氢氧化钠是一种重要的化工原料。
①少量氢氧化钠可用石灰石、水、纯碱(Na2CO3)为原料制取,流程如下:
Ⅰ.用化学方程式表示白色固体加入纯碱溶液后所有发生的化学反应 (10) 。
Ⅱ.滤液中存在少量的Na2CO3,用适量 (11) 试剂可以去除该物质。
②为测定某部分变质的氢氧化钠固体中氢氧化钠的质量分数,设计以下装置进行实验(假设每步实验都完全进行,浓硫酸具有吸水性)。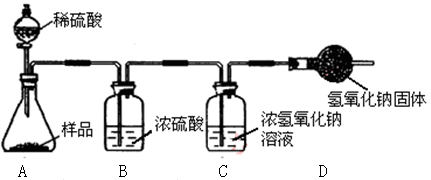
Ⅰ. 要确定该样品中氢氧化钠的质量分数,所需要的数据是 (12)
| A.固体样品的质量 |
| B.浓硫酸实验前后质量 |
| C.浓氢氧化钠溶液实验前后质量 |
| D.所用稀硫酸质量 |
氢氧化钠是一种重要的化工原料。
①少量氢氧化钠可用石灰石、水、纯碱(Na2CO3)为原料制取,流程如下:

Ⅰ.用化学方程式表示白色固体加入纯碱溶液后所有发生的化学反应 (10) 。
Ⅱ.滤液中存在少量的Na2CO3,用适量 (11) 试剂可以去除该物质。
②为测定某部分变质的氢氧化钠固体中氢氧化钠的质量分数,设计以下装置进行实验(假设每步实验都完全进行,浓硫酸具有吸水性)。
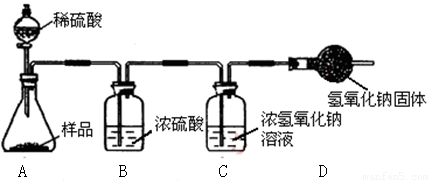
Ⅰ. 要确定该样品中氢氧化钠的质量分数,所需要的数据是 (12)
A.固体样品的质量
B.浓硫酸实验前后质量
C.浓氢氧化钠溶液实验前后质量
D.所用稀硫酸质量
E.仪器D中氢氧化钠固体实验前后质量
F.稀硫酸质量分数
Ⅱ. D装置的作用是 (13) 。没有D装置对氢氧化钠质量分数的测定结果影响是 (14) (填“偏大”“偏小”或“不变”)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com