
题目列表(包括答案和解析)
 肥田粉是常用的氮肥,如图为某品牌肥田粉的部分标签,为了计算该品牌肥田粉的纯度(样品中硫酸铵的质量分数),小玉和小昊采用了两种不同的方法.
肥田粉是常用的氮肥,如图为某品牌肥田粉的部分标签,为了计算该品牌肥田粉的纯度(样品中硫酸铵的质量分数),小玉和小昊采用了两种不同的方法. ×100%
×100%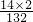 ×100%
×100%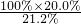 =94.3%
=94.3% ×100%
×100%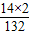 ×100%
×100%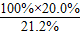 =94.3%
=94.3%
| 2×N原子的相对原子质量 |
| (NH4)2SO4相对分子质量 |
| 14×2 |
| 132 |
| 100%×20.0% |
| 21.2% |

 肥田粉是常用的氮肥,如图为某品牌肥田粉的部分标签,为了计算该品牌肥田粉的纯度(样品中硫酸铵的质量分数),小玉和小昊采用了两种不同的方法.
肥田粉是常用的氮肥,如图为某品牌肥田粉的部分标签,为了计算该品牌肥田粉的纯度(样品中硫酸铵的质量分数),小玉和小昊采用了两种不同的方法.| 2×N原子的相对原子质量 |
| (NH4)2SO4相对分子质量 |
| 14×2 |
| 132 |
| 100%×20.0% |
| 21.2% |
| N的相对原子质量×2 |
| (NH2)2SO4的相对分子质量 |
| 14×2 |
| 132 |
| 7.08g |
| 7.5g |
| ||
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com