
题目列表(包括答案和解析)
 通过学习,同学们应该知道有多种途径可以制取氧气.如:
通过学习,同学们应该知道有多种途径可以制取氧气.如:
| ||
| ||
| 加热 |
| 加热 |
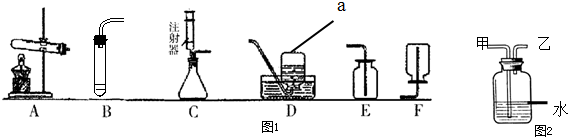
实验室常用加热氯酸钾和二氧化锰混合物的方法制取氧气,请回答下列问题:
A B C D E
⑴反应的化学方程式为 。
⑵写出下列编号仪器的名称a________________ b_______________。
⑶用所给仪器组装用上述反应制氧气的装置,你选择的发生装置为________,B装置试管口要略
向下倾斜的原因是_______________________________________________;收集装置为__________。
上述装置选择的依据是 (填字母)。
| A.属于固固型加热的反应 | B.属于固液型不加热的反应 |
| C.制取的气体密度比空气大 | D.制取的气体难溶于水 |

|
| 实验序号 | 二氧化锰与氯酸钾的质量比 | 用时(秒) |
| 1 | 6:6 | 42 |
| 2 | 2.5:5 | 25 |
| 3 | 2:5 | 34 |
| 4 | 3:10 | 65 |
| 5 | 2:10 | 41 |
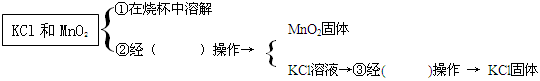
 通过常见盐知识的学习,我们知道Na2CO3和NaHCO3有一些相似的化学性质.(1)甲同学为了探究它们的水溶液都显碱性,用两只干净的试管各取两种溶液少许,分别用________蘸取少许溶液滴在pH试纸上,然后与标准比色卡比较,pH________7.
通过常见盐知识的学习,我们知道Na2CO3和NaHCO3有一些相似的化学性质.(1)甲同学为了探究它们的水溶液都显碱性,用两只干净的试管各取两种溶液少许,分别用________蘸取少许溶液滴在pH试纸上,然后与标准比色卡比较,pH________7.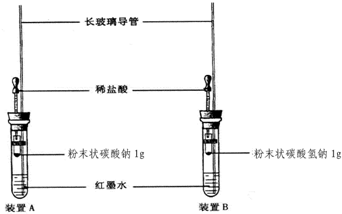
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com