
题目列表(包括答案和解析)

| 加热 |
| 加热 |
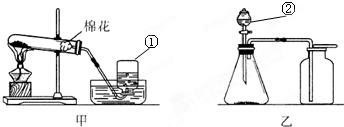


实验室常用于制取氧气的方法有:a、加热氯酸钾晶体和二氧化锰粉末;b、加热高锰酸钾固体;c、混合二氧化锰粉末与过氧化氢(H2O2)溶液分解产生水和氧气。
(1)写出指定的仪器名称
① ②
(2)请仔细分析装置甲的特点,推测其所用的制氧气的方法是________(填a、b或c)
(3)采用方法c制取氧气应该选用装置___________(填“甲”或“乙”)。为检验装置乙中氧气是否收集满,可用带火星的木条放在集气瓶的_______,这是利用了氧气_______的性质。
(4)利用装置甲制氧气,甲中发生的反应的文字表达式: ,该反应属于 反应,在结束实验时要先撤离导管出水面,再熄灭酒精灯,其目的是______________________________________。
(5)利用乙装置制氧气的优点有: ,a和c两制氧方法中二氧化锰的共同作用都是 。

| 方案 | 选用的药品 | 选用的实验装置及组装时接口连接顺序 | 需测得的实验数据(从上述可测得的数据中选取) | 混合物中Na2CO3的质量分数计算式 | |
| 选用的实验装置序号 | 组装时接口编号顺序 | ||||
| 一 | ________ | A、B、D、F | (毋须填写) | ________ | ________ |
| 二 | ________ | ________ | ________ | ag、cg、dg | ________ |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com