
题目列表(包括答案和解析)
用下列物质的序号回答有关问题:
(1)已知“○”、“●”表示质子数不同的原子。下列各图表示的物质中,属于化合物的是________;属于混合物的是_______。
 |
(2)有下列物质:
①雨水 ②蒸馏水 ③雨后洁净的空气 ④四氧化三铁
⑤液氮 ⑥高锰酸钾完全分解后的固体产物
其中属于混合物是 ,属于单质的是 ,属于氧化物的是 。
下表是NaCl和KCl的溶解度数据,请回答下列问题。
| 温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度 (g) | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.2 |
| KCl | 27.6 | 34.0 | 40.0 | 45.5 | 51.1 | 56.7 |
(1)40℃时,氯化钠的溶解度是 g。
(2)将80℃时, 同质量的NaCl和KCl的饱和溶液,分别冷却到0℃,析出晶体最多的是_ (填“NaCl”或“KCl”)溶液。
(3)20℃时,向两只分别盛有35 g NaCl和KCl固体的烧杯中,各加入100g水,充分溶解后,能形成饱和溶液的物质是 ,其溶液的溶质质量分数是______(精确到0.1%)。
(4)温度不变的情况下,若要将接近饱和的KCl溶液变成饱和溶液,可采用的方法是_______________。(写一种)
 Ⅱ.(6分)阅读下列三段材料,回答问题:
Ⅱ.(6分)阅读下列三段材料,回答问题:
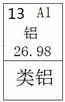
材料一:l869年,俄国化学家门捷列夫对已发现的元素进行研究,制作了元素周期表(右表是其片断),并在他的元素周期表中留下了许多空位代表尚未发现的新元素,其中就预言了“类铝”这种新元素。
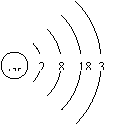 材料二:l875年,法国化学家布瓦博德朗公布了他发现的新元素镓(元素符号为Ga)的性质:镓是银白色金属,密度4.7g·cm-3,能与水剧烈反应生成氢气和氢氧化镓。不久,他收到门捷列夫的来信称:镓就是我预言的“类铝”,其密度应在5.9-6.0 g·cm-3之间。
材料二:l875年,法国化学家布瓦博德朗公布了他发现的新元素镓(元素符号为Ga)的性质:镓是银白色金属,密度4.7g·cm-3,能与水剧烈反应生成氢气和氢氧化镓。不久,他收到门捷列夫的来信称:镓就是我预言的“类铝”,其密度应在5.9-6.0 g·cm-3之间。
材料三:l876年,布瓦博德朗将金属镓提纯后测得镓的密度为
5.94g·cm-3,从而验证了元素周期表的正确性。随后科学家根据元素
周期表的空位,按图索骥,发现了许多新元素。目前金属镓广泛用于
制造半导体材料。镓的原子结构示意图如右图所示。
(1)镓元素的质子数为__________,其氯化物的化学式为_____________。
(2)请根据上述材料,小结金属镓的有关知识:
① 物理性质:镓是银白色金属,密度为5.94g·cm -3
-3
② 化学性质(请用化学方程式表示):_____________________________________;
③ 用途:____________________________________。
下表是NaCl和KCl的溶解度数据,请回答下列问题。
| 温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度 (g) | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.2 |
| KCl | 27.6 | 34.0 | 40.0 | 45.5 | 51.1 | 56.7 |
(1)40℃时,氯化钠的溶解度是 g。
(2)将80℃时, 同质量的NaCl和KCl的饱和溶液,分别冷却到0℃,析出晶体最多的是_ (填“NaCl”或“KCl”)溶液。
(3)20℃时,向两只分别盛有35 g NaCl和KCl固体的烧杯中,各加入100g水,充分溶解后,能形成饱和溶液的物质是 ,其溶液的溶质质量分数是______(精确到0.1%)。
(4)温度不变的情况下,若要将接近饱和的KCl溶液变成饱和溶液,可采用的方法是_____
___________。(写一种)
 Ⅱ.(6分)阅读下列三段材料,回答问题:
Ⅱ.(6分)阅读下列三段材料,回答问题:
材料一:l869年,俄国化学家门捷列夫对已发现的元素进行研究,制作了元素周期表(右表是其片断),并在他的元素周期表中留下了许多空位代表尚未发现的新元素,其中就预言了“类铝”这种新元素。
 材料二:l875年,法国化学家布瓦博德朗公布了他发现的新元素镓(元素符号为Ga)的性质:镓是银白色金属,密度4.7g·cm-3,能与水剧烈反应生成氢气和氢氧化镓。不久,他收到门捷列夫的来信称:镓就是我预言的“类铝”,其密度应在5.9-6.0 g·cm-3之间。
材料二:l875年,法国化学家布瓦博德朗公布了他发现的新元素镓(元素符号为Ga)的性质:镓是银白色金属,密度4.7g·cm-3,能与水剧烈反应生成氢气和氢氧化镓。不久,他收到门捷列夫的来信称:镓就是我预言的“类铝”,其密度应在5.9-6.0 g·cm-3之间。
材料三:l876年,布瓦博德朗将金属镓提纯后测得镓的密度为
5.94g·cm-3,从而验证了元素周期表的正确性。随后科学家根据元素
周期表的空位,按图索骥,发现了许多新元素。目前金属镓广泛用于
制造半导体材料。镓的原子结构示意图如右图所示。
(1)镓元素的质子数为__________,其氯化物的化学式为_____________。
(2)请根据上述材料,小结金属镓的有关知识:
① 物理性质:镓是银白色金属,密度为5.94g·c m-3
m-3
② 化学性质(请用化学方程式表示):_____________________________________;
③ 用途:____________________________________。


(7分)水是人类生活中不可缺少的物质。
(1)下列日常生活和生产中常见的水,属于纯净物的是___ ____。
A. 矿泉水 B. 蒸馏水 C. 河水 D. 雨水
(2)如右图所示的简易净化水的装置,运用了如下净水方法中的___ ____ (填序号)。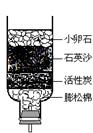
A、消毒 B、过滤 C、蒸馏 D、吸附
(3)某同学设计了电解水简易装置,其中A、B电极由金属曲别针制成。通电一段时间后的现象如图所示,则与电源负极相连的是___ ____电极[填A或B],发生反应的化学方程式为___ ____。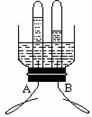
(4)自来水中含有少量Ca(HCO3)2等可溶性化合物,烧水时Ca(HCO3)2发生分解反应,生成难溶性的碳酸钙、水和二氧化碳。请写出Ca(HCO3)2受热分解的化学方程式___ ____;若洁厕灵的主要成分是盐酸,则用洁厕灵除水垢的化学方程式为___ ____。
(5)根据上述电解水实验现象,若已知水的相对分子质量为18,标准状况下氢气密度:0.089g/L,氧气密度:1.429g/L。则计算一个水分子中氧原子个数的数学表达式为___ ____。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com