
题目列表(包括答案和解析)
(7分)铁和铜是生产生活中常见的金属.
(1)能有效防止铁制品生锈的措施是_______
| A.家用水龙头镀铬 | B.汽车表面喷漆打蜡 |
| C.自行车链条涂油 | D.菜刀用后洗净擦干 |

铁和铜是我们熟悉的金属。
(1)下列生活中的铁、铜制品,主要利用了它们的________性和________性。
(2)铁是使用量很大的金属。
①工业上用赤铁矿(主要成分Fe2O3)炼铁的化学方程式是________________。
②铁制品容易生锈,铁生锈的条件是________________。防止铁生锈的具体措施有________________(举1例即可)。
③稀硫酸可用于除铁锈,该反应的化学方程式是________________。
(3)铜是人类认识并应用最早的金属。某小组同学用下图所示装置(夹持仪器略去)模拟“湿法炼铜”。
①从装有过量铁屑和铁粉的异形玻璃管上端加入硫酸铜溶液。发生反应的化学方程式是________________________。该反应属于的基本反应类型是________;实验过程中观察到的现象是________________________________。
②反应结束后,将固体从异形玻璃管中取出,放于烧杯中;向烧杯中加入足量的试剂A,过滤得到铜。该试剂A是________。
水和二氧化碳而变质。某实验小组为确定一瓶久置的碱石灰样品的成分,设计了如图所示实验流程。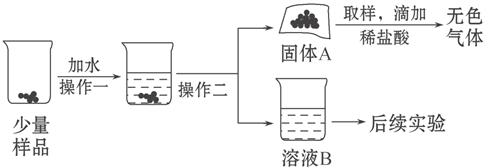
请你参与探究过程:
(1)为了使样品充分溶解,操作一还要用到的玻璃仪器是 ;操作二的名称是 。
(2)固体A中一定含有 。
(3)溶液B成分的探究:
【查阅资料】①Ca(OH)2、Na2CO3溶于水无明显的温度变化;
②Na2CO3溶液呈碱性,能使酚酞试液变红;
③CaCl2溶液呈中性。
【猜想】溶液B中的溶质可能为:①NaOH ②Na2CO3
③NaOH和Na2CO3④Ca(OH)2和 (填化学式)。
【设计方案并进行实验】甲、乙同学分别设计如下方案并进行探究:
甲同学:取少量溶液B于试管中,滴加足量的稀盐酸,产生大量气泡,则溶液B中的溶质是Na2CO3。
乙同学:取少量溶液B于试管中,滴加几滴酚酞试液,溶液变成红色,则溶液B中的溶质一定含有NaOH。
【反思与评价】丙同学认真分析上述两位同学的实验,认为他们的结论均有不足之处,并且做出了正确的判断。他认为溶液B中的溶质一定含有Na2CO3,可能含有NaOH。为进一步确认溶液B中是否含NaOH,他做了如下实验。
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量溶液B于试管中,加入足量CaCl2溶液 ②过滤,在滤液中滴加酚酞试液 | ①有白色沉淀生成 ②溶液由无色变为红色 | 猜想③正确 |
风和日丽的假日,同学们相约去湖边烧烤。
(1)小黄采购食物时,已购买了土豆、牛肉、虾和黄油,就营养均衡的角度而言,还应采购 (填字母);
| A.鲫鱼 | B.青椒 | C.鸡翅 | D.面包 |
水和溶液在生命活动和生产、生活中起着十分重要的作用。
(1)净水器中经常使用活性炭,主要利用活性炭的 性。
(2)下图实验中,当试管1中气体的体积为6mL时,试管2中气 体体积约为 mL;反应的化学方程式是 。
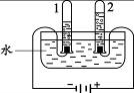
(3)农业生产常用溶质的质量分数为10% ~ 20%的NaCl溶液来选种。现将300g 25%的NaCl溶液稀释为10%的NaCl溶液,需要加水的质量为 g。
(4)甲、乙两物质的溶解度曲线如右图所示。20℃时,将等质量的甲、乙两种固体,分别加入盛有10 g水的A、B试管中,充分溶解后,可观察到如图所示的现象。则20℃ t℃(填“>”、“<”或“=”)。
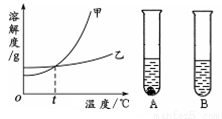
20℃时,对A试管进行如下操作,最终A试管中溶液
溶质的质量分数一定发生变化的是 (填字母序号)。
A.加少量水 b.加入少量甲物质
c.升温到40℃ d.蒸发部分溶剂,恢复到20℃
e.加入少量40℃甲的饱和溶液,恢复到20℃
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com