13、金属是现代生活、工业生产以及科学研究中应用极为普遍的一类材料.

(1)青少年看书、写字一定要爱护眼睛,台灯是在光线不足时常用的照明用具.
①图1中标示的物质属于金属材料的有
①②④
(填序号).
②灯管后面的反光片为铝箔.铝块能制成铝箔是利用了铝的
延展
性.
③铝比铁活泼,但铝箔却比铁螺丝钉耐腐蚀,其原因是
铝与氧气反应表面形成致密氧化膜(表述合理即可);
.
(2)已知在相同的条件下,金属的活动性越强,金属和酸反应产生气泡(氢气)的速度就越快.Mg、Cu、Fe三种金属在稀盐酸里的反应现象如图2所示.
①如图中Y所代表的金属是
Cu
(填“Mg”或“Cu”或“Fe”);
②Mg、Cu、Fe三种金属的活动性由强到弱的顺序为
Mg>Fe>Cu
;
(3)金属的开发和利用是人类文明和社会进步的标志.
①我国古代将炉甘石(ZnCO
3)、赤铜矿(Cu
2O)和木炭粉混合加热至800℃左右,即可得到与黄金外观相似的“药金”.
I.该方法不能制得金(Au)是因为
反应物中不含有金元素
;
II.“药金”是
合金
(填“纯金属”或“合金”);
②钛因常温下不与酸、碱反应等优良的性能,被誉为“未来金属”.由钒钛磁铁矿提取金属钛的主要工艺过程如下:

I.TiCl
4在高温下与足量Mg反应置换生成金属Ti,该反应的化学方程式为:
TiCl4+2Mg═Ti+2MgCl2;
.
II.上述生产过程中得到的金属钛中混有少量金属杂质,可加入
稀盐酸(或稀硫酸)
除去.
(4)已知某金属粉末中除含有Al外还含有一定量的Fe和Cu,为证明Fe和Cu的存在,某化学兴趣小组的同学展开了如下的实验探究.
资料在线:Al与氢氧化钠溶液反应生成溶于水的偏铝酸钠和氢气(反应的化学方程式为:2Al+2H
2O+2NaOH═2NaAlO
2+3H
2↑),Fe和Cu不与氢氧化钠溶液反应.
请完成证明金属粉末中存在Fe和Cu的实验设计:
| 实验操作 |
实验现象 |
结论 |
| I.取少量的金属粉末于试管中,加入足量的 氢氧化钠溶液 (填试剂名称). |
有气泡产生(或固体减少) |
仅除去铝 |
| II.将试管静置,弃去上层清液,加入足量的稀硫酸. |
有气泡产生(或固体减少或产生浅绿色溶液). |
证明含有铁 |
| III.将试管静置,弃去上层清液,加水,多次洗涤剩余固体 |
剩余固体呈紫红色 |
证明含有铜 |

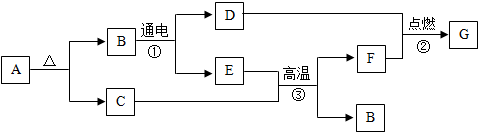
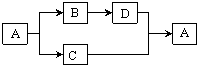 25、A~D都是初中化学中的常见物质,且有如图所示转化关系(反应条件、其他反应物及多余产物均已略去).请按要求写出下列物质的 化学式和化学方程式:
25、A~D都是初中化学中的常见物质,且有如图所示转化关系(反应条件、其他反应物及多余产物均已略去).请按要求写出下列物质的 化学式和化学方程式:
