
题目列表(包括答案和解析)
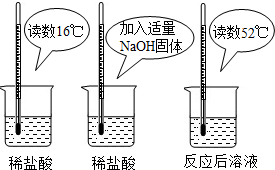
| 烧杯编号 | A | B | C | D | E |
| 盐酸的溶质质量分数 | 5% | 10% | 15% | 20% | 25% |
| 反应后溶液温度(℃) | 24℃ | 34℃ | 46℃ | 54℃ | 54℃ |
 为测定某氢氧化钠溶液中NaOH的质量分数,小江同学用7.3%的稀盐酸与20g待测氢氧化钠溶液反应,并绘制溶液pH随加入稀盐酸质量变化的图象(如图).
为测定某氢氧化钠溶液中NaOH的质量分数,小江同学用7.3%的稀盐酸与20g待测氢氧化钠溶液反应,并绘制溶液pH随加入稀盐酸质量变化的图象(如图).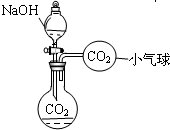
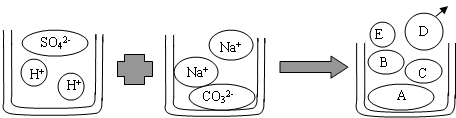
| 实验目的 | 实验步骤 | 预计现象 |
| 除尽溶液中的CO32- | ①:取少量烧瓶中的溶液于试管中,滴加足量的______试 剂 | 有白色沉淀产生 |
| 证明溶液中尚存NaOH | ②:将上述实验所得混合物过滤后观察滤液 | ______________ |
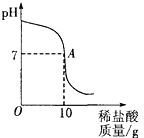 为测定某氢氧化钠溶液中NaOH的质量分数,小江同学用7.3%的稀盐酸与20g待测氢氧化钠溶液反应,并绘制溶液pH随加入稀盐酸质量变化的图象(如图).
为测定某氢氧化钠溶液中NaOH的质量分数,小江同学用7.3%的稀盐酸与20g待测氢氧化钠溶液反应,并绘制溶液pH随加入稀盐酸质量变化的图象(如图).
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com