
题目列表(包括答案和解析)
 下面是有关“神舟七号”飞船的三张资料图片
下面是有关“神舟七号”飞船的三张资料图片
 (2012?湖州)用过氧化氢制氧气时,有同学对事先在烧瓶中加水产生了疑问.他提出了猜想:
(2012?湖州)用过氧化氢制氧气时,有同学对事先在烧瓶中加水产生了疑问.他提出了猜想:| 实验 | 1 | 2 | 3 | 4 | 5 |
| 过氧化氢溶液溶质质量分数 | 1% | 3% | 5% | 10% | 15% |
| MnO2粉末用量/克 | 0.5 | 0.5 | 0.5 | 0.5 | 0.5 |
| 收集到500mL气体时所用时间/秒 | 560 | 186 | 103 | 35 | 12 |
| 反应后液体温度/℃ | 26 | 38 | 43 | 59 | 71 |
| ||
| ||
| 物质 | Na2SO4 | Na2CO3 | NaHCO3 |
| 溶解度/g | 19.5 | 21.5 | 9.6 |
| 实 验 步 骤 | 实 验 现 象 | 实 验 结 论 |
| 取少量溶液于试管中,加稀盐酸 | 溶液有气泡产生 | 该溶液是________溶液 |
 与足量的氢氧化钡溶液反应,理论上能产生多少克沉淀?
与足量的氢氧化钡溶液反应,理论上能产生多少克沉淀?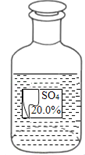

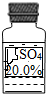 小华同学在化学实验室发现一瓶盛有无色溶液的试剂瓶,其标签严重破损(如右图所示).老师告诉他,这瓶试剂可能是硫酸、硫酸钠、硫酸镁溶液中的一种.小华同学通过查阅资料得知,常温下这三种物质的溶解度如下表:
小华同学在化学实验室发现一瓶盛有无色溶液的试剂瓶,其标签严重破损(如右图所示).老师告诉他,这瓶试剂可能是硫酸、硫酸钠、硫酸镁溶液中的一种.小华同学通过查阅资料得知,常温下这三种物质的溶解度如下表:| 物质 | H2SO4 | Na2SO4 | MgSO4 |
| 溶解度/g | 与水任意比互溶 | 19.0 | 39.0 |
| 实 验 步 骤 | 实 验 现 象 | 实 验 结 论 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com