
题目列表(包括答案和解析)
 化学是一门综合学科,学习过程中既能培养你较强的定性分析能力,又能提升你熟练的定量计算能力.下面设置了两道综合应用题,请你自主选择其中一道题解答(多选不加分).
化学是一门综合学科,学习过程中既能培养你较强的定性分析能力,又能提升你熟练的定量计算能力.下面设置了两道综合应用题,请你自主选择其中一道题解答(多选不加分).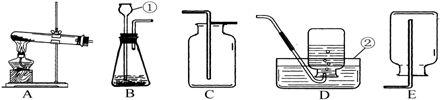
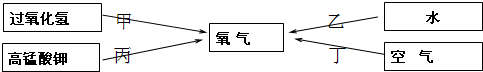
| 加热 |
| 加热 |
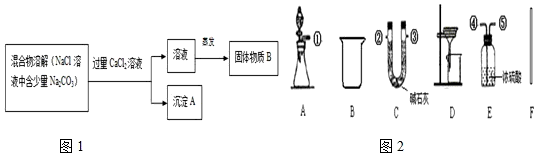
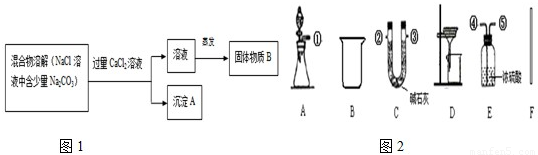
| 方案 | 选用的药品 | 选用的实验装置及组装时接口连接顺序 | 需测得的实验数据(从上述可测得的数据中选取) | 混合物中Na2CO3的质量分数计算式 | |
| 选用的实验装置序号 | 组装时接口编号顺序 | ||||
| 一 | ________ | A、B、D、F | (毋须填写) | ________ | ________ |
| 二 | ________ | ________ | ________ | ag、cg、dg | ________ |
化学是一门综合学科,学习过程中既能培养你较强的定性分析能力,又能提升你熟练的定量计算能力。下面设置了两道综合应用题,请你自主选择其中一道题解答(多选不加分)。
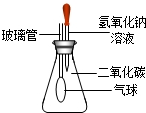
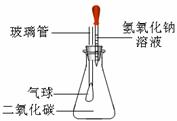
(1)某同学为探究氢氧化钠溶液的性质,进行如右图实验,将10g质量分数为40%氢氧化钠溶液滴入锥形瓶中试根据要求,回答下列问题:
①写出观察到的一项实验现象:________ ___ 。
②滴入氢氧化钠溶液,反应结束后,整个装置的质量与之前相比较_______(填写下列各项的序号)。
a.没有变化 b.有变化,后者质量变小
c.有变化,后者质量变大 d.不能确定
③若氢氧化钠溶液完全反应,二氧化碳仍有剩余,试通过计算,求此时所得不饱和溶液中溶质的质量。
(2)某校学习小组的同学要配制氯化钙溶液,药品柜中可供选择的药品有氢氧化钙、氧化钙、碳酸钙三种固体及一定溶质质量分数的稀盐酸。同学们交流讨论后,选择了一种固体药品并称取该固体15.4g加入烧杯中,再向其中加入100g稀盐酸,恰好完全反应,反应后溶液质量为111g。请根据题目中数据的变化分析回答下列问题:
①同学们选择的固体药品是 ;
②该实验过程看到的一项明显现象是
③请写出题中发生反应的化学方程式 ;
④所配制氯化钙溶液的溶质质量分数为多少?(写出解题过程)
| 方案 | 选用的药品 | 选用的实验装置及组装时接口连接顺序 | 需测得的实验数据(从上述可测得的数据中选取) | 混合物中Na2CO3的质量分数计算式 | |
| 选用的实验装置序号 | 组装时接口编号顺序 | ||||
| 一 | ______ | A、B、D、F | (毋须填写) | ______ | ______ |
| 二 | ______ | ______ | ______ | ag、cg、dg | ______ |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com