
题目列表(包括答案和解析)


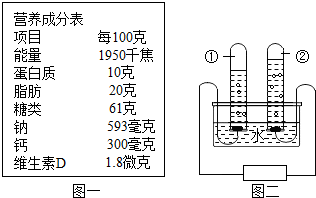 化学与生活密切相关.
化学与生活密切相关.| 序号 | 实验操作 | 主要实验现象 | 实验结论和解释 |
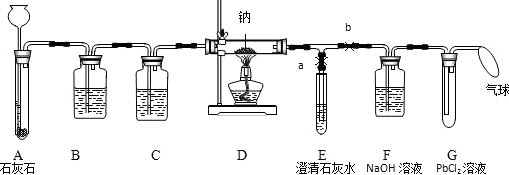
| ① | 打开a,关闭b,由长颈漏斗注入稀盐酸 | A中产生大量气泡 E中出现浑浊 |
A、E中反应的化学方程式分别为 CaCO3+2HCl=CaCl2+H2O+CO2↑ CaCO3+2HCl=CaCl2+H2O+CO2↑ 、CO2+Ca(OH)2=CaCO3↓+H2O CO2+Ca(OH)2=CaCO3↓+H2O |
| ② | 当E中出现混浊时,打开b,关闭a,点燃酒精灯 | D中Na剧烈燃烧,产生白烟内壁附着黑色、白色固体;G中产生黑色沉淀 | 反应产物一定有 C和CO C和CO |
| ③ | 取D中白色固体于试管中,加水溶解,再加入石灰水 | 产生白色沉淀 | 反应产物还有 Na2CO3 Na2CO3 |
| ||
| ||
| 分别向右侧溶液中 加入无色酚酞溶液 |
CaCl2 | NaCl | Na2CO3 | NaOH |
| 主要实验现象 | 无色 | 无色 | 由无色变为红色 | 由无色变为红色 |
| 序号 | 实验操作 | 主要实验现象 | 实验结论及解释 |
| ① | 打开a,关闭b,由长颈漏斗注入稀盐酸 | A中产生大量气泡 E中出现浑浊 |
E中反应的化学方程式为 CO2+Ca(OH)2═CaCO3↓+H2O CO2+Ca(OH)2═CaCO3↓+H2O |
| ② | 当E中出现浑浊时,打开b,关闭a,点燃酒精灯 | D中Na剧烈燃烧,产生白烟 内壁附着黑色、白色固体 G中产生黑色沉淀 |
反应产物一定 有 C C 和CO CO |
| ③ | 取D中白色固体于试管中,加水溶解,再加入CaCl2溶液 | 产生白色沉淀 | 反应产物还有 Na2CO3 Na2CO3 |

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com