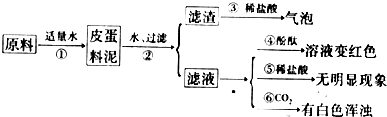
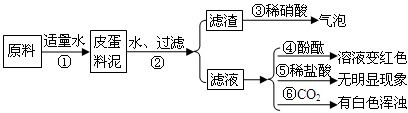
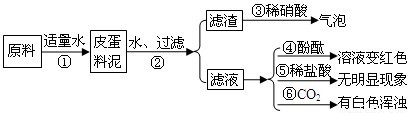
松花皮蛋是我们喜爱的食品,某小组同学查阅资料得知,制皮蛋料泥的原料主要是:生石灰、纯碱、食盐等.同学们对料泥进行了如下探究:
探究一:料泥的主要成份
| 实验步骤 |
实验现象 |
实验结论 |
| 1、将皮蛋料泥的原料放入烧杯中,加适量的水搅拌、充分反应 |
试管外壁 发热 发热 ,有白色沉淀生成 |
滤渣中一定有
CaCO3、Ca(OH)2 CaCO3、Ca(OH)2 . |
| 2、将上述烧杯中的物质过滤、洗涤,滤渣中滴加稀盐酸 |
有气泡冒出 |
| 3、取少量滤渣于试管中加水充分溶解,取上层清液滴加 酚酞试液 酚酞试液 |
上层清液由无色变成红色 |
| 4、取滤液三份,分别滴加酚酞、稀盐酸和通入CO2气体 |
溶液变红色、无明显现象、有白色浑浊 |
滤液中的溶质一定有 Ca(OH)2、NaOH Ca(OH)2、NaOH |
回答下列问题:
(1)请写出步骤①发生反应的化学方程式:
CaO+H2O═Ca(OH)2
CaO+H2O═Ca(OH)2
;
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
.
(2)由上述实验现象推断,料泥的主要成份是
NaOH、NaCl、CaCO3、Ca(OH)2
NaOH、NaCl、CaCO3、Ca(OH)2
.
探究二:测定料泥的原料中生石灰的含量(假设每步都能反应完全)
查阅资料:CaCO
3+CO
2+H
2O=Ca(HCO
3)
2实验步骤:
1.称得料泥原料的样品28g,放入烧杯中,加适量的水搅拌、充分反应.
2.向其中通入过量的CO
2,过滤,洗涤干燥后称得滤渣为5g
回答下列问题:
(1)通入过量的CO
2原因是
将氢氧化钙完全转变为碳酸钙沉淀
将氢氧化钙完全转变为碳酸钙沉淀
.
(2)利用测得的数据计算出料泥原料中生石灰的质量分数(要求写出计算过程).
思考:上述实验方案
不合理
不合理
(填合理或不合理).如不合理,原因是
可能有部分碳酸钙被通入的过量的二氧化碳转变成了可溶于水的碳酸氢钙
可能有部分碳酸钙被通入的过量的二氧化碳转变成了可溶于水的碳酸氢钙
;求出的值
偏小
偏小
(填偏大或偏小).
CaO+H
2O=Ca(OH)
2;CaCO
3+2HCl=CaCl
2+H
2O+CO
2↑
应用:你认为应该如何食用松花蛋?
蘸食醋食用
蘸食醋食用
,原因是
制作过程中生成碱性物质使其呈碱性
制作过程中生成碱性物质使其呈碱性
.