
题目列表(包括答案和解析)
小强家的电线晚上出了问题,几个电灯忽亮忽灭,忽明忽暗,爸爸说一定是电路中有接触不良的地方,他用干燥的木棍轻轻拨动屋檐下的电线,几经周折才恢复了正常.
第二天,小强帮电工师傅一起查找线路故障,他们检查了电线的每一部位,直到检查一处铜线和铝线的,接口处才发现了问题.他们发现上面“长满了”灰色、绿色的粉末.师傅说:“铝、铜的接口处易生锈,问题往往发生在这些地方.”小强对师傅的话半信半疑,又检查一遍,的确是铝铜接口处生了锈,而铝铝接口处和铜铜接口处都没有生锈.这是必然原因还是偶然原因造成的?只有铝铜接口处易生锈吗?不同金属的接口处都易生锈吗?
小强想通过实验解决这些问题.他找到了铜丝、铝丝、铁丝和锌条,用它们模仿自然条件下较长时间后导线接口处的生锈情况.
请你和小强完成下列问题:
(1)
怎样设计这个实验?请写出实验步骤和操作方法.(2)
通过几个月的观察,若得出“只要是不同种金属相连接,就比同种金属相连接容易生锈”的结论,那么上面所设计的实验在几个月后出现的现象应分别是什么?(3)
为避免类似小强家断电情况的发生,安装居民线路时,你能给电工师傅提出怎样的建议.(4)
在学习和生活接触到的用品中,还有类似现象发生吗(并举一例)?对防止这类锈蚀你有何建议?
| 实验操作 | 实验现象 | 实验结论 |
| 实验Ⅰ:把一小片pH试纸放在一块干净的玻璃片上,用玻璃棒蘸取沉淀溶解后的澄清溶液沾在试纸上,把试纸呈现的颜色与标准比色卡对照. | 测得被测液 pH=8 |
猜 想① 不成立 不成立 .(填“成立”或“不成立”) |
| 实验Ⅱ:取沉淀溶解成澄清的溶液于另一支试管中,加入 稀盐酸 稀盐酸 . |
有气体产生 | 猜想②成立. |
| 实验 装置 |
 |
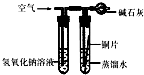 |
 |
 |
| 实验 现象 |
铜片不生锈 | 铜片不生锈 | 铜片不生锈 | 铜片生锈且水面 附近锈蚀最严重 |
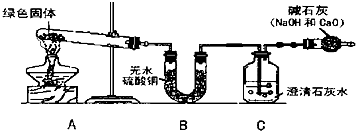
请你参与某学习小组的探究活动,并回答相关问题.
某化学兴趣小组的同学把氢氧化钠的片状固体放在表面皿中,离开实验室.三天后进行观察.
发现问题:三天后片状固体变成白色粉末状固体了
提出问题:“白色粉末固体物质是什么?”
建立假设:
设计实验:请你来完成以下实验,把相关内容填写在表格中.
| 实验方法及操作 | 可能观察到的现象 | 实验结论 |
| | | |
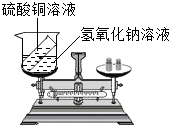 请你参与某学习小组的探究活动,并回答相关问题.
请你参与某学习小组的探究活动,并回答相关问题.| 实验方法及操作 | 可能观察到的现象 | 实验结论 |
| ______ | 有气泡产生 | ______ |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com