
题目列表(包括答案和解析)


| 序号 | 实验内容 | 实验现象 | 实验结论 |
| ① | 取少量样品于烧杯中,滴加稀盐酸 | 有大量气泡生成 | 本格不填 |
| ② | 用铂丝蘸取①中溶液,在酒精灯上灼烧 | 火焰为砖红色 | 溶液中含有钙离子 |
| ③ | 另取少量样品于烧杯中,加水充分溶解,滴加 碘水或碘酒 碘水或碘酒 |
无蓝色出现 | 样品中不含有淀粉 |
| ④ | 另取少量样品于烧杯中,加水溶解,静置、过滤,在滤液中加入适量浓硝酸,加热至沸 | 产生黄色固体 产生黄色固体 |
样品中含蛋白粉 (氨基酸) |
| 100 |
| x |
| 44 |
| 0.44g |
| 1g |
| 1.1g |
| 100 |
| x |
| 44 |
| 0.44g |
| 1g |
| 1.1g |
阅读下列材料,完成下列探究:
珍珠约含92%的CaCO3、4%的蛋白质(氨基酸)以及水等其他物质。以珍珠磨成的珍珠粉具有安神、美容等医用价值。央视《每周质量报告》曾揭露现今市场上存在大量以蚌壳粉冒充的珍珠粉(用氢氧化钠溶液去除蚌壳表面的有机物,用双氧水去除表面的黑色素等,然后磨成粉即可)。某研究性学习小组对本地的一种市售珍珠粉进行了以下探究。
探究一:该珍珠粉的主要成分
| 序号 | 实验内容 | 实验现象 | 实验结论 |
| ① | 取少量样品于烧杯中,滴加稀盐酸 | 有大量气泡生成 | 本格不填 |
| ② | 用铂丝蘸取①中溶液,在酒精灯上灼烧 | 火焰为砖红色 | 溶液中含有钙离子 |
| ③ | 另取少量样品于烧杯中,加水充分溶解,滴加 ▲ | 无蓝色出现 | 样品中不含有淀粉 |
| ④ | 另取少量样品于烧杯中,加水溶解,静置、过滤,在滤液中加入适量浓硝酸,加热至沸 | __ ▲ | 样品中含蛋白粉 (氨基酸) |
 (1)小名认为根据实验①、②可以推断样品中一定含有碳酸钙,小星不同意其观点。为了确认样品中含有碳酸钙,他需要补充完成的实验是(写出实验方法与现象): ▲ ;
(1)小名认为根据实验①、②可以推断样品中一定含有碳酸钙,小星不同意其观点。为了确认样品中含有碳酸钙,他需要补充完成的实验是(写出实验方法与现象): ▲ ;
(2)根据上述实验,可以判断该珍珠粉为 ▲ (填“真”或“假”)。
探究二:该珍珠粉中碳酸钙含量的测定
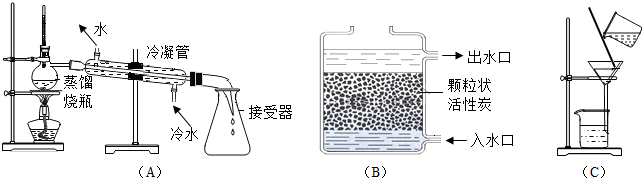
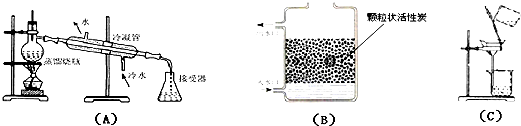
【方法1】小王用右图1所示装置测定该珍珠粉中碳酸钙的含量。实验方案如下:
(1)检查装置气密性:按图连接装好置后,将注射器活塞(不考虑活塞的摩擦和自重,下同)从刻度1mL处向上拉至刻度20mL处, ▲ (填操作和现象),则气密性良好。
(2)在锥形瓶内装入0.4g上述珍珠粉样品,注射器内吸入12mL的稀盐酸,再次连接装置。
(3)用力向锥形瓶内注入所有稀盐酸,并晃动锥形瓶。当没有气泡产生后,记录注射器刻度为92mL。
 (4)数据处理:该实验过程中产生CO2的体积为 ▲ mL,再根据CO2的密度(约2g/L)计算出其质量,计算出碳酸钙的质量,从而计算该珍珠粉中碳酸钙的含量。
(4)数据处理:该实验过程中产生CO2的体积为 ▲ mL,再根据CO2的密度(约2g/L)计算出其质量,计算出碳酸钙的质量,从而计算该珍珠粉中碳酸钙的含量。
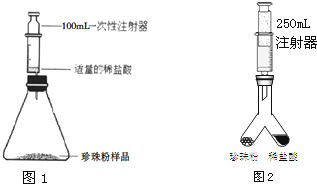
【方法2】同组的小明同学另外设计了一套装置,如右图2。实验方案如下:
(1)检查装置气密性;
(2)在右图Y形装置左管内装入1.1g上述珍珠粉样品,右管内倒入一定量的稀盐酸,针筒(规格为250mL)活塞推到底部,再次连接装置。
(3)设法使左右两管内的药品混合,反应结束后读取针筒读数为220mL。
(4)数据处理:请计算该珍珠粉中碳酸钙的质量分数。(写出计算过程,最终结果保留小数点后1位。4分)
▲
【实验反思】
(1)考虑针筒的因素,上述两个实验方案对珍珠粉的用量多少必须作要求吗?为什么?
▲ 。
(2)【方法2】中第(3)步如何实现两种药品的混合? ▲ 。
(3)小明设计的装置与小王比,有何优点? ▲ (写出1点即可)。
阅读下列材料,完成下列探究:
珍珠约含92%的CaCO3、4%的蛋白质(氨基酸)以及水等其他物质。以珍珠磨成的珍珠粉具有安神、美容等医用价值。央视《每周质量报告》曾揭露现今市场上存在大量以蚌壳粉冒充的珍珠粉(用氢氧化钠溶液去除蚌壳表面的有机物,用双氧水去除表面的黑色素等,然后磨成粉即可)。某研究性学习小组对本地的一种市售珍珠粉进行了以下探究。
探究一:该珍珠粉的主要成分
| 序号 | 实验内容 | 实验现象 | 实验结论 |
| ① | 取少量样品于烧杯中,滴加稀盐酸 | 有大量气泡生成 | 本格不填 |
| ② | 用铂丝蘸取①中溶液,在酒精灯上灼烧 | 火焰为砖红色 | 溶液中含有钙离子 |
| ③ | 另取少量样品于烧杯中,加水充分溶解,滴加 | 无蓝色出现 | 样品中不含有淀粉 |
| ④ | 另取少量样品于烧杯中,加水溶解,静置、过滤,在滤液中加入适量浓硝酸,加热至沸 | __ | 样品中含蛋白粉 (氨基酸) |


湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com