
题目列表(包括答案和解析)
 2Cu +CO2↑ 的反应外,还可能发生的化学反应方程式: 。
2Cu +CO2↑ 的反应外,还可能发生的化学反应方程式: 。(13分)某研究性学习小组设计并进行了如下实验。
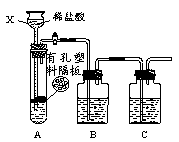
(1)甲组同学用下图装置制取干燥纯净的二氧化碳气体。
请回答下列问题:
①仪器X的名称是 ;有孔塑料隔板上的固体物质为 (填名称)。
②实验前,关闭活塞,向X中加入水使X中液面高于试管中的液面,一段时间后液面保持不变说明 。
③为除去CO2中混有的HCl气体,B装置中盛放饱和NaHCO3溶液,写出该反应的化学方程式: 。要得到干燥的CO2,C装置应盛放 (填“试剂名称”)。
④装置B、C中所装试剂的顺序不可以颠倒,理由是: 。
(2)乙组同学围绕C还原CuO产生的红色固体是否一定是Cu进行探究。
【查阅资料】 ①在空气中高温灼烧时,CuO会分解生成Cu2O;Cu2O粉末呈红色,在高温下性质稳定;②Cu2O在酸性溶液中不稳定,如在稀硫酸中:Cu2O+H2SO4=CuSO4+Cu+ H2O。
【提出猜想】猜想Ⅰ:红色固体是Cu; 猜想Ⅱ:红色固体是Cu2O;猜想Ⅲ:红色固体是 。
【实验探究】同学们又分为两组,分别进行以下实验:
①第一组同学取一定质量的红色固体a g ,在空气中高温灼烧,直到质量不再发生改变,称量所得固体质量为b g 。并进行数据分析:若a = b,则猜想 成立;若b>a,则说明红色固体中一定含有 物质。
②第二组同学没有用测量质量的方法也得出了红色固体中含有Cu2O的结论。该同学设计的实验方法是 。(写出“实验操作、现象和结论”)
【解释与结论】 根据实验探究,可知C还原CuO时除了发生2CuO+C 2Cu +CO2↑ 的反应外,还可能发生的化学反应方程式: 。
2Cu +CO2↑ 的反应外,还可能发生的化学反应方程式: 。
【拓展延伸】同学们又就Cu2O是否具有氧化性展开了讨论,请你设计实验方案: 。
【实验反思】通过以上实验探究,你对“问题的发现与解决”有何认识? 。
(13分)某研究性学习小组设计并进行了如下实验。
(1)甲组同学用下图装置制取干燥纯净的二氧化碳气体。

请回答下列问题:
①仪器X的名称是 ;有孔塑料隔板上的固体物质为 (填名称)。
②实验前,关闭活塞,向X中加入水使X中液面高于试管中的液面,一段时间后液面保持不变说明 。
③为除去CO2中混有的HCl气体,B装置中盛放饱和NaHCO3溶液,写出该反应的化学方程式: 。要得到干燥的CO2,C装置应盛放 (填“试剂名称”)。
④装置B、C中所装试剂的顺序不可以颠倒,理由是: 。
(2)乙组同学围绕C还原CuO产生的红色固体是否一定是Cu进行探究。
【查阅资料】 ①在空气中高温灼烧时,CuO会分解生成Cu2O;Cu2O粉末呈红色,在高温下性质稳定;②Cu2O在酸性溶液中不稳定,如在稀硫酸中:Cu2O+H2SO4=CuSO4+Cu+ H2O。
【提出猜想】猜想Ⅰ:红色固体是Cu; 猜想Ⅱ:红色固体是Cu2O;猜想Ⅲ:红色固体是 。
【实验探究】同学们又分为两组,分别进行以下实验:
①第一组同学取一定质量的红色固体a g ,在空气中高温灼烧,直到质量不再发生改变,称量所得固体质量为b g 。并进行数据分析:若a = b,则猜想 成立;若b>a,则说明红色固体中一定含有 物质。
②第二组同学没有用测量质量的方法也得出了红色固体中含有Cu2O的结论。该同学设计的实验方法是 。(写出“实验操作、现象和结论”)
【解释与结论】 根据实验探究,可知C还原CuO时除了发生2CuO+C 2Cu +CO2↑ 的反应外,还可能发生的化学反应方程式: 。
2Cu +CO2↑ 的反应外,还可能发生的化学反应方程式: 。
【拓展延伸】同学们又就Cu2O是否具有氧化性展开了讨论,请你设计实验方案: 。
【实验反思】通过以上实验探究,你对“问题的发现与解决”有何认识? 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com