
题目列表(包括答案和解析)
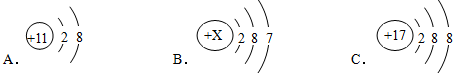
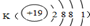 三种金属,
三种金属,在元素周期表的指导下,利用元素之间的一些规律性知识来分类学习物质的性质,就使化学学习和研究变得有规律可循。下图所示是元素周期表的一部分。
(1)地壳中含量最多的金属元素是 (写元素符号),其质子数为 。
(2)地壳中硅元素的含量仅次于氧元素,硅元素的相对原子质量为 。
(3)第三周期中具有相对稳定结构的原子的原子序数为 。
(4) 当11号元素与17号元素组成化合物时,构成此物质的阳离子的符号为 。
(5)下图所示的微粒中,属于同种元素的是 (填序号),元素的化学性质相似的是
(填序号),由A和D两种元素组成的物质的化学式为 。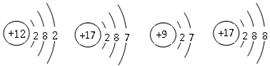
A B C D
在元素周期表的指导下,利用元素之间的一些规律性知识来分类学习物质的性质,就使化学学习和研究变得有规律可循。下图所示是元素周期表的一部分。
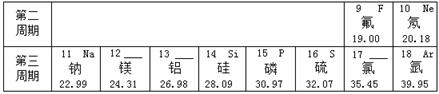
(1)地壳中含量最多的金属元素是 (写元素符号),其质子数为 。
(2)地壳中硅元素的含量仅次于氧元素,硅元素的相对原子质量为 。
(3)第三周期中具有相对稳定结构的原子的原子序数为 。
(4) 当11号元素与17号元素组成化合物时,构成此物质的阳离子的符号为 。
(5)下图所示的微粒中,属于同种元素的是 (填序号),元素的化学性质相似的是 (填序号),由A和D两种元素组成的物质的化学式为 。
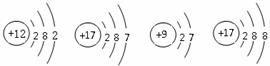
A B C D.
在元素周期表的指导下,利用元素之间的一些规律性知识来分类学习物质的性质,就使化学学习和研究变得有规律可循。下图所示是元素周期表的一部分。
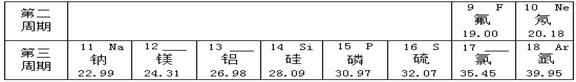
(1)地壳中含量最多的金属元素是 (写元素符号),其质子数为 。
(2)地壳中硅元素的含量仅次于氧元素,硅元素的相对原子质量为 。
(3)第三周期中具有相对稳定结构的原子的原子序数为 。
(4)当11号元素与17号元素组成化合物时,构成此物质的阳离子的符号为 。
(5)下图所示的微粒中,属于同种元素的是 (填序号),元素的化学性质相似的是 (填序号),由A和D两种元素组成的物质的化学式为 。
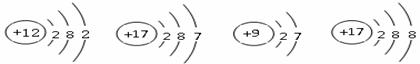
A B C D
在元素周期表的指导下,利用元素之间的一些规律性知识来分类学习物质的性质,就使化学学习和研究变得有规律可循。下图所示是元素周期表的一部分。
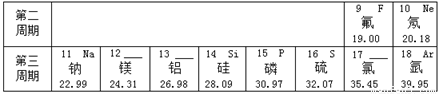
(1)地壳中含量最多的金属元素是 (写元素符号),其质子数为 。
(2)地壳中硅元素的含量仅次于氧元素,硅元素的相对原子质量为 。
(3)第三周期中具有相对稳定结构的原子的原子序数为 。
(4) 当11号元素与17号元素组成化合物时,构成此物质的阳离子的符号为 。
(5)下图所示的微粒中,属于同种元素的是 (填序号),元素的化学性质相似的是
(填序号),由A和D两种元素组成的物质的化学式为 。
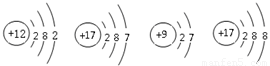
A B C D
一、选择题(本题20分)每题只有一个正确答案,将其标号填在下表中。每题2分。
题号
1
2
3
4
5
6
7
8
9
10
答案
D
D
B
C
C
A
B
C
B
D
二、选择题(本题共10分)每题有1~2个正确答案,将其标号填在下表中。每题2分。正确答案只有一个选项的,多选不给分;正确答案包括两个选项的只选一个且正确给1分,一对一错不给分。
题号
11
12
13
14
15
答案
D
BD
A
AC
BD
三、(本大题共5题 共15分)
16.(5分)每空1分。(1)A (2)D (3)C (4)B (5)E
17.(1分)每空1分。H2O
18.(4分)每空1分。D B ABEF BC
19.(3分)每空1分。(1)60 20 (2)90
20.(2分)每空1分。(1)

 21.(6分)每空1分。 (1)C+2CuO====2Cu+CO2↑ 置换
21.(6分)每空1分。 (1)C+2CuO====2Cu+CO2↑ 置换
(2)2H2O====2H2↑+O2↑ 1:2 (3)3Fe+2O2====Fe3O4 火星四射 放出大量的热 生成一种黑色固体
22.(1分)每空1分。酸
23.(4分)每种物质1分。(1)高锰酸钾 胆矾 (2)碳酸钙 (3)胆矾
24.(4分)每空1分。(1)CO2 NaOH溶液 (2)Zn+H2SO4(稀)====ZnSO4+H2↑
(3)锥形瓶内外存在气体压强差 其他合理答案可酌情给分
五、(本大题共2题 共15分)
25.(8分)每空1分。⑴ CaO+H2O====Ca(OH)2 CaCO3====CaO+CO2↑ Fe+CuSO4==FeSO4+Cu CuSO4+Ca(OH)2==Cu(OH)2↓+CaSO4
⑵① Ca(OH)2+Na2CO3==CaCO3↓+2NaOH ② MgCl2+2NaOH==Mg(OH)2↓+2NaCl
③ BaCO3+ H2SO4==BaSO4↓+H2O+CO2↑ ④ Zn+CuCl2 ==ZnCl2+Cu
26.(3分)每空1分。 HCl+AgNO3==AgCl↓+HNO3
H2SO4+Ba(NO3)2==BaSO4↓+2HNO3
2KOH + Cu(NO3)2==Cu(OH)2↓+2NaNO3
27.(3分)每空1分。⑴溶液由红色逐渐变为无色 ⑵挥发性 盐酸能跟碱发生中和反应
五、(本大题共2题 共12分)
28.(6分)每空1分。⑴CuSO4 ⑵BaCO3 BaSO4 ⑶Na2SO4 BaCl2 Na2CO3;Na2SO4 BaCl2 BaCO3;Na2SO4 BaCl2 Na2CO3 BaCO3;(每种可能性1分)
29.(6分)实验步骤和实验现象每空0.5分,化学方程式每个1分。
实验步骤
实验现象
化学方程式
稀盐酸
无色的气泡
Na2CO3+2HCl==2NaCl+H2O+CO2↑
BaCl2溶液
白色沉淀
Na2SO4+BaCl2==BaSO4↓+2NaCl
AgNO3溶液
白色沉淀
NaCl+AgNO3==AgCl↓+ NaNO3
六、(本大题共2题 共13分)
30.(6分)⑴题1分,其余每空1分。⑴丙戊甲已丁 ⑵ A ⑶ 甲中黑色物质变红乙中无水硫酸铜变蓝⑷ 甲中黑色物质变红丁中石灰水变浑浊⑸没有尾气的处理 在B导管处点燃
31.(7分)⑴每个物质1分,多答不给分 NaCl Na2SO4 ⑵每空一分,多答不给分Na2SO4 ;NaCl ;Ba(NO3)2, AgNO3;Na2SO4+Ba(NO3)2==BaSO4↓+2NaNO3
七、计算题(本大题共2题 共10分)
32.(4分)解:(1)设需用这种盐酸的质量为χ
χ=

(2)设可制得氢气的质量为У
Zn+2HCl==ZnCl2+H2↑
65 2
У=
答:可制得氢气
33.(6分)解:设25%的氢氧化钠溶液的质量为m
mg-
m=
设生成的硫酸钠溶液的质量为χ,生成的氢氧化铜沉淀的质量为У,硫酸铜溶液中溶质的质量为z
2NaOH + CuSO4== Na2SO4+ Cu(OH)2↓
80 160 142 98
80 160 142 98




χ=
У=
z=
硫酸铜溶液的质量为
硫酸铜溶液的溶质质量分数为

本资料由《七彩教育网》www.7caiedu.cn 提供!
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com