
4.沉淀溶解平衡是动态平衡,其影响因素主要有:
①温度:一般升温时,沉淀溶解度增大,能促进溶解,但要注意Ca(OH)2的溶解度随温度的升高而减小。
②同离子效应:增大体系中沉淀溶解平衡中离子浓度,平衡向生成沉淀的方向移动;反之,则向沉淀溶解的方向移动。
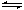
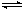 在沉淀后用(s)标明状态,并用“ ”,如:Ag2S(s)
2Ag+ (aq)+ S2-(aq)
在沉淀后用(s)标明状态,并用“ ”,如:Ag2S(s)
2Ag+ (aq)+ S2-(aq)
3.溶解平衡方程式的书写:
2.反应后离子浓度降至1×10-5mol/L以下的反应为完全反应,故用“=”,常见的难溶物在水中的离子浓度均远低于10-5mol/L
1.溶解度小于
3.掌握三个守恒关系:
(1)电荷守恒:电解质溶液中,不论存在多少种离子,溶液总是呈电中性,即阴离子所带负电荷总数一定等于阳离子所带正电荷总数。如在Na2CO3溶液中有c(Na+)+c(H+)=c(HCO3-)+
(2)物料守恒:电解质溶液中,由于某些离子水解或电离,使离子种类增多,但某些主要原子的总数是守恒的。如在Na2 CO3溶液中有c(Na+)=
(3)质子守恒:任何溶液中,最后溶液中仅由水电离出的H+与OH-守恒,即由水电离产生的c(H+)=c(OH-)。在电解质溶液中,由于某些离子发生水解,结合了水电离的H+或OH-,使溶液中c(H+)≠c(OH-),但由水电离出的H+与OH-守恒。如在Na2CO3溶液中有c(OH-)=c(H+)+c(HCO3-)+
八、溶沉淀解平衡及沉淀溶解平衡常数
要点一:沉淀溶解平衡:
2.混合溶液:混合溶液中离子浓度的比较,要注意能发生反应的先反应再比较,同时要注意混合后溶液体积的变化,一般情况下,混合溶液的体积等于各溶液体积之和。在此,常用到以下两组混合液:①NH
1.多元弱酸、多元弱酸盐溶液
如H2S溶液: c(H+)>c(HS-)>c(S2一)>c(OH一)。
如Na2CO3溶液:c(Na+)>c(CO32-)>c(OH-) >c(HCO3-)>(H+)。
8.明矾净水:Al3+水解成氢氧化铝胶体,胶体具有很大的表面积,吸附水中悬浮物而聚沉
注意:NH4HCO3、(NH4)2CO3溶液两种离子均可水解且互相促进,但不能水解进行到底,故它们可以大量共存,配成溶液。
七、溶液中离子浓度大小的比较
7.泡沫灭火器中药剂的使用,如Al2(SO4)3和NaHCO3
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com