
3.能正确表示下列反应的离子方程式是
A.Cl2通入NaOH溶液:Cl2+OH-=Cl-+ClO-+H2O
B.NaHCO3溶液中加入稀HCl:CO32-+2H+=CO2↑+H2O
C.AlCl3溶液中加入过量稀氨水:Al3++4NH3·H2O=AlO2-+4NH4++2H2O
D.Cu溶于稀HNO3:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
2.下列关于物质分类的说法正确的是
A.金刚石、白磷都属于单质
B.漂白粉、石英都属于纯净物
C.氯化铵、次氯酸都属于强电解质
D.葡萄糖、蛋白质都属于高分子化合物
一、选择题
1.化学与生活密切相关。下列说法不正确的是
A.乙烯可作水果的催熟剂
B.硅胶可作袋装食品的干燥剂
C.福尔马林可作食品的保鲜剂
D.氢氧化铝可作胃酸的中和剂
五、实验题
27、(10分)用酸式滴定管准确移取25.00mL某未知浓度的盐酸溶于一洁净的锥形瓶中,然后用0.20mol·L -1的氢氧化钠溶液(指示剂为酚酞).滴定结果如下:
|
|
NaOH起始读数 |
NaOH终点读数 |
|
第一次 |
0.10mL |
18.60mL |
|
第二次 |
0.30mL |
18.00m L L |
(1)根据以上数据可以计算出盐酸的物质的量浓度为 mol·L-1.
(2)达到滴定终点的标志是
(3)以下操作造成测定结果偏高的原因可能是 。
A. 配制标准溶液的氢氧化钠中混有Na2CO3杂质
 B. 滴定终点读数时,俯视滴定管的刻度,其它操作均正确
B. 滴定终点读数时,俯视滴定管的刻度,其它操作均正确
C. 盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
D. 未用标准液润洗碱式滴定管
(4) 滴定时边滴边摇动锥形瓶,眼睛应观察 。
A.滴定管内液面的变化B.锥形瓶内溶液颜色的变化
(5)下列各物质的溶液物质的量浓度均为0.1mol/L。
①HCl ②H2SO4 ③CH3COOH 按它们pH由小到大的排列顺序为


2013~2014学年第2学期第二学段考试
26.(8分)碳酸甲乙酯(CH3OCOOC2H5)是一种理想的锂电池有机电解液,生成碳酸甲乙酯的原理为:C2H5OCOOC2H5(g)+ CH3OCOOCH3(g) 2 CH3OCOOC2H5(g)
ΔH1
2 CH3OCOOC2H5(g)
ΔH1
(1)其他条件相同,CH3OCOOCH3的平衡转化率(α)与温度(T)、反应物配比(R)的关系如图所示。
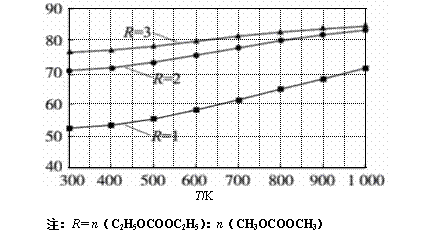

① ΔH1______0(填“<”、“=”或“>”)。
② 由图可知,为了提 高CH3OCOOCH3的平衡转化率,除了升温,另一措施是_______。
高CH3OCOOCH3的平衡转化率,除了升温,另一措施是_______。
③ 在密闭容器中,将1mol C2H5OCOOC2H5和1mol CH3OCOOCH3混合加热到650K,利用图中的数据,求此温度下该反应的平衡常数K。
四、计算题
25、(10分)在一固定容积的密闭容器中进行着如下反应:
CO2(g) + H2(g)  CO(g) + H2O(g)
其平衡常数K和温度t的关系如下:
CO(g) + H2O(g)
其平衡常数K和温度t的关系如下:
|
t℃ |
700 |
800 |
850 |
1000 |
1200 |
|
K |
2.6 |
1.7 |
1.0 |
0.9 |
0.6 |
(1)K的表达式为: ;
(2)该反应的正反应为 反应(“吸热”或“放热”);
(3)能判断该反应是否已经达到化学平衡状态的是:
A.容器中压强不变B.混合气体中CO浓度不变C.v(H2)正 = v(H2O)逆 D.c(CO2) = c(CO)
(4)在850℃时,可逆反应:CO2(g) + H2(g)  CO(g) + H2O(g),已知CO2和H2的起始浓度为1mol/L计算反应达到平衡时CO的平衡浓度为
;
CO(g) + H2O(g),已知CO2和H2的起始浓度为1mol/L计算反应达到平衡时CO的平衡浓度为
;
CO2 (g)的转化率为
24、CuCl2溶液,为防止出现浑浊,应加少量的_______
23、把三氯化铁溶液蒸干灼烧,最后得到的固体产物是 (1)
用方程式表示该过程:(2) ;(3)
22.(4分)CuCl2溶液有时呈黄色,有时呈黄绿色或蓝色,这是因为在CuCl2的水溶液中存在如下平衡:[Cu (H2O)4]2— (蓝色)+ 4Cl—  [CuCl4]2—
(黄色)+ 4H2O
[CuCl4]2—
(黄色)+ 4H2O
现欲使溶液由黄色变为黄绿色或蓝色,请写出两种可采用的方法:
方法一:
方法二:
三、填空题
21.(8分)在a、b两支试管中分别装上形态相同、质量相等的一颗锌粒,然后向两支试管中分别加入相同物质的量浓度、相同体积的稀盐酸和稀醋酸。填写下列空白:
(1)a、b两支试管中的现象相同点是 ,不同点是 。
(2)a、b两支试管中生成气体的体积开始时是a b(填“>”、“<”、“=”,下同),反应完毕后生成气体的总体积是a b
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com