
8. 共20分
共20分
(1)a、CH3CH2CH2COOH b、CH3CH2COOCH3
(2)羟基、醛基(或-OH和-CHO) CH3COCH2COOH
(3)a; b、c
(4)CH3CH(OH)CH2CHO→CH3CH=CHCHO+H2O
(5)nCH3CH=CHCH2OH→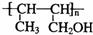 (6)
(6)
 (4分,其余均2分)
(4分,其余均2分)
10.(14分)煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程。
(1)将水蒸气通过红热的碳即可产生水煤 气。反应为:
气。反应为:
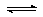 C(s)+H2O(g) CO(g)+H2(g) ΔH=+131.3 kJ•mol-1,ΔS=+133.7J•(K•mol) -1
C(s)+H2O(g) CO(g)+H2(g) ΔH=+131.3 kJ•mol-1,ΔS=+133.7J•(K•mol) -1
①该反应能否自发进行与 有关;
②一定温度下,在一个容积可变的密闭容器中,发生上述反应,下列能判断该反应达到化学平衡状态的是 (填字母)。
a.容器中的压强不变 b.1 mol H—H键断裂的同时断裂2 molH—O键
c.v正(CO) = v逆(H2O) d.c(CO)=c(H2)
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应
 CO(g)+H2O(g) CO2(g)+H2(g),得到如下三组数据:
CO(g)+H2O(g) CO2(g)+H2(g),得到如下三组数据:
|
实验组 |
温度/℃ |
起始量/mol |
平衡量/mol |
达到平衡所 需时间/min |
||
|
H2O |
CO |
H2 |
CO |
|||
|
1 |
650 |
2 |
4 |
1.6 |
2.4 |
5 |
|
2 |
900 |
1 |
3 |
0.75 |
2.25 |
3 |
|
3 |
900 |
2 |
4 |
x |
y |
t |
①实验1中以v(CO2) 表示的反应速率为 。
②该反应的逆反应为 (填“吸”或“放”)热反应
③该反应平衡常数的数学表达式为___________________________________
表中x = _____________; y = _____________
9. (14分)乙二酸(HOOC-COOH)俗称草酸,该酸广泛存在于多种植物的细胞膜内,其晶体通常含有结晶水(H2C2O4·2H2O),晶体的熔点为101.5℃,无水草酸的熔点为189.5℃。草酸易升华,其在157
(14分)乙二酸(HOOC-COOH)俗称草酸,该酸广泛存在于多种植物的细胞膜内,其晶体通常含有结晶水(H2C2O4·2H2O),晶体的熔点为101.5℃,无水草酸的熔点为189.5℃。草酸易升华,其在157 ℃时大量升华,并开始分解,
℃时大量升华,并开始分解, 分解产物为CO、CO2、H2O。w.某研究性学习小组的同学决定对草酸的分解反应进行探究,设计出如下实验验证乙二酸的分解并测定其分解率,操作步骤如下:
分解产物为CO、CO2、H2O。w.某研究性学习小组的同学决定对草酸的分解反应进行探究,设计出如下实验验证乙二酸的分解并测定其分解率,操作步骤如下: w.
w. w.w.zxxk.c.o.m
w.w.zxxk.c.o.m
①先把乙二酸晶体放在烘箱中进行烘烤,去掉结晶水,备用。
②按图2连接好装置。

③检查装置的气密性。
④打开活塞a,通入H2一会儿,再关闭a;点然酒精灯b、c。
⑤当C装置中固体消失后,停止加热
⑥打开活塞a,继续通入H2,直至冷却。
试回答下列问题:
⑴装置A的作用_______________________________________________,
B的作用________________________;装置E的作用________________________。
⑵检验该套装置的气密性的方法是______________________________________。
⑶若分解结束后,不再通入氢气,会使所测的乙二酸的分解率_________(填“增大”、“减小”或“不变”)。
⑷可以代替装置G的方法是___________________ _________________________。
_________________________。
⑸若称取H2C2O4(烘干)的质量为4.5g,实验结束后,称得D、E、F分别增重0.95g、0.40g、1.98g,则乙二酸的分解率为_______________。
8. (20分)己知 A 为有机合成中间体,在一定条件下发生消去反应,可能得到两种互为同分异构体的产物;其中的一种 B 可用 于制取合成树脂、染料等化工产品, A 可能发生如图所示的变化。
于制取合成树脂、染料等化工产品, A 可能发生如图所示的变化。

试回答:
( l )写出符合下述条件的 A 的同分异构体的结构简式(各任写一种):
a.具有酸性 ________________________________________________________;
________________________________________________________;
 b.能发生水解反应____________________________________________________。
b.能发生水解反应____________________________________________________。
( 2 ) A 分子中官能团的名称是________________,D 的结构简式_______________。
( 3 ) C→D的反应类型是___________,E→F的反应类型是___________
a.氧化反应 b.还原反应 c.加成反应 d.取代反应
( 4 )写出化学方程式: A→B________________________________。
( 5 )写出 E 在一定条件下生成高聚物的化学方程式:
_______________________________________________________。
(6)C的同分异构体Cl与C有相同官能团,两分子Cl脱去两分子水形成含有六元环的C2,写出C2可能具有的结构简式:
_________________________________________________________。
7.(16分) 短周期主族元素A、B、C、D、E、F 的原子序数依次增大,它们的原子核外电子层数之和为13。B的化合物种类繁多,数目庞大;C、D是空气中含量最多的两种元素,D、E两种元素的单质反应可以生成两种不同的离子化合物;F的最高化合价为+7。试回答以下问题:
 (1)写出A与D以 1:1的原子个数比形成的化合物的电子式:
。F的原子结构示意图为:
(1)写出A与D以 1:1的原子个数比形成的化合物的电子式:
。F的原子结构示意图为:
 。
。
 (2)化合物甲、乙由A、B、D、E中的三种或四种组成,且甲、乙的水溶液均呈碱性。则甲
(2)化合物甲、乙由A、B、D、E中的三种或四种组成,且甲、乙的水溶液均呈碱性。则甲 、乙反应的离子方程式为: _________________________________
。
、乙反应的离子方程式为: _________________________________
。
(3)常温下,若将0.2mol/LMOH溶液与0.1mol/LHCl溶液等体积混合,测得混合溶液的pH<7,则说明在相同条件下MOH的电离程度 MCl的水解程度。(填“>”、“<”、或“无法确定”)
 (4)常温下将0.2mol/L HCl溶液与0.2mol/L MOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=6,试回答以下问题:
(4)常温下将0.2mol/L HCl溶液与0.2mol/L MOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=6,试回答以下问题:
 ①混合溶液中由水电离出的c(H+) 0.2mol/LHCl溶液中由水电离出的c(H+);
①混合溶液中由水电离出的c(H+) 0.2mol/LHCl溶液中由水电离出的c(H+);
 (填“>”、“<”、或“=”)
(填“>”、“<”、或“=”)
 ②求出混合溶液中下列算式的精确计算结果(填具体数字):
②求出混合溶液中下列算式的精确计算结果(填具体数字):
 c(Cl-)-c(M+)= mol/L;
c(Cl-)-c(M+)= mol/L;

 (5)已知500m L 0.1 mol/L EDA 溶液与足量A F稀溶液反应,放出热量2.865 KJ ,试写出此反应的热化学方程式
(5)已知500m L 0.1 mol/L EDA 溶液与足量A F稀溶液反应,放出热量2.865 KJ ,试写出此反应的热化学方程式
———————————————————————————————————
6.下列对实验现象的解释与结论正确的是
|
编号 |
实验操作 |
实验现象 |
解释与结论 |
|
A |
向鸡蛋清溶液中加入饱和(NH4)2SO4溶液 |
有白色沉淀产生 |
蛋白质发生了变性 |
|
B |
向某溶液中加入BaCl2溶液 |
有白色沉淀产生 |
生成难溶于水的BaSO4,该溶液中一定含有SO42- |
|
C |
向苯中滴入少量浓溴水,振荡,静置 |
溶液分层,上层呈橙红色,下层几乎无色 |
苯和溴水发生取代反应,使溴水褪色 |
|
D |
向蔗糖中加入浓硫酸 |
蔗糖变黑,体积膨胀,放热并放出刺激性气味气体 |
浓硫酸具有脱水性和强氧化性,反应中生成C、SO2和CO2等 |
第Ⅱ卷
5.利用右图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生

 产。下列说法中正确的是--
产。下列说法中正确的是-- ---------------------( )
---------------------( )
A.氯碱工业中,X、Y均为石墨,Y附近能得到氢氧化钠
B.铜的精炼中,X是纯铜,Y是粗铜,Z是CuSO4
C.电镀工业中,X是待镀金属,Y是镀层金属
D.外加电流的阴极保护法中,X是待保护金属
4. 下列离子方程式书写正确的是-------------------------------( )
 A.碳酸氢钠的水解反应:HCO3- + OH-
CO32-+ H2O
A.碳酸氢钠的水解反应:HCO3- + OH-
CO32-+ H2O
|
C.Cl2通入热的KOH溶液中制取KClO3:3Cl2 + 6OH-=== ClO3- + 5Cl- + 3H2O
 D.苯酚钠溶液中通入少量CO2:CO2
+ H2O + 2C6H5O-
2C6H5OH
+ CO32-
D.苯酚钠溶液中通入少量CO2:CO2
+ H2O + 2C6H5O-
2C6H5OH
+ CO32-
3. 某二元酸H2A在水中发生电离: 下列叙述中不正确的是
-----------------------( )
下列叙述中不正确的是
-----------------------( )
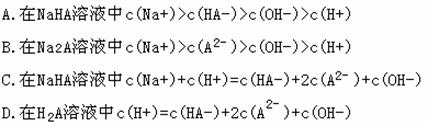
2. 设NA表示阿伏加德罗常数,下列说法中正确的是---------( )
 A. 0.01molMg在空气中完全燃烧生成MgO和Mg3N2,转移电子数目为0.02NA
A. 0.01molMg在空气中完全燃烧生成MgO和Mg3N2,转移电子数目为0.02NA
 B.常温常压下,18.00克重水(D2O)中所含电子数约为1
B.常温常压下,18.00克重水(D2O)中所含电子数约为1 0NA
0NA
 C.在熔融状态下1molNaHSO4所含阳离子数为2NA
C.在熔融状态下1molNaHSO4所含阳离子数为2NA
 D.1mol FeCl3完全水解转化为氢氧化铁胶体后能生成NA个胶粒
D.1mol FeCl3完全水解转化为氢氧化铁胶体后能生成NA个胶粒
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com