
9、只用下列鉴别方法不能把待鉴别的物质区分开的是
|
|
待鉴别的物质 |
鉴别方法 |
|
A |
澄清石灰水和氢氧化钠溶液 |
加盐酸,观察现象 |
|
B |
硬水和软水 |
加肥皂水,振荡,观察产生泡沫情况 |
|
C |
过氧化氢溶液和纯水 |
加硫酸铜溶液,观察有无气泡产生 |
|
D |
羊毛线和涤纶线 |
点燃,闻燃烧产生的气味 |
8.以下应用守恒思想解决相关问题,推论正确的是( )
A.14g碳与32g氧气反应,根据质量守恒推出生成的二氧化碳的质量为46g
B.乙炔燃烧生成二氧化碳和水,根据元素守恒推出乙炔由碳、氢、氧元素组成
C.铁丝燃烧后固体质量增加了,因此不遵循质量守恒定律
D.水电解生成H2和02的分子数比为2︰l,根据原子守恒推出水分子中H、O个数比为2︰1
7.类推是化学学习中常用的思维方法。现有以下类推结果,其中正确的是( )
A.有机物中都含有碳元素,所以含碳元素的化合物都是有机物
B.把燃着的木条插入某无色气体中,木条火焰熄灭,证明瓶中的气体一定是CO2
C.在某固体中滴加稀盐酸,有气泡产生,则该固体中一定含有活泼金属
D.水在通电条件下,可分解为氧气和氢气,说明在化学反应中分子是可分的
6. 稀土元素在现代科技发展中有着非常重要的作用,如图是稀土元素钇(Y)和镧(La)的相关信息。下列有关说法错误的是( )
稀土元素在现代科技发展中有着非常重要的作用,如图是稀土元素钇(Y)和镧(La)的相关信息。下列有关说法错误的是( )
A.钇原子的质子数是39 B.镧原子的核外电子数为57
C.钇的相对原子质量为88.91 D.镧原子的序数为138.9
5.2013年12月以来,安徽陷入“霾伏圈”,全省空气质量急剧下降,多个城市空气受到严重污染,因此省环保部门倡导保护环境尽一份责任。下列措施不正确的是( )
A.纸张“双面打印” B.国家应大力发展火力发电
C.提倡步行或骑自行车上、下班 D.在生产和生活中提倡使用节能技术和节能用具
4.LiFePO4新型锂离子动力电池以其独特的优势成为奥运会绿色能源的新宠,已知P的化合价为+5价,则LiFePO4中Fe的化合价为( )
A.+1 B.+2 C.+3 D.+4
2.下列各组物质中,富含蛋白质的是( )
A.鸡蛋、牛奶 B.米饭、土豆 C.香蕉、桃子 D.牛油、奶油
3薄荷醇(化学式为C10H20O)可用于糖果、饮料的加香,下列有关薄荷醇的说法正确的是( )
A.薄荷醇属于有机高分子化合物
B.薄荷醇由10个碳原子、20个氢原子和1个氧原子构成
C.薄荷醇中碳元素、氢元素和氧元素的质量比为10︰20︰1
D.薄荷醇中碳元素的质量分数约为76.9%
一. 我会选
1. 我省有着悠久的历史和丰富的文化内涵,下列变化主要是物理变化的( )

A.粮食酿洒 B.松枝烧墨 C.石刻砚台 D.竹子造纸
20.(9分)铁及其化合物在生活生产中有重要的应用。请回答下列问题:
(1)在盛有氧气的集气瓶中点燃细铁丝发生剧烈燃烧的化学方程式是 。
(2)把铁粉和铜 粉的混合物放入硝酸银溶液中,充分反应后,过滤,为确定滤渣和
粉的混合物放入硝酸银溶液中,充分反应后,过滤,为确定滤渣和 滤液
滤液 的成分,甲同学向滤渣中滴加稀盐酸,无气泡产生;
乙同学向滤
的成分,甲同学向滤渣中滴加稀盐酸,无气泡产生;
乙同学向滤 液中滴加稀盐酸,产生白色沉淀。根据两同学实验的现象,分析下列结论不正确的是 (填序号)。
液中滴加稀盐酸,产生白色沉淀。根据两同学实验的现象,分析下列结论不正确的是 (填序号)。
A.滤渣中只含银
B.滤渣中一定含 有银,可能含有铜
有银,可能含有铜
C.滤液中一定有Ag+ 、Fe2+ 和Cu2+ D.滤液中只含Ag+ 和Fe2+,不含Cu2+
[探究]废旧金属的回收利用。
废铁屑的主要成份是铁,同时还有少量铁锈(Fe2O3),生产动物饲料添加剂硫酸亚铁的工艺之一如下图所示:
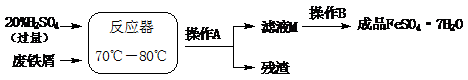
(3)在反应器中发生反应的化学方程式有:
Fe + H2SO4 =FeSO4 +H2↑、 、 Fe2(SO4)3 + Fe = 3FeSO4。
(4)滤液M中肯定含有的溶质的化学式是 ;
(5)在化学反应中,凡是有元素化合价变化的反应属于氧化还原反应。下列反应类型肯定属于氧化还原反应的是 (填字母编号);
A.化合反应 B.置换反应 C.分解反应 D.复分解反应
(6)(4分)取表面含有氧化镁的镁条(无其它杂质)2.5g,加入到足量的20.0g的稀硫酸中,充分反应后,所得溶液的质量为22.3g。求:①生成氢气的质量 ②该镁条中单质镁的质量分数(写出计算过程)。
19. (8分)对比学习有利于发现事物的共性与个性.为探究酸的性质,同学们进行了如下实验.
(8分)对比学习有利于发现事物的共性与个性.为探究酸的性质,同学们进行了如下实验.
|
实 验 内 容 |
 |
|
|
|
实 验 现 象 |
① (填字母编号) 瓶口的蓝色石蕊试纸很快变红. |
两试管中均产生 ② |
试管E:绿色粉末逐渐溶解,产生气泡,溶液显蓝色.
试管F:绿色粉末逐渐溶解,产生气泡,溶液显绿色. |
|
分 析 与 结 论 |
该酸有 ③
性,另一种酸没有。不同的酸可能有不同的物理性质 |
不同的酸具有相似的化学性质,这是因为酸溶液中都含 有 ④ (填符号). |
试管E中发生反应的化学方程式: Cu2(OH)2CO3+2H2SO4═ 2CuSO4+3H2O+CO2↑ 试管F中发生反应的化学方程式: ⑤ |
[发现问题]碱式碳酸铜与稀硫酸反应形成的CuSO4溶液显蓝色,而与盐酸反应形成的CuCl2溶液显绿色.
[提出问题]同样都含有Cu2+,为什么试管E中的CuSO4溶液显蓝 色,而试管F中的
色,而试管F中的
CuCl2溶液显绿色. [猜想与假设]
猜想一:若溶液中Cu2+显蓝色,则SO42- 对Cu2+显色无影响,而Cl-对Cu2+显色有影响; 猜想二:若溶液中Cu2+显绿色,则 ⑥ _;
猜想三:… [实验验证]同学们用下列两种不同方案初步验证猜想一,请你补全实验所需试剂:
方案一:取少量试管E中的CuSO4溶液于另一支试管中,向其中加入足量_ ⑦ ,
观察到产生白色沉淀,溶液仍为蓝色的现象,猜想一正确. 方案二:取少量试管F中的CuCl2溶液于另一支试管中,向其中加入足量_ ⑧ _,
观察到产生白色沉淀,溶液由绿色变为蓝色的现象,猜想一正确.
[评价与反思]同学们在实验探究的过程中,体会到了 溶液颜色成因复杂,相关知识还有待进一步学习.
溶液颜色成因复杂,相关知识还有待进一步学习.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com