
5.(2013·江苏化学·1)燃料电池能有效提高能源利用率,具有广泛的应用前景。下列物质均可用作燃料电池的燃料,其中最环保的是
A.甲醇  B.天然气 C.液化石油气 D.氢气
B.天然气 C.液化石油气 D.氢气
11、解析:SO2具有漂白性,常用于漂白纸浆和草帽辫,A合理;硫酸与锅炉中水垢的主要成分碳酸钙反应生成的微 溶硫酸钙会覆辙在碳酸钙表面阻碍反应的继续进行,所以应选用盐酸除垢而非硫酸,B不合理;焦炭在高温下与SiO2反应生成硅和一氧化碳,C合理;Cu2+、Hg2+与S2—反应生成难溶的CuS、HgS沉淀,D正确。答案:B
溶硫酸钙会覆辙在碳酸钙表面阻碍反应的继续进行,所以应选用盐酸除垢而非硫酸,B不合理;焦炭在高温下与SiO2反应生成硅和一氧化碳,C合理;Cu2+、Hg2+与S2—反应生成难溶的CuS、HgS沉淀,D正确。答案:B
命题意图:元素化合物
4.(2013·广东理综·11)下列措施不合理的是
A.用SO2漂白纸浆和草帽辫 B.用硫酸清洗锅 炉中的水垢
炉中的水垢
C.高温下用焦炭还原SiO2制取粗硅D.用Na2S作沉淀剂,除去废水中Cu2+和Hg2+
3.(2013·新课标卷I·7)化学无处不在,下列与化学有关的说法不正确的是
A.侯氏制碱法的工艺过程中应用了物质溶解度的差异
B.可用蘸浓盐酸的棉棒检验输送氨气的管道是否漏气
C.碘是人体必需微量元素,所以要多吃富含高碘酸的食物
D.黑火药由硫黄、硝石、木炭三种物质按一定比例混合制成
[考点]化学与生活、科技等,关注STS知识,该题与人们日常生活紧密结合,均为最基本的化学常识,为容易题。
[解析]侯氏制碱法是将CO2、NH3通入饱和NaCl溶 液中,由于NaHCO3溶解度小于Na2CO3,故NaHCO3在溶液中析出,A项正确;浓盐酸易挥发,与NH3结合生成NH4Cl固体小颗粒,为白烟状态,B项正确;碘是人体必需元素,补碘常在食盐中加入KIO3固体而不是高碘酸,高碘酸为强酸性物质,C项错误;制备黑火药的原料为S、KNO3、C,三者比例为1:2:3,D项正确。
液中,由于NaHCO3溶解度小于Na2CO3,故NaHCO3在溶液中析出,A项正确;浓盐酸易挥发,与NH3结合生成NH4Cl固体小颗粒,为白烟状态,B项正确;碘是人体必需元素,补碘常在食盐中加入KIO3固体而不是高碘酸,高碘酸为强酸性物质,C项错误;制备黑火药的原料为S、KNO3、C,三者比例为1:2:3,D项正确。
[答案]C
2.(2013·山东理综·7)化学与生活密切相关,下列说法正确的是
A.聚乙烯塑料的老化是由于发生了加成反应
B.煤经过气化和液化等物理变化可以转化为清洁燃料
C.合成纤维、人造纤维及碳纤维都属于有机高分子材料
D.利用粮食酿酒经过了淀粉→葡萄糖→乙醇的化学变化过程
解析:聚乙烯塑料的老化是因为被氧化所致,A选项错;煤的气化是化学变化,B错;碳纤维是碳的单质,C错;用粮食酿酒时,先在糖化酶作用下水解为葡萄糖,然后在酵母作用下转变为酒精,都是化学变化。D正确。
答案:D
1、(2013·天津化学·2)以下食品化学知识的叙述不正确的是
A、食盐可作调味剂,液可作食品防腐剂
B、新鲜蔬菜做熟后,所含维生素C会有损失
C、纤维素在人体内可水解为葡萄糖,故可做人类的营养物质
D、葡萄糖中的花青素在碱性环境下显蓝色,故可用苏打粉检验假红酒。
[解析]该 题考查和生活相关的一些物质的主要性质。命题依据来源于选修1,《化学
题考查和生活相关的一些物质的主要性质。命题依据来源于选修1,《化学 与生活》
与生活》
A选项正确,考查食盐的常识性知识。B选项考查维生素C的性质,维生素C在水溶液中或受热时很容易被氧化,生吃新鲜蔬菜比熟吃时损失小,正确。C选项,纤维素在人体内不能水解,所以 不能作为人类的营养物质,错误。D选项苏打是碳酸钠,呈碱性,假红酒中没有葡萄糖时与苏打不显蓝色。正确。
不能作为人类的营养物质,错误。D选项苏打是碳酸钠,呈碱性,假红酒中没有葡萄糖时与苏打不显蓝色。正确。
答案:C
0.17 mol·L-1
(4)③④
23.(2011上海23)工业上制取冰晶石(Na3AlF6)的化学方程式如下:
2Al(OH)3+ 12HF+ 3Na2CO3=2Na3AlF6+ 3CO2↑+ 9H2O
根据题意完成下列填空:
(1)在上述反应的反应物和生成物中,属于非极性分子的电子式 ,
属于弱酸的电离方程式 。
(2)反应物中有两种元素在元素周期表中位置相邻,下列能判断它们的金属性或非金属性强弱的是
(选填编号)。
a.气态氢化物的稳定性 b.最高价氧化物对应水化物的酸性
c.单质与氢气反应的难易 d.单质与同浓度酸发生反应的快慢
(3)反应物中某些元素处于同一周期。它们最高价氧化物对应的水化物之间发生反应的离子方程式为 。
(4) Na2CO3俗称纯碱,属于 晶体。工业上制取纯碱的原料是 。
解析:本题考察电子式和方程式的书写、元素周期律的应用和具体类型的判断。CO2属于非极性分子,HF和H2O属于极性分子;其中氟和氧位置相邻,且位于同一周期;钠和铝、C和O及F处于同一周期。
答案: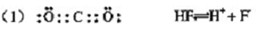
(2)ac
(3)Al(OH)3+OH-=AlO2-+H2O
(4)离子晶体 氯化钠、二氧化碳和氨
22.(2011四川,15分)
甲、乙、丙、丁、戊为原子序数依次增大的短周期元素。甲、丙处于同一主族,丙、丁、戊处于同一周期,戊原子的最外层电子数是甲、乙、丙原子最外层电子数之和。甲、乙组成的成的常见气体X能使湿润的红色石蕊试纸变蓝;戊的单质与X反应能生成乙的单质,同时生成两种溶于水均呈酸性的化合物Y和Z,0.1mol/L的Y溶液pH>1;丁的单质既能与丙元素最高价氧化物的水化物的溶液反应生成盐L也能与Z的水溶液反应生成盐;丙、戊可组成化合物M。
请回答下列问题
(1) 戊离子的结构示意图为_______。
(2) 与出乙的单质的电子式:_______。
(3) 戊的单质与X反应生成的Y和Z的物质的量之比为2:4,反应中被氧化的物质与被还原的物质的物质的量之比为________。
(4) 写出少量Z的稀溶液滴入过量L的稀溶液中发生反应的离子方程式:_________。
(5) 按下图电解M的饱和溶液,写出该电解池中发生反应的总反应方程式:_______。将充分电解后所得溶液逐滴加入到酚酞试液中,观察到得现象是__________。
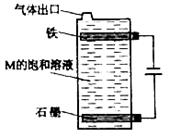
解析:本题主要考察元素周期表的结构、元素周期律及电解的应用。由题意知甲、乙、丙、丁、戊分别为H、N、Na、Al、Cl。
答案:(1)Cl-:
(2)
(3)2:3
(4)H++AlO2-+H2O=Al(OH)3↓
(5)NaCl+H2O NaClO+H2↑ 先变红后褪色
NaClO+H2↑ 先变红后褪色
21.(2011海南,20分)
19-I(6分)下列分子中,属于非极性的是
A.SO2 B.BeCl2 C.BBr3 D.COCl2
[答案]BC
命题立意:考查价层电子对互斥理论(VSEPR)对分子结构分析或识记
解析:根据价层电子对互斥理论(VSEPR)可得四种分子的结构如下:

[思维拓展]进入新课标高考以来,关于价层电子对互斥理论的运用成了重要的常考点,每年都会考到,是高考复习必备知识与能力点。
19-II(14分)铜是重要金属,Cu的化合物在科学研究和工业生产中具有许多用途,如CuSO4溶液常用作电解液、电镀液等。请回答以下问题:
(1)CuSO4可由金属铜与浓硫酸反应制备,该反应的化学方程式为___________;
(2)CuSO4粉末常用来检验一些有机物中的微量水分,其原因是_______;
(3)SO42-的立体构型是________,其中S原子的杂化轨道类型是_______;
(4)元素金(Au)处于周期表中的第六周期,与Cu同族,Au原子最外层电子排布式为______;一种铜合金晶体具有立方最密堆积的结构,在晶胞中Cu原子处于面心,Au原子处于顶点位置,则该合金中Cu原子与Au原子数量之比为_______;该晶体中,原子之间的作用力是________;
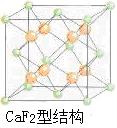
(5)上述晶体具有储氢功能,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中。若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构为CaF2的结构相似,该晶体储氢后的化学式应为__________。
[答案](1)Cu+2 H2SO4(浓)  CuSO4 + SO2↑+ 2H2O;
CuSO4 + SO2↑+ 2H2O;
(2)白色无水硫酸铜可与水结合生成蓝色的CuSO4·5 H2O,显示水合铜离子特征蓝色;
(3)正四面体,sp3;(4)6s1;(5)3:1;(4)金属键;(5)H8AuCu3
命题立意:物质结构与性质的综合考查。包含有铜元素相关的性质考查、硫酸根空间结构考查、杂化轨道考查、原子结构考查、晶体结构及计算考查。
解析:本题各小题内容考查点相互的联系不大,仍属于“拼盘”式题。(3)硫酸根中心原子的价层电子对为:孤对电子数6-2×4+2=0,成键电子对数4,所以为正四面体结构,中心原子为sp3杂化;(4)Au电子排布或类比Cu,只是电子层多两层,由于是面心立方,晶胞内N(Cu)=6×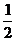 =3,N(Au)=8×
=3,N(Au)=8×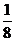 =1;(5)CaF2结构如下图所示,所以氢原子在晶胞内有4个,可得储氢后的化学式为H8AuCu3
=1;(5)CaF2结构如下图所示,所以氢原子在晶胞内有4个,可得储氢后的化学式为H8AuCu3
[思维拓展]由于《物质结构与性质》模块近年才在在高考中出现,不可能出很难的题,且结构与性质之间的关系的紧密联系也不能体现过深,因而目前的高考来看,试题只能是拼盘式的。学习过程中有一定的难度,但学会后变化较少。主要的几个考点除配位外,基本在本题中都考到,与近三年的考题变化不大。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com