
2.下列关于0.1 mol/L氨水的叙述正确的是( )
A.加入少量氯化钠溶液,平衡不移动
B.加入少量NaOH固体,平衡正向移动
C.通入少量氯化氢气体,平衡正向移动
D.加入少量MgSO4固体,抑制NH3·H2O电离
解析:选C 加氯化钠溶液相当于加水稀释,促进NH3·H2O电离,A错误;氢氧化钠抑制氨水电离,B错误;氯化氢溶于水生成盐酸,盐酸与氨水电离出的OH-反应,促进氨水的电离平衡正向移动,C正确;镁离子结合OH-,促进氨水电离,D错误。
一、选择题
1.关于强、弱电解质的叙述错误的是( )
A.强电解质在溶液中完全电离,一定不存在电离平衡
B.在溶液里,导电能力强的电解质是强电解质,导电能力弱的电解质是弱电解质
C.同一弱电解质的溶液,当温度、浓度不同时,其导电能力也不同
D.纯净的强电解质在液态时有的导电,有的不导电
解析:选B 在水溶液中能完全电离的电解质是强电解质,但强电解质溶液的导电能力不一定强,导电能力取决于溶液中离子浓度的大小和离子所带电荷的多少;由于弱电解质的电离是一个吸热过程,故温度升高,则电离程度增大,导电能力增强;对于离子化合物的强电解质(如氯化钠、硫酸钾)液态时是可导电的,但对于共价化合物的强电解质(如硫酸、氯化氢)来讲,在其液态时(无水)是不导电的。
11.某有机物的结构确定:
(1)测定实验式:某含C、H、O三种元素的有机物,经燃烧分析实验测定其碳的质量分数是64.86%,氢的质量分数是13.51%, 则其实验式是________。
(2)确定分子式:如图是该有机物的质谱图,则其相对分子质量为________,分子式为________。
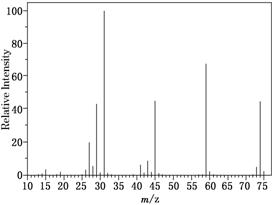
解析:(1)该物质中碳的质量分数是64.86%,氢的质量分数是13.51%,则氧的质量分数为1-64.86%-13.51% =21.63%,所以C、H、O三种原子的个数比为4∶10∶1,即实验式为C4H10O,分子式为(C4H10O)n
(2)由质谱图可知其相对分子质量为74,则74n=74,n=1,所以分子式为C4H10O。
答案:(1)C4H10O (2)74 C4H10O
10.(1)写出同时满足下列条件的C4H6O4的所有同分异构体的结构简式(不考虑立体异构)________________________________________________________________________
________________________________________________________________________。
a.属于酯类 b.能发生银镜反应
(2)① 的同分异构体有多种,写出其中一种不含甲基的羧酸的结构简式:
的同分异构体有多种,写出其中一种不含甲基的羧酸的结构简式:
________________________________________________________________________。
②化合物丁仅含碳、氢、氧三种元素,相对分子质量为110。丁与FeCl3溶液作用显现特征颜色,且丁分子中烃基上的一氯取代物只有一种。则丁的结构简式为________________________________________________________________________。
(3)X是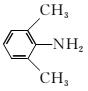 的同分异构体,X分子中含有苯环,且苯环上一氯代物只有两种,则X所有可能的结构简式有
的同分异构体,X分子中含有苯环,且苯环上一氯代物只有两种,则X所有可能的结构简式有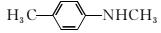 、____________、____________、____________。
、____________、____________、____________。
解析:(1)符合条件的C4H6O2的同分异构体应满足:①分子式为C4H6O2;②分子中含有酯基(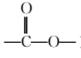 )和醛基(—CHO),有以下4种:HCOOCH===CHCH3、
)和醛基(—CHO),有以下4种:HCOOCH===CHCH3、
HCOOCH2CH===CH2、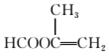
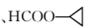 。
。
(2)① ,分析该有机物结构,一个
,分析该有机物结构,一个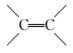 ,一个酯基,如果同分异构体不含甲基,并且为羧酸,那么若有碳碳双键,则
,一个酯基,如果同分异构体不含甲基,并且为羧酸,那么若有碳碳双键,则 与
与 必须在两头,为CH2===CHCH2CH2COOH,若无碳碳双键,则烃基中应有环状结构,
必须在两头,为CH2===CHCH2CH2COOH,若无碳碳双键,则烃基中应有环状结构, 或
或
②丁与FeCl3溶液作用显现特征颜色,为酚,烃基上一氯取代物只有一种,则苯环对位上有两个相同取代基,再结合相对分子质量为110,可以推知丁为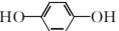 。
。
(3)苯环上一氯代物只有两种,则排除苯环上1个取代基,又不能多于3个。若有两个取代基,必须在对位,

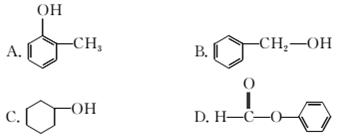
9.今有化合物

(1)请写出甲中含氧官能团的名称:________________________________________________________________________。
(2)请判别上述哪些化合物互为同分异构体:________________________________________________________________________。
(3)与丙同属于一类物质的有________________。
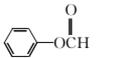
(4)化合物E是乙的同分异构体,且化合物E具有以下特点:①属于芳香族化合物,②能发生银镜反应,③能发生水解反应,则化合物E的结构简式为____________________。
解析:(1)甲中含醛基和(酚)羟基两种含氧官能团。(2)甲、乙两种物质分子式相同,结构不同,互为同分异构体。(3)丙属于酚类,酚类要求羟基与苯环直接相连。(4)化合物E中应含有苯环、醛基和酯基。
答案:(1)醛基和(酚)羟基 (2)甲和乙 (3)A
(4) 
8.有A、B两种烃,其相关信息如表所示:
|
A |
①完全燃烧的产物中n(CO2)∶n(H2O)=2∶1 |
|
②28<M(A)<60 |
|
|
③不能使溴的四氯化碳溶液褪色 |
|
|
④一氯代物只有一种结构 |
|
|
B |
①饱和链烃,通常情况下呈气态 |
|
②有同分异构体 |
|
|
③二溴代物有三种 |
回答下列问题:
(1)烃A的最简式是________________。
(2)烃A的结构简式是________________。
(3)烃B的三种二溴代物的结构简式为________________________________________________________________________
______________________________________________________________________。
(4)烃C为烃B的同系物,常温下为气态且只有一种一溴代物,则烃C的一溴代物的结构简式为________________________________________________________________________
(填一种即可)。
解析:(1)烃A完全燃烧的产物中n(CO2)∶n(H2O)=2∶1,则烃A的分子式为(CH)n。(2)因28<M(A)<60,所以烃A的分子式为C3H3或C4H4,结合另外两个信息可知烃A的结构简式是
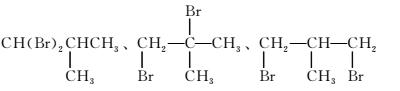
 。(3)烃B为饱和链烃,通常情况下呈气态,则烃B为CH4或C2H6或C3H8或C4H10;有同分异构体,则不可能为CH4、C2H6、C3H8,所以烃B为C4H10。它的三种二溴代物的结构简式分别为CH(Br)2CHCH3CH3、CH2BrCCH3BrCH3、CH2BrCHCH3CH2Br。(4)烃B的同系物中常温下为气态的是CH4、C2H6、C3H8,C3H8有两种一溴代物,CH4、C2H6都只有一种一溴代物,分别为CH3Br、C2H5Br。
。(3)烃B为饱和链烃,通常情况下呈气态,则烃B为CH4或C2H6或C3H8或C4H10;有同分异构体,则不可能为CH4、C2H6、C3H8,所以烃B为C4H10。它的三种二溴代物的结构简式分别为CH(Br)2CHCH3CH3、CH2BrCCH3BrCH3、CH2BrCHCH3CH2Br。(4)烃B的同系物中常温下为气态的是CH4、C2H6、C3H8,C3H8有两种一溴代物,CH4、C2H6都只有一种一溴代物,分别为CH3Br、C2H5Br。
答案:(1)CH (2)
(3) 
(4)CH3Br(或C2H5Br)
7.乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物。

回答下列问题:
(1)正四面体烷碳碳键键角为________,其二氯取代产物有________种。
(2)关于乙烯基乙炔分子的说法错误的是________(填字母符号)。
A.能使酸性KMnO4溶液褪色
B.1 mol乙烯基乙炔最多能与3 mol Br2发生加成反应
C.乙烯基乙炔分子内含有两种官能团
D.等质量的乙炔与乙烯基乙炔完全燃烧时的耗氧量不相同
E.乙烯基乙炔分子中的所有原子一定都共平面
(3)环辛四烯的分子式为__________________,写出与环辛四烯互为同分异构体且属于芳香烃的分子的结构简式:__________________________。
(4)下列属于苯的同系物的是________(填字母符号)。
A.CHCH2 B.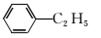
C.
 D.
D.
(5)请分别写出乙炔、CH3CHO、CH3COOH、CH3COOC2H5所含官能团的名称__________、__________、__________、__________。
解析:(1)根据碳的四价原则,推知分子中每个碳原子只结合一个氢原子。由于其为正四面体结构,所以二氯取代物只有1种,碳碳键键角为60°。(2)因为乙烯基乙炔分子中含有一个碳碳双键和一个碳碳三键,所以A、B、C正确,乙烯基乙炔与乙炔最简式相同,相同质量的乙烯基乙炔与乙炔完全燃烧耗氧量相同,D错误,乙烯基乙炔可以看成是乙烯与乙炔拼接而成,所有原子一定在同一个平面,E正确。(3)由于环辛四烯的不饱和度为5,所以其属于芳香烃的同分异构体含有一个双键便可达到要求。(4)根据同系物的概念,苯的同系物只能有一个苯环,且与苯相差一个或若干个CH2原子团。
答案:(1)60° 1 (2)D (3)C8H8 
(4)B、D (5)碳碳三键 醛基 羧基 酯基
6.有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取。纯净的A为无色粘稠液体,易溶于水。为研究A的组成与结构,进行实验如表所示:
|
实验步骤 |
解释或实验结论 |
|
(1)称取A 9.0 g,升温使其汽化,测其密度是相同条件下H2的45倍 |
(1)A的相对分子质量为________ |
|
(2)将此9.0 g A在足量纯O2中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重5.4 g和13.2 g |
(2)A的分子式为______________ |
|
(3)另取A 9.0 g,跟足量的NaHCO3粉末反应,生成2.24 L CO2(标准状况),若与足量金属钠反应则生成2.24 L H2(标准状况) |
(3)用结构简式表示A中含有的官能团:_________、_________________ |
(4)A的核磁共振氢谱如图: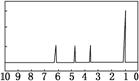 |
(4)A中含有________种氢原子 |
|
(5)综上所述,A的结构简式为______________________ |
解析:(1)A的密度是相同条件下H2密度的45倍,则A的相对分子质量为45×2=90,9.0 g A的物质的量为0.1 mol。(2)燃烧产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重5.4 g和13.2 g,说明0.1
mol A燃烧生成0.3 mol H2O和0.3
mol CO2,则1 mol A中含有6
mol H、3 mol C。(3)0.1 mol A跟足量的NaHCO3粉末反应,生成2.24 L(标准状况)CO2,若与足量金属钠反应则生成2.24 L(标准状况下)H2,说明分子中含有一个—COOH和一个—OH。(4)A的核磁共振氢谱中有4个峰,说明分子中含有4种处于不同化学环境的氢原子。(5)综上所述,A的结构简式为 。
。
答案:(1)90 (2)C3H6O3 (3)—COOH —OH (4)4
(5) 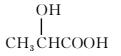
5.某化合物6.4 g在氧气中完全燃烧,只生成8.8 g CO2和7.2 g H2O。说法正确的是( )
A.该化合物仅含碳、氢两种元素
B.该化合物中碳、氢原子个数比为1∶4
C.无法确定该化合物是否含有氧元素
D.该化合物一定是C2H8O2
解析:选B 8.8 g CO2的物质的量是0.2 mol,含C的物质的量为0.2 mol,质量为2.4 g;同理可算出在7.2 g H2O中含H的物质的量为0.8 mol,质量为0.8 g;因C、H两元素质量之和小于6.4 g,所以一定含有氧元素,但D项不符合碳原子的成键原则。
4.3甲基戊烷的一氯代产物有(不考虑立体异构)( )
A.3种 B.4种 C.5种 D.6种
解析:选B 先写出3甲基戊烷的结构简式,观察其有几种氢原子,便有几种一氯代物。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com