
2.下列分子式表示的一定是纯净物的是 ( )
A.C5H10 B.C7H8O C.CH4O D.C2H4Cl2
一、选择题
1.下列表示物质结构的化学用语或模型正确的是( )
A.羟基的电子式: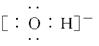
 B.CH4分子的球棍模型:
B.CH4分子的球棍模型:
C.乙烯的最简式(实验式):CH2 D.苯乙醛结构 简式:
简式: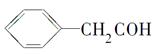
29.(8分)同学们在实验室用混合两种固体药品的办法自制“钾,氮复合肥料”,使用到的药品有KCl,K2SO4,NH4HCO3,NH4Cl。同学们制得了成分不同的“钾,氮复合肥料”,从中抽取一份作为样品探究其成分,请回答有关问题:
限选试剂:稀HCl,稀H2SO4,BaCl2溶液,AgNO3溶液,蒸馏水
(1) 提出合理假设。所抽样品的成分有4总共可能:
假设1:KCl和 NH4HCO3 ; 假设2:KCl和NH4Cl;
假设3:K2SO4和 NH4HCO3 ; 假设4: 。
(2) 形成设计思路。
①甲同学先提出先用AgNO3溶液确定是否含有KCl,你是否同意并说出理由: 。
②乙同学提出先确定是否含有NH4HCO3,则可以选择的试剂是 。
(3) 完成实验方案。请填写实验操作,与表中结论相符的预期现象。
|
实验操作 |
预期现象 |
结论 |
|
步骤1:
|
|
假设2成立 |
|
步骤2:
|
|
28.(8分)粗盐中除NaCl外还含有MgSO4以及泥沙等杂质。初步提纯粗盐的实验流程如下:
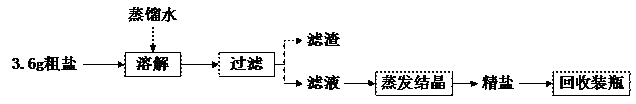
(1)“滤渣”是粗盐中含有的 。
(2)实验过程中四次用到玻璃棒,分别是:
第一次:溶解时搅拌;
第二次: ;
 第三次: ;
第三次: ;
第四次:将精盐从蒸发皿转移出来。
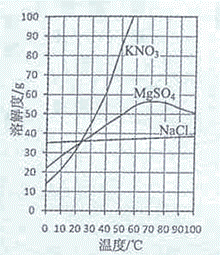
(3)本实验从滤液得到精盐,采用的是蒸发溶剂的方法而不用降低溶液温度的方法,参考溶解度曲线图分析的原因:
(4)看图可知,200C时NaCl的溶解度为 g,本实验溶解3.6g的粗盐,蒸馏水的最佳使用量约为 ml.增加蒸馏水的用量虽然能加快粗盐的溶解,但会引起的不良后果是 。
27.(10分)实验室部分装置如图所示,请回答下列问题。

(1)仪器X的名称是 。
(2)实验室用CaCO3和稀盐酸制备CO2的化学方程式为 ,若需制备22g CO2,不计实验损耗,至少需要消耗 g CaCO3。
(3)①用大理石和稀盐酸制取CO2时,能作为发生装置的是 、 (填字母,下同)。
②若要制备多瓶CO2,并在制取过程中便于补充稀盐酸,发生装置应选择 ,收集装置应选择 。
(4)实验室通过加热亚硝酸钠和氯化铵的混合溶液制取并收集N2时,应选择 与
组合而成的装置。
三、本题包括4小题,共28分。
26.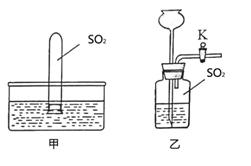 (2分)甲、乙两个装置均可用于证明SO2易溶于水。
(2分)甲、乙两个装置均可用于证明SO2易溶于水。
(1)甲装置中,在水面下松开橡皮塞,一段时间后可观察到的现象是 。
(2)收集一瓶SO2,按乙装置组装仪器,打开活塞K,向长颈漏斗加水至如图位置,关闭活塞K,一段时间后可观察到的现象是 。
25.(7分)使用密度小、强度大的镁合金能减轻汽车自重,从而减少汽油消耗和废气排放。
|
(2)工业制镁的一种原理是2MgO+Si+2CaO ====== 2Mg↑+Ca2SiO4,抽走容器中的空气对反应有促进作用,且能防止空气中的物质与Mg反应使产品混有 (填化学式)。
(3)制镁的原料MgO可从海水中获得。小华利用镁与盐酸反应后的废液,模拟从海水中获取MgO的过程,实验如下:
步骤1:向上述废液中,边搅拌边分批加入CaO,至MgCl2完全沉淀为止,过滤得Mg(OH)2固体。共消耗8.4g CaO。
步骤2:将Mg(OH)2固体加热分解为MgO和水,所得MgO的质量为4.0g 。
①步骤2中Mg(OH)2分解的化学方程式为 。
②通过所得MgO的质量计算上述废液中含MgCl2的质量m= g。
③ 分析实验数据,可知步骤Ⅰ中反生的化学反应有:
CaO+H2O==Ca(OH)2 ;Ca(OH)2+MgCl2==CaCl2+Mg(OH)2↓; 。
24.(10分)组成相似的盐具有一些相似的化学性质。
(1)①Cu(NO3)2溶液和CuSO4溶液都含有大量 (填离子符号)。
②向Cu(NO3)2溶液中加入NaOH溶液,充分振荡。反应的化学方程式为 。
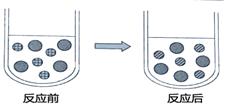
③向CuSO4溶液中加入过量的锌片,充分反应后,可看到的现象是 ,右图表示该反应前后溶液中存在的主要离子,请写出每种图形代表的离子(填离子符号)

(2)除上述实验外,在溶液中与Cu(NO3)2和CuSO4均能反应的物质还有 、
(任举二例,填化学式,下同)
(3)在溶液中能与CuSO4反应而不与Cu(NO3)2反应的物质有 (任举一例)。
23.(6分)已知镉(Cd)的金属活动性与铁、锌相近,镉元素在化合物中常显+2价。
(1)细铁丝在氧气中点燃发生剧烈燃烧,化学方程式是______________________________。
(2)将镉丝插入下列溶液有明显现象的是__________(填序号)。
①NaCl溶液 ②HCl溶液 ③AgNO3溶液 ④NaOH溶液
(3)镍镉电池应用广泛,为了防止污染环境,将废旧镍镉电池中回收镉的一种方法如下:
步骤1:将废旧电池破碎成细颗粒后培烧,将镉转化为氧化镉(CdO);
步骤2:将含氧化镉的细颗粒和炭粉混合后,隔绝空气加热至1200℃,可得镉蒸气和
一氧化碳。
步骤2中氧化镉变成镉的化学方程式是____________________________________。
22.(4分)合理运用燃烧与灭火的化学原理对保障生命财产安全非常重要。
(1)2013年12月广州建业大厦发生严重火灾。从燃烧条件分析,大厦内存放的大量鞋、纸箱等物品充当了________________。
(2)高层建筑物通常设计了灭火用的洒水系统。从灭火原理分析,洒水的作用主要是___________________________________。
 (3)分析下表中的数据,回答问题:
(3)分析下表中的数据,回答问题:
|
物质代号 |
L |
M |
N |
P |
|
熔点/℃ |
-117 |
3550 |
44 |
-259 |
|
沸点/℃ |
78 |
4827 |
257 |
-253 |
|
着火点/℃ |
510 |
370 |
40 |
580 |
① 有人认为“物质的熔、沸点越高,着火点越高”,该结论___________________(填“合理”或“不合理”)。
② 已知酒精灯火焰的温度约为500℃。利用上图装置,验证达到可燃物着火点是燃烧的条件之一,上表中可用于完成该实验的两种可燃物是_________和________(填代号)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com