
3. (2013·湛江二模)下列陈述Ⅰ、Ⅱ正确并且有因果关系的是( )
|
选项 |
陈述Ⅰ |
陈述Ⅱ |
|
A |
H2O2、SO2都能使酸性高锰酸钾褪色 |
前者表现出还原性,后者表现出漂白性 |
|
B |
纯银器表面在空气中渐渐变暗 |
发生了化学腐蚀 |
|
C |
SiO2能与氢氟酸及碱反应 |
SiO2是两性氧化物 |
|
D |
BaSO4饱和溶液中加入饱和Na2CO3溶液有白色沉淀 |
Ksp(BaSO4)<Ksp(BaCO3) |
2. 下列有关实验操作、现象和解释或结论都正确的是( )
|
选项 |
实验操作 |
现象 |
解释或结论 |
|
A |
过量的Fe粉中加入稀硝酸,充分反应后,滴入KSCN溶液 |
溶液呈红色 |
稀硝酸将Fe氧化为Fe3+ |
|
B |
AgI沉淀中滴入稀KCl溶液 |
有白色沉淀出现 |
AgCl比AgI更难溶 |
|
C |
Al箔插入稀硝酸中 |
无现象 |
Al箔表面被HNO3氧化,形成致密的氧化膜 |
|
D |
用玻璃棒蘸取浓氨水点到红色石蕊试纸上 |
试纸变蓝色 |
浓氨水呈碱性 |
一、 单项选择题
1. 下列说法不正确的是( )
A. 易燃试剂与强氧化性试剂分开放置并远离火源
B. 用湿润的红色石蕊试纸检验氨气
C. 在50 mL量筒中配制0.100 0 mol·L-1碳酸钠溶液
D. 金属钠着火时,用细沙覆盖灭火
18. (2013·惠州调研)设nA为阿伏加德罗常数的值,下列叙述正确的是( )
A. 25℃时,1.0LpH=13的Ba(OH)2溶液中含有的OH-数目为0.2nA
B. 标准状况下,2.24LCl2与过量稀NaOH溶液反应,转移的电子总数为0.2nA
C. 室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5nA
D. 标准状况下,22.4L甲醇中含有的氧原子数为nA
卷Ⅱ(化学实验基础,共52分)
17. (2013·韶关一模)设nA为阿伏加德罗常数的值,下列说法正确的是( )
A. 常温常压下,22.4LNH3中含有3nA个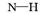 键
键
B. 1mol·L-1CaCl2溶液含有nA个Ca2+
C. 48gO3和O2的混合气体中含有3nA个O原子
D. 1molNO2溶于水后溶液中含有nA个N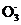
16. (2013·扬州二模)设nA为阿伏加德罗常数的值,下列叙述错误的是( )
A. 常温常压下,0.17gNH3中含有的共用电子对数为0.1nA
B. 常温常压下,1LpH=1的稀硫酸中含有的氢离子数为0.1nA
C. 10g由CaCO3与KHCO3组成的混合物中含有的碳原子数为0.1nA
D. 标准状况下,2.24LCl2与足量稀NaOH反应,转移的电子数为0.1nA
15. (2013·清远模拟)设nA为阿伏加德罗常数的值,下列叙述正确的是( )
A. 标准状况下,2.24LH2O中分子数为0.1nA
B. 1L0.5mol·L-1AlCl3溶液中含有的Al3+数为0.5 nA
C. 常温常压下,16gO2中氧原子数为nA
D. 0.1mol铁粉与足量的盐酸充分反应,转移的电子数为0.3nA
14. (2013·广州番禺模拟)设nA为阿伏加德罗常数的值,下列叙述正确的是( )
A. 常温常压下,11.2L氧气所含的原子数为nA
B. 1.8g的N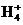 中含有的电子数为0.1nA
中含有的电子数为0.1nA
C. 常温常压下,48gO3和O2的混合气体含有的氧原子数为3nA
D. 2.4g金属镁变为镁离子时失去的电子数为0.1nA
13. (2012·海南高考改编)设nA为阿伏加德罗常数的值,下列说法正确的是( )
A. 在密闭容器中加入1.5molH2和0.5molN2,充分反应后可得到NH3的分子数为nA
B. 标准状况下,0.1molCl2溶于水,转移的电子数目为0.1nA
C. 1.0L0.1mol·L-1Na2S溶液中H2S、HS-、S2-的总数为0.1nA
D. 标准状况下,22.4L的CCl4中含有分子数为nA
12. 设nA为阿伏加德罗常数的值,下列叙述正确的是( )
A. 7.8gNa2O2中含有0.4nA个离子
B. 0.5mol雄黄(As4S4,结构如右图)含有nA个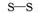 键
键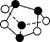
C. 用惰性电极电解CuSO4溶液时,当阳极产生2.24L气体(标准状况),转移0.2nA个电子
D. 一定条件下,某密闭容器充入0.2molSO2和0.1molO2,充分反应后分子数可能是0.22nA
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com