
三、 非选择题
9. (2013·东莞第七高级中学月考)氧化还原反应在生产、生活中具有广泛的用途,贯穿古今。
(1) 下列生产、生活中的事例中没有发生氧化还原反应的是 (填字母)。
A. 煤的形成 B. 原电池工作 C. 简单机械织布 D. 我国古代烧制陶器
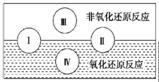
(2) 水是人体的重要组成部分,是人体中含量最多的一种物质。“四种基本反应类型与氧化还原反应的关系”可用右图表示。
试写出有水参加的符合反应类型Ⅳ的一个化学方程式: ,其中水为 剂。
(3)
氯化铵常用于焊接。如在焊接铜器时用氯化铵除去铜器表面的氧化铜以便焊接,其反应的化学方程式为 CuO+ NH4Cl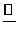 Cu+ CuCl2+ N2↑+ H2O。
Cu+ CuCl2+ N2↑+ H2O。
①配平此氧化还原反应的化学方程式。
②该反应中,被氧化的元素是 (填元素名称),氧化剂是 (填化学式)。
③反应中若产生0.2mol的气体,则有 mol的电子转移。
8. (2013·六校第一次联考)已知:①向KClO3晶体中滴加浓盐酸,产生黄绿色气体;②向NaI溶液中通入少量实验①产生的气体,溶液变黄色;③取实验②生成的溶液滴在淀粉-KI试纸上,试纸变蓝色。下列判断正确的是( )
A. 实验①证明Cl-具有还原性
B. 实验②中氧化剂与还原剂的物质的量之比为2∶1
C. 实验③说明KI被氧化
D. 上述实验证明氧化性:Cl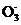 >Cl2>I2
>Cl2>I2
二、 双项选择题
7.
(2013·松昌中学月考)三氟化氮(NF3)是微电子工业中优良的等离子刻蚀气体,它在潮湿的环境中能发生反应:3NF3+5H2O 2NO+HNO3+9HF。下列有关该反应的说法正确的是( )
2NO+HNO3+9HF。下列有关该反应的说法正确的是( )
A. NF3在潮湿的空气中泄漏会产生红棕色气体
B. NF3是氧化剂,H2O是还原剂
C. 氧化剂与还原剂的物质的量之比为2∶1
D. 若生成0.2molHNO3,则转移0.2mol电子
6. (2013·肇庆中学月考)实验室制氯气时,多余氯气用氢氧化钠溶液吸收,下列关于该反应的说法正确的是( )
A. Cl2仅作氧化剂
B. NaClO是还原产物
C. 每生成1molNaCl,有1molCl2被氧化
D. 每转移1mol电子,有0.5molCl2被还原
5. (2013·深圳中学第二次月考)已知NH4CuSO3与足量的2mol·L-1稀硫酸溶液混合微热,产生下列现象:①有红色金属生成;②产生刺激性气味的气体;③溶液呈现蓝色。据此判断下列说法正确的是( )
A. 反应中硫酸作氧化剂
B. NH4CuSO3中硫元素被氧化
C. 1molNH4CuSO3完全反应转移0.5mol电子
D. 刺激性气味的气体是氨气
4. 下列反应中,氧化剂与还原剂物质的量的关系为1∶2的是( )
A.
2F2+2H2O 4HF+O2
4HF+O2
B.
2CH3COOH+Ca(ClO)2 Ca(CH3COO)2+2HClO
Ca(CH3COO)2+2HClO
C.
I2+2NaClO3 2NaIO3+Cl2
2NaIO3+Cl2
D.
4HCl+MnO2 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
3.
(2013·广东六校联考)据悉,2012伦敦奥运会上使用的发令枪所用的“火药”成分是氯酸钾和红磷,经撞击发出响声,同时产生白色烟雾。撞击时发生反应的化学方程式为5KClO3+6P 3P2O5+5KCl,则下列有关叙述错误的是( )
3P2O5+5KCl,则下列有关叙述错误的是( )
A. 上述反应中氧化剂和还原剂的物质的量之比为5∶6
B. 产生白色烟雾的原因是生成的P2O5白色固体小颗粒(烟)吸水性很强,吸收空气中的水分,生成磷酸小液滴(雾)
C. 上述反应中消耗3molP时,转移电子的物质的量为15mol
D. 因红磷和白磷互为同素异形体,所以上述火药中的红磷可以用白磷代替
2. (2013·佛山一中第二次段考)下列化工生产过程所发生的反应不属于氧化还原反应的是( )
A. 用油脂制肥皂
B. 用铝土矿制金属铝
C. 用氯气和消石灰制漂白粉
D. 用氢气和氮气合成氨
一、 单项选择题
1.
(2013·广东六校联考)实验室利用以下反应制取少量氮气:NaNO2+NH4Cl NaCl+N2↑+2H2O,下列关于该反应的说法正确的是( )
NaCl+N2↑+2H2O,下列关于该反应的说法正确的是( )
A. NaNO2是氧化剂
B. 每生成1molN2转移电子的物质的量为6mol
C. NH4Cl中的氮元素被还原
D. N2既是氧化剂,又是还原剂
8.
(1) ①K=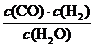 ②BC
②BC
(2) Z 催化效率高且活性温度低(或催化活性高,速率快,反应温度低,产率高)
(3) >
(4) 提高原料利用率(或提高产量、产率)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com