
6. (1) ①0.003mol·L-1·min-1 ②< 2.25×10-4
(2) ③< BD ④a. 见下表 b. 见下图
|
实验编号 |
T/℃ |
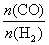 |
p/Mpa |
|
i |
150 |
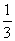 |
0.1 |
|
ii |
150 |
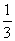 |
5 |
|
iii |
350 |
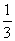 |
5 |
0.2 0.3 0.3
K=c[(NH2)2CO]·c(H2O)=0.3×0.3=0.09
0.3 0.3 0.3
平衡浓度/mol·L-1
0.5 0 0
转化浓度/mol·L-1
5. (1) ABC
(2) ①> =
②由图知,平衡时NH2COONH4的转化率为60%。
NH2COONH4(l)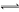 (NH2)2CO(g)+H2O(g)
(NH2)2CO(g)+H2O(g)
初始浓度/mol·L-1
4. (1) K=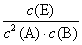 变大 >
变大 >
(2) ①0.05mol·L-1·min-1
②10.7
③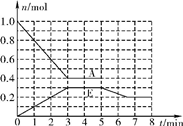
(3) ④⑥
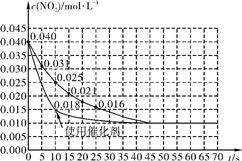
3. (1) 1.1×10-3mol·L-1·s-1
(2) ①减小 ②正向
(3) 、(4)见下图
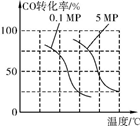
2. (1) 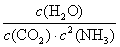 100
100
(2) AB
1. (1) 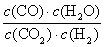 (2) 吸热 (3) bc (4) 830
(2) 吸热 (3) bc (4) 830
8. (2013·茂名华侨中学期初)固定和利用CO2能有效地利用资源,并减少空气中的温室气体。工业上有一种用CO2来生产甲醇燃料的方法:
CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH=-49.0kJ·mol-1
CH3OH(g)+H2O(g) ΔH=-49.0kJ·mol-1
某科学实验将6molCO2和8molH2充入2L的密闭容器中,测得H2的物质的量随时间变化如下图所示(实线)。
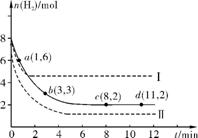
(1) a点正反应速率 (填“大于”、“等于”或“小于”)逆反应速率。
(2) 下列时间段平均反应速率最大的是 ,最小的是 。(填字母)
A. 01min B. 13min C. 38min D. 811min
(3)求平衡时氢气的转化率和该条件下反应的平衡常数K。(写出计算过程)
(4)仅改变某一实验条件再进行两次实验,测得H2的物质的量随时间变化如图中虚线所示,曲线Ⅰ对应的实验条件改变是 ,曲线Ⅱ对应的实验条件改变是 。
专题六 化学反应速率 化学平衡
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com