
9. (1)放热 (2) 0.16 mol·L-1·min-1 (3) 20%
(4)使用了催化剂;增大了压强(任答一种即可)
8. BC
7. BD
6. D
5. B
4. C
3. C
2. B
1. D
12. 二甲醚(CH3OCH3)被称为21世纪的清洁、高效能源。
(1)合成二甲醚反应一:3H2(g)+3CO(g) CH3OCH3(g)+CO2(g) ΔH=-247
kJ·mol-1
CH3OCH3(g)+CO2(g) ΔH=-247
kJ·mol-1
①一定条件下该反应在密闭容器中达到平衡后,要提高CO的转化率,可以采取的措施是 (填字母)。
A. 低温高压 B. 加催化剂 C. 体积不变充入N2
D. 增加CO浓度 E. 分离出二甲醚
②合成气的制备方法有:CH4(g)+H2O(g) CO(g)+3H2(g) ΔH1=+206.1
kJ·mol-1。
CO(g)+3H2(g) ΔH1=+206.1
kJ·mol-1。
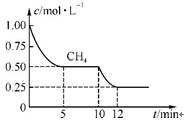
在密闭容器中进行反应,测得CH4的物质的量浓度随反应时间的变化如右图所示。反应进行的前5 min内,v(H2)= ;10 min时,改变的外界条件可能是 (任填一种即可)。
(2)合成二甲醚反应二:2CH3OH(g) CH3OCH3(g)+H2O(g)。在不同温度下,分别在1
L密闭容器中加入不同物质的量的CH3OH,反应达到平衡,测得各组分的浓度如下:
CH3OCH3(g)+H2O(g)。在不同温度下,分别在1
L密闭容器中加入不同物质的量的CH3OH,反应达到平衡,测得各组分的浓度如下:
|
实验组 |
温度/K |
平衡浓度/mol·L-1 |
||
|
|
|
CH3OH |
CH3OCH3 |
H2O |
|
1 |
403 |
0.01 |
0.2 |
0.2 |
|
2 |
453 |
0.02 |
0.3 |
0.4 |
通过平衡常数的计算说明该反应是放热反应还是吸热反应。
第三篇 化学反应原理
专题六 化学反应速率 化学平衡
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com