
11. (1)过二硫酸铵法是目前最流行的制备H2 的方法,即电解含
H2SO4、(NH4)2SO4的溶液制取(NH4)2S2O8(如右图所示),再加热水解即可得H2O2和(NH4)2SO4。
的方法,即电解含
H2SO4、(NH4)2SO4的溶液制取(NH4)2S2O8(如右图所示),再加热水解即可得H2O2和(NH4)2SO4。

①电解时,阳极的电极反应式为 。
②写出生成H2O2的化学方程式: 。
(2) 工业上在碱性条件下电解水,氧气在特制的阴极上反应可以得到H ,从而制得H2O2。将H2O2溶液与消石灰反应,经过滤、洗涤、干燥,可得过氧化钙晶体。
,从而制得H2O2。将H2O2溶液与消石灰反应,经过滤、洗涤、干燥,可得过氧化钙晶体。
①写出电解过程中氧气参与的阴极的电极反应式: 。
②H2O2与Ca(OH)2反应时,若不加稳定剂,需控制温度在05℃,原因是 。
(3) 酸性条件下,SnSO4可用作双氧水去除剂,试写出发生反应的离子方程式: 。
(4) 工业上用铂作阳极、铜或银作阴极电解盐酸也可制得高氯酸,在阳极区可得到20%的高氯酸。写出阳极的电极反应式: 。
10. (2013·苏锡常镇徐连一调改编)利用硫酸渣(主要含Fe2O3、SiO2、Al2O3、MgO等杂质)制备氧化铁的工艺流程如下:
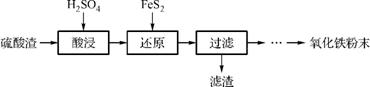
(1) “酸浸”中硫酸要适当过量,目的是:①提高铁的浸出率,② 。
(2) “还原”是将Fe3+转化为Fe2+,同时FeS2被氧化为S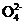 ,该反应的离子方程式为
。
,该反应的离子方程式为
。
(3) 可选用 (填化学式)检验滤液中含有Fe3+。产生Fe3+的原因是 (用离子方程式表示)。
二、非选择题
9. (2013·徐州模拟改编)某兴趣小组模拟氯碱工业生产原理并探究其产品的性质。已知文献记载:
①氯气与冷的氢氧化钠溶液反应生成NaClO,氯气与热的氢氧化钠溶液反应可生成NaClO和NaClO3;
②在酸性较弱时KI只能被NaClO氧化,在酸性较强时亦能被NaClO3氧化。
(1) 该小组利用如右图所示装置制取家用消毒液(主要成分为NaClO),则a为 (填“阳极”或“阴极”)。生成NaClO的离子方程式为 。

(2) 该小组将0.784 L(标准状况)Cl2通入50.00 mL热的NaOH溶液中,两者恰好完全反应后,稀释到250.0 mL。
①取稀释后的溶液25.00 mL用醋酸酸化,加入过量KI溶液。用0.2000
mol·L-1 Na2S2O3溶液滴定:I2+2S2
 2I-+S4
2I-+S4 ,消耗Na2S2O3溶液10.00
mL时恰好到达终点。
,消耗Na2S2O3溶液10.00
mL时恰好到达终点。
②将上述滴定后的溶液用盐酸酸化至强酸性,再用上述Na2S2O3溶液滴定到终点,消耗Na2S2O3溶液30.00 mL。
操作②中氯酸钠与碘化钾反应的离子方程式为 。
8.
(2013·扬州中学模拟)如下图所示,其中甲池的总反应式为2CH3OH+3O2+4KOH 2K2CO3+6H2O,下列说法正确的是( )
2K2CO3+6H2O,下列说法正确的是( )
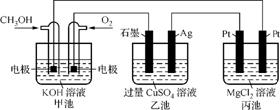
A. 甲池是电能转化为化学能的装置,乙、丙池是化学能转化电能的装置
B. 甲池通入CH3OH的电极反应式为CH3OH-6e-+2H2O C
C +8H+
+8H+
C. 反应一段时间后,向乙池中加入一定量的Cu(OH)2固体能使CuSO4溶液恢复到原浓度
D. 甲池中消耗280 mL(标准状况)O2,此时丙池中理论上最多产生1.45g固体
7. 向四支试管中分别加入少量不同的无色溶液进行以下操作,其中结论正确的是( )
|
选项 |
操作 |
现象 |
结论 |
|
A |
滴加BaCl2溶液 |
生成白色沉淀 |
原溶液中有Ag+ |
|
B |
滴加氯水和CCl4,振荡、静置 |
下层溶液显紫色 |
原溶液中有I- |
|
C |
用洁净铂丝蘸取溶液进行焰色反应 |
火焰呈黄色 |
原溶液中有Na+,无K+ |
|
D |
滴加稀NaOH溶液,将湿润的红色石蕊试纸置于试管口 |
试纸不变蓝 |
原溶液中无N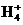 |
6. (2013·淮安模拟)下列表示对应化学反应的离子方程式正确的是( )
A. MgSO4溶液中加入Ba(OH)2溶液:Ba2++S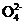
 BaSO4↓
BaSO4↓
B. 小苏打溶液中加入足量的Ca(OH)2溶液:HC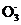 +Ca2++OH-
+Ca2++OH- CaCO3↓+H2O
CaCO3↓+H2O
C. 用稀硝酸洗涤试管内壁银镜:Ag+2H++N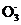
 Ag++NO↑+H2O
Ag++NO↑+H2O
D. 醋酸与水垢中的CaCO3反应:CaCO3+2H+ Ca2++H2O+CO2↑
Ca2++H2O+CO2↑
5. (2013·南通模拟)下列表示对应化学反应的离子方程式正确的是( )
A. 钠和水反应:Na+2H2O Na++2OH-+H2↑
Na++2OH-+H2↑
B. AlCl3溶液中滴加足量氨水:Al3++4OH- Al
Al +2H2O
+2H2O
C. 将SO2通入氯水中:SO2+Cl2+2H2O S
S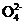 +2Cl-+4H+
+2Cl-+4H+
D. 向Ca(ClO)2溶液中通入过量CO2:2ClO-+CO2+H2O 2HClO+C
2HClO+C
4. 下列有关实验操作、现象和解释或结论都正确的是( )
A. 用洁净的铂丝蘸取某溶液进行焰色反应,火焰呈黄色,则原溶液中一定不含K+
B. 向某溶液中滴加盐酸,若无沉淀生成,
再滴加BaCl2溶液若有白色沉淀生成, 则原溶液中一定含有S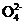
C. 向某溶液中滴加NaOH溶液并加热,将湿润的红色石蕊试纸置于试管口,试纸变蓝,则原溶液中一定含有N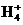
D. 为检验卤代烃中含有的卤元素,可向卤代烃中加入NaOH溶液并加热,充分反应后,再加入AgNO3,观察沉淀的颜色
3. 下列各组离子一定能大量共存的是( )
A. 强碱溶液中:Na+、K+、Al 、C
、C
B. 含大量Fe3+的溶液中:N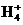 、Na+、Cl-、SCN-
、Na+、Cl-、SCN-
C. c(H+)=10-13mol·L-1的溶液中:N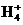 、Al3+、S
、Al3+、S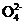 、N
、N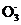
D. pH=1的溶液中:K+、Fe2+、Cl-、N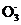
2. 在水溶液中能大量共存的一组离子是( )
A. Ba2+、Na+、S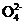 、Cl-
、Cl-
B. Mn 、S
、S 、H+、K+
、H+、K+
C. Al 、Mg2+、K+、HC
、Mg2+、K+、HC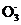
D. K+、Na+、N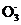 、S
、S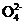
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com