
4.(20分)(2012·汕头期末)邻羟基桂皮酸是合成香精的重要原料,下图为合成邻羟基桂皮酸的路线之一:
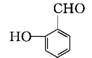

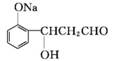

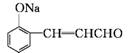
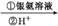
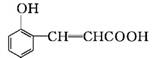
Ⅰ Ⅱ Ⅲ Ⅳ
试回答下列问题:
(1)化合物Ⅱ→化合物Ⅲ的有机反应类型为 。
(2)化合物Ⅲ在银氨溶液中发生反应的化学方程式为 。
(3)有机物X为化合物Ⅳ的同分异构体,且知有机物X有如下特点:
A.是苯的对位取代物 B.能与NaHCO3反应放出气体 C.能发生银镜反应
请写出化合物X的结构简式: 。
(4)下列说法正确的是 (填序号)。
A.化合物Ⅰ遇氯化铁溶液呈紫色 B.化合物Ⅱ能与NaHCO3溶液反应
C.1mol化合物Ⅳ完全燃烧消耗9.5molO2 D.1mol化合物Ⅲ最多能与3molH2反应
(5)有机物R(C9H9ClO3)经过反应也可制得化合物Ⅳ,则R在NaOH醇溶液中反应的化学方程式为 。
3.(20分)(2012·广东九校联考)化合物Ⅴ是中药黄芩中的主要活性成分之一,具有抗氧化和抗肿瘤作用。化合物Ⅴ也可通过下图所示方法合成:
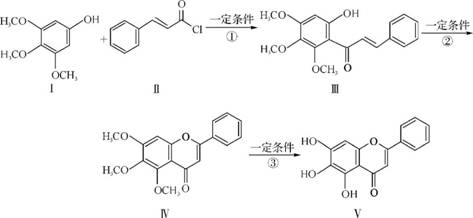
(1)化合物Ⅰ的分子式为 ,化合物Ⅴ中含有的含氧官能团的名称为 (任写两种)。
(2)化合物Ⅱ的合成方法如下:
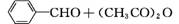

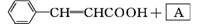
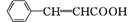
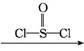 化合物Ⅱ
化合物Ⅱ
肉桂酸
合成肉桂酸的反应式中,反应物的物质的量之比为1∶1,生成物A呈酸性,则其名称是 。一定条件下,肉桂酸与乙醇反应生成香料肉桂酸乙酯,其反应的化学方程式为 (不要求写出反应条件)。
(3)反应①属于 (填反应类型)。化合物Ⅰ和Ⅱ反应还可以得到一种酯,该酯的结构简式是 。
(4)下列关于化合物Ⅴ的说法正确的是 (填序号)。
A.分子中有三个苯环 B.能发生水解反应
C.使酸性KMnO4溶液褪色 D.与FeCl3发生显色反应
2.(20分)(2012·广东六校第二次联考)冠心平F是降血脂、降胆固醇的药物,它的一条合成路线如下:
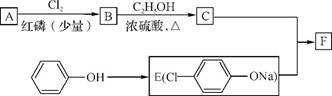
已知:RCH2COOH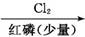
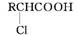
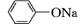 +RCl
+RCl
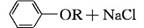 (R表示烃基或H原子)
(R表示烃基或H原子)
(1)A为羧酸,其分子式为C4H8O2,8.8gA与足量NaHCO3溶液反应生成 LCO2(标准状况,不考虑CO2溶于水)。
(2)写出符合A分子式且属于羧酸类物质的结构简式: 。
(3)已知A→B属于取代反应,B为一卤代羧酸,其核磁共振氢谱只有两个峰,写出B→C的化学方程式: 。
(4)写出F的结构简式: 。
(5)按如下路线,由C可合成酯类高聚物H:
C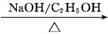 G
G H
H
写出G→H的化学方程式: 。
1.(20分)(2012·宁波模拟)幸福可以“人工合成”吗?精神病学专家通过实验发现,人体中的一种脑内分泌物多巴胺(结构简式如右图),可影响一个人的情绪。多巴胺是一种神经递质,用来帮助细胞传送脉冲的化学物质。这种脑内分泌物主要负责大脑的情欲、感觉,将兴奋及开心的信息传递,使人感到愉悦和快乐。多巴胺可由香兰素与硝基甲烷缩合,再经锌还原水解而得,合成过程如下:
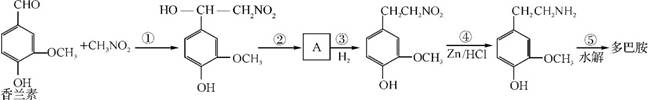
请回答下列问题:
(1)写出香兰素中含有的两种官能团名称是 、 。
(2)上述合成过程中属于加成反应的是 (填反应序号)。
(3)反应②的反应条件是 ;有机物A的结构简式为 。
(4)写出符合下列条件的多巴胺的所有同分异构体的结构简式: 。
(i)属于1,3,5 三取代苯 (ii)苯环上直接连有一个羟基和一个氨基 (iii)分别能与钠和氢氧化钠反应,消耗钠与氢氧化钠的物质的量之比为2∶1
三取代苯 (ii)苯环上直接连有一个羟基和一个氨基 (iii)分别能与钠和氢氧化钠反应,消耗钠与氢氧化钠的物质的量之比为2∶1
(5)多巴胺遇足量浓溴水会产生沉淀,请写出该反应的化学方程式: 。
23、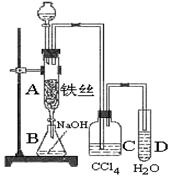 (12分)溴苯是一种用来合成医药、农药的重要原料,某化学课外活动小 组用如图装置制取溴苯。先向分液漏斗中加入苯和液溴,在A下端活塞关闭的前提下,再将混合液慢慢滴入反应器A中。
(12分)溴苯是一种用来合成医药、农药的重要原料,某化学课外活动小 组用如图装置制取溴苯。先向分液漏斗中加入苯和液溴,在A下端活塞关闭的前提下,再将混合液慢慢滴入反应器A中。
(1)写出A中反应的化学方程式
(2)实验结束时,打开A下端的活塞,让反应液流入B中,充 分振荡,静置,观察到下层 为 ,锥形瓶中加入NaOH溶液目的是
,C中盛放CCl4的作用是 ;
为 ,锥形瓶中加入NaOH溶液目的是
,C中盛放CCl4的作用是 ;
(3)能证明苯和液溴发生的是取代反应,而不是加 成反应,可向试管D中加入 溶液,现象是
;或者向试管D中加入 溶液,现象是
,则能证明该结论。
成反应,可向试管D中加入 溶液,现象是
;或者向试管D中加入 溶液,现象是
,则能证明该结论。
22.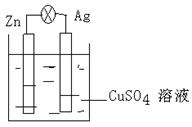 (8分)在银锌原电池中,以硫酸铜为电解质溶液。
(8分)在银锌原电池中,以硫酸铜为电解质溶液。
(1)锌为 极,电极反应式为 ,
(2)银电极上发生的是 反应(“氧化”或“还原”)。
银电极上观察到的现象是
(3)此电池转移1mol电子,电解质溶液质量的变化为 g
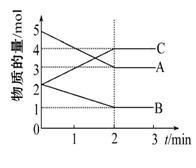
21. (12分)(1)A、B、C三种气体在体积为2L的密闭容器中发生反应,在不同反应时间各物质的量的变化情况如图所示。
①该 反应的化学方程式为 。
反应的化学方程式为 。
②从0~2min用C表示此反应的速率为 。
③此反应达到最大限度时A的转化率是
(2)某学生为了探究锌与盐酸反应过程中速率变化,在100 mL稀盐酸中加入足量的锌粉,标准状况下测得数据累计值如下:
|
时间(min) |
1 |
2 |
3源:Z。X。X。K] |
4 |
5 |
|
氢气体积(mL) |
50 |
120 |
232 |
290 |
310 |
①在0 min~1 min、1 min~2 min、2 min~3 min、3 min~4 min、4 min~5 min时间段中,反应速率最大的时间段是 ,原因为 ;
②在2 min~3 min时间段内,用 盐酸的浓度变化表示的反应速率为 。
盐酸的浓度变化表示的反应速率为 。
③为了减缓反应速率但不减少产生氢气的量,在盐酸中分别加入等体积的下列溶液,其中可行的是 。
A.蒸馏水 B. NaNO3溶液 C. Na2SO4溶液 D.CuSO4溶液
20. (6分)已知在高温、高压、催化剂 作用下,1 mol石墨转化为金刚石,吸收1.9 kJ的热量。
作用下,1 mol石墨转化为金刚石,吸收1.9 kJ的热量。
(1)该反应 (填“是”或“不是”)吸热反应。
(2)石墨和金刚石相比, 能量高, 更稳定。
 (3)推测石墨与金刚石各1 mol在相同条件下燃烧, 放出的热量多。
(3)推测石墨与金刚石各1 mol在相同条件下燃烧, 放出的热量多。
第二部分 非选择题
19.(8分)下表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白:
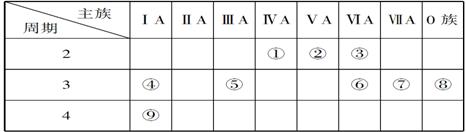
(1)在这些元素中,化学性质最不活泼的是________(填元素符号,下同)。
(2)在最高价氧化物的水 化物中,酸性最强的化合物的化学式:________,碱性最强的化合物的电子式:________。该化合物含有的化学键是
化物中,酸性最强的化合物的化学式:________,碱性最强的化合物的电子式:________。该化合物含有的化学键是
(3)最高价氧化物是两性氧化物的元素是________;写出它的氧化物与氢氧化钠反应的离子方程式:_______________________ _________________________________________。
18.现向一容积不变的2 L密闭容器中充入4 mol NH3和3 mol O2,发生反应4NH3(g)+3O2(g) 2N2(g)+6H2O(g),4
min后,测得生成的H2O占混合气体体积的40%,则下列表示此段时间内该反应的平均速率不正确的是( )
2N2(g)+6H2O(g),4
min后,测得生成的H2O占混合气体体积的40%,则下列表示此段时间内该反应的平均速率不正确的是( )
A.v(N2)=0.125 mol·L-1·min-1 B.v(H2O)=0.375 mol·L-1·min-1
C.v(O2)=0.225 mol·L-1·min-1 D.v(NH3)=0.250 mol·L-1·min-1
2013—2014学年下学期学期期中考试
高一年级化学学科 试 卷
本试卷分第Ⅰ卷和第Ⅱ卷两部分,满分为100分,答题时间为90分钟。考生作答时,选择题答案和非选择题答案答在答题卡上。考试结束后,将答题卡交回。
可能用到的相对原子质量:H:1 C:12 O:16 Na:23 Mg:24 S:32 Al:27 Cl:35.5 K:39 Ca:40 Br:80 Fe:56 Cu:6 4 Z
4 Z n:65
n:65
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com