
8.(2011·广雅三模)锌锰电池以氢氧化钾溶液为电解液,电池总反应式为Zn(s)+2MnO2(s)+H2O(l) Zn(OH)2(s)+Mn2O3(s)。下列说法错误的是( )
Zn(OH)2(s)+Mn2O3(s)。下列说法错误的是( )
A.电路中每通过0.2mol电子,锌的质量理论上减小6.5g
B.电池负极的电极反应式为Zn-2e-+2OH- Zn(OH)2
Zn(OH)2
C.电池工作时,电流由负极通过外电路流向正极
D.碱性锌锰电池是二次电池
二、双项选择题
7.(2011·广州模拟)已知下列过程都能自发进行,其中不能用“焓判据”解释的是( )
A.2Na(s)+Cl2(g) 2NaCl(s) ΔH<0
2NaCl(s) ΔH<0
B.C3H8(g)+5O2(g) 3CO2(g)+4H2O(l) ΔH<0
3CO2(g)+4H2O(l) ΔH<0
C.2NH4Cl(s)+Ca(OH)2(s) 2NH3(g)+CaCl2(s)+2H2O(l) ΔH>0
2NH3(g)+CaCl2(s)+2H2O(l) ΔH>0
D.NH4NO3(s) N
N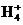 (aq)+N
(aq)+N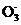 (aq) ΔH>0
(aq) ΔH>0
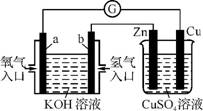
6.(2012·广州天河二模)右图装置中盛KOH溶液的部分是一个氢氧燃料电池,对此装置的分析合理的是( )
A.该装置中Cu极为正极
B.一段时间后锌片质量减少
C.b极的电极反应式为H2-2e- 2H+
2H+
D.一段时间后,硫酸铜溶液的浓度不变
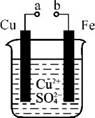
5.(2011·广东高考)某小组为研究电化学原理,设计如右图所示装置。下列叙述错误的是( )
A.a和b不连接时,铁片上会有金属铜析出
B.a和b用导线连接时,铜片上发生的反应为Cu2++2e- Cu
Cu
C.a和b分别连接足够电压的直流电源正、负极时,Cu2+向铜电极移动
D.无论a和b是否用导线连接,铁片均溶解,溶液从蓝色逐渐变成浅绿色
4.(2012·江苏高考)下列有关说法正确的是( )
A.CaCO3(s) CaO(s)+CO2(g)室温下不能自发进行,说明该反应的ΔH<0
CaO(s)+CO2(g)室温下不能自发进行,说明该反应的ΔH<0
B.镀铜铁制品镀层受损后,铁制品比受损前更容易生锈
C.N2(g)+3H2(g) 2NH3(g) ΔH<0,其他条件不变时升高温度,反应速率v(H2)和氢气的转化率均增大
2NH3(g) ΔH<0,其他条件不变时升高温度,反应速率v(H2)和氢气的转化率均增大
D.水的离子积常数Kw随着温度的升高而增大,说明水的电离是放热反应
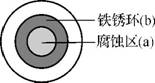
3.(2011·浙江高考)将NaCl溶液滴在一块光亮清洁的铁板表面上,一段时间后发现液滴覆盖的圆周中心区(a)已被腐蚀而变暗,在液滴外沿形成棕色铁锈环(b),如右图所示。导致该现象的主要原因是液滴之下氧气含量比边缘少。下列说法正确的是( )
A.液滴中的Cl-由a区向b区迁移
B.液滴边缘是正极区,发生的电极反应为O2+2H2O+4e- 4OH-
4OH-
C.液滴下的Fe因发生还原反应而被腐蚀,生成的Fe2+由a区向b区迁移,与b区的OH-形成Fe(OH)2,进一步氧化、脱水形成铁锈
D.若改用嵌有一铜螺丝钉的铁板,在铜铁接触处滴加NaCl溶液,则负极发生的电极反应为Cu-2e- Cu2+
Cu2+
2.碳酸铵[(NH4)2CO3]在室温下就能自发地分解产生氨气,对其说法正确的是( )
A.碳酸铵分解是因为生成了易挥发的气体,使体系混乱度增大
B.碳酸铵分解是吸热反应,根据能量判据不能自发分解
C.自发反应一定是熵增大,非自发反应一定是熵减小或不变
D.自发反应在任何条件下都能实现
一、单项选择题
1.(2011·惠州模拟)随着人们生活质量的不断提高,废电池集中处理的问题被提到议事日程,其首要原因是( )
A.回收电池外壳的金属材料
B.防止电池中汞、镉和铅等重金属离子对土壤和水源的污染
C.避免电池中渗泄的电解液腐蚀其他物品
D.回收其中石墨电极
12.(1)B (2)漏斗下端尖嘴未紧贴烧杯内壁
(3)AgNO3溶液(或硝酸酸化的AgNO3溶液) 坩埚
(4)除去HCl 吸收水蒸气 碱石灰(或NaOH与CaO的混合物)
11.(1)①Fe+H2SO4(稀)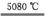 FeSO4+H2↑
FeSO4+H2↑
②Fe3++2Fe 3Fe2+ ③减少FeSO4的损失 防止空气进入试管将Fe2+氧化为Fe3+ ④有浅绿色晶体析出
3Fe2+ ③减少FeSO4的损失 防止空气进入试管将Fe2+氧化为Fe3+ ④有浅绿色晶体析出
(2)①Fe2++2HC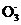
 FeCO3↓+CO2↑+H2O
FeCO3↓+CO2↑+H2O
②FeCO3 FeO+CO2↑ CO2+C
FeO+CO2↑ CO2+C 2CO
2CO
FeO+CO Fe+CO2
Fe+CO2
③过滤 N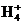 +H2O
+H2O NH3·H2O+H+,温度过高,NH3挥发使平衡向右移动,溶液酸性增强,生成NH4HSO4
NH3·H2O+H+,温度过高,NH3挥发使平衡向右移动,溶液酸性增强,生成NH4HSO4
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com