
一、选择题
1、下列有机物的系统命名中正确的是( )
A.3-甲基-4-乙基戊烷 B.2,3-二甲基戊烷
C.3,4,4-三甲基已烷 D.3,5-二甲基已烷
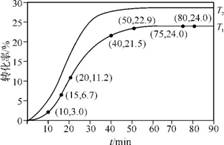
8. (1) 0.045 9.0×10-3 (2)①反应初期:虽然甲酸甲酯的量较大,但甲酸量很小,催化效果不明显,反应速率较慢。②反应中期:甲酸量逐渐增多,催化效果显著,反应速率明显增大。③反应后期:甲酸量增加到一定程度后,浓度对反应速率的影响成主导因素,特别是逆反应速率的增大,使总反应速率逐渐减小,直至为零。该反应中甲酸具有催化作用
(3) 0.14
(4)
7.
(1)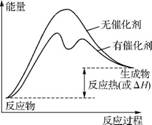
(2)升高温度,增大反应物N2的浓度,不断移出生成物脱离反应体系
(3)①66.7% ②0.005
6.
(1) 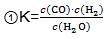 ②BC (2)
Z 催化效率高且活性温度低(或催化活性高,速度快,反应温度低,产率高) (3)> (4)提高原料利用率(或提高产量、产率)
②BC (2)
Z 催化效率高且活性温度低(或催化活性高,速度快,反应温度低,产率高) (3)> (4)提高原料利用率(或提高产量、产率)
5. (1)①B、C ②K=c(CO2)·c2(NH3)=1.6×3.22×10-9=1.64×10-8(mol·L-1) ③增加 ④> > (2)①0.05 mol·L-1·min-1 ②25.0 ℃时,反应物的起始浓度较小,但06 min的平均反应速率(曲线的斜率)仍比15.0 ℃时的大
0.70-x x x
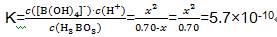
得出x=2.0×10-5mol·L-1
(3) BD
0.70 0 0
转化浓度/mol·L-1:
x x x
平衡浓度/mol·L-1:
4.
(1)
2H3BO3 B2O3+3H2O↑
B2O3+3H2O↑
(2)①H3BO3+OH- [B(OH)4]-
[B(OH)4]-
②H3BO3(aq)+H2O
(l) [B(OH)4]-(aq)+H+(aq)
[B(OH)4]-(aq)+H+(aq)
起始浓度/mol·L-1:
3. (1)①0.56 ②减小CO2的浓度 ③<
(2) CH4(g)+2NO2(g) N2(g)+CO2(g)+2H2O(l) ΔH=-955
kJ·mol-1
N2(g)+CO2(g)+2H2O(l) ΔH=-955
kJ·mol-1
(3) NO2+N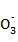 -e-
-e- N2O5
N2O5
2.
(1)
N2H4(l)+O2(g) N2(g)+2H2O(l) ΔH=-621.8
kJ·mol-1 (2) H2O2
N2(g)+2H2O(l) ΔH=-621.8
kJ·mol-1 (2) H2O2 H
H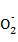 +H+ (3)①2S
+H+ (3)①2S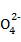 -2e-
-2e- S2
S2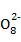
②(NH4)2S2O8+2H2O H2O2+(NH4)2SO4+H2SO4
H2O2+(NH4)2SO4+H2SO4
(4)①8.0×10-6 ②过氧化氢在温度过高时迅速分解 ③反应速率趋向于零
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com