
22.下列有关实验原理或实验操作正确的是( )
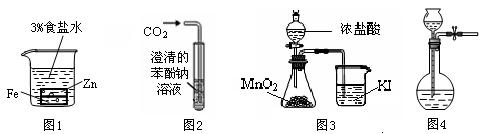
A.图1中正极反应是Zn-2e-=Zn2+
B.图2可用于比较碳酸、苯酚酸性的强弱
C.图3可以用于比较MnO2、Cl2、I2氧化性强弱
D.图4可用于检查装置气密性
2 3.室温下,某浓度的醋酸溶液中n(CH3COO—)=0.01mol,下列叙述正确的是( )
3.室温下,某浓度的醋酸溶液中n(CH3COO—)=0.01mol,下列叙述正确的是( )
A.向该醋酸溶液中加入等体积等浓度的盐酸,抑制醋酸的电离,溶液中c(H+)增大
B.若醋酸溶液体积为1L,则c(CH3COOH)=0.01mol/L
C.与NaOH恰好中和时,溶液中c(Na+)<c(CH3COO—)
D.与等体积等浓度的醋酸钠溶液混合,溶液中c(Na+)+ c(H+)=c(CH3COO—)+ c(OH—)
12.下列有关物质的性质和该性质的应用均正确的是( )
A.氯气具有酸性,可与烧碱或石灰乳反应制备含氯消毒剂
B.稀硝酸具有强氧化性,常温下可用铝罐盛装
C.氢氟酸具有弱酸性,可用氢氟酸雕刻玻璃
D.氢氧化铝是两性氢氧化物,可用与治疗胃酸过多
11.下列物质的应用不涉及氧化还原反应的是 ( )
A.用稀硝酸洗去附在试管内壁的银镜
B.用热的纯碱溶液清洗油污
C.用新制的氢氧化铜悬浊液与病人的尿液混合加热,来检验病人是否患糖尿病
D.在铁质镀件上镀铜
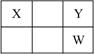
10.X、Y、Z、W、Q是原子序数依次增大的五种短周期主族元素。其中Z是金属,W的单质是淡黄色固体,X、Y、W在周期表中的相对位置关系如右下图所示,下列说法一定正确的是
 A.最高价氧化物对应水化物的酸性最强的是W
A.最高价氧化物对应水化物的酸性最强的是W
B.Y与Z只能形成一种化合物
C.简单阴离子还原性:Y>W
D.Z与Q形成的化合物水溶液可能显酸性
9.用NA表示阿伏加德罗常数的值。下列叙述正确的是
A.18 g的D216O中含有的中子数为9 NA
B.物质的量浓度均为1.0mol/L的硫酸与高氯酸(HClO4)溶液中含有的氧原子数均为4NA
C.33.6 L NO2溶于足量的水得到的溶液中含有的NO数为NA
D.32 g铜发生氧化还原反应,一定失去NA个电子
8.下列离子在溶液中能大量共存的一组是
A.Fe3+、H+、ClO-、SO32- B.K+、Al3+、Cl-、CO32-
C.Na+、Ca2+、HCO3-、OH- D.Fe2+、NH4+、NO3-、SO42-
7.下列关于有机物的叙述正确的是
A.棉花和合成纤维的主要成分都是纤维素
B.蛋白质溶液中加入浓的硫酸铵溶液会发生变性
C.乙酸乙酯中混有的乙酸杂质可以用饱和碳酸钠溶液除去
 D.由
D.由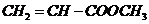 合成的聚合物为
合成的聚合物为 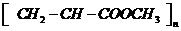
12.(10分)通过粮食发酵可获得某含氧有机化合物X,其相对分子质量为46,其中碳的质量分数为52.2%,氢的质量分数为13.0%。
(1)X的分子式是 。
(2)X与金属钠反应放出氢气,反应的化学方程式是 。
(3)X与空气中的氧气在铜或银催化下反应生成Y,Y的结构简式是 。
(4)X与酸性高锰酸钾溶液反应可生成Z。在加热和浓硫酸作用下,X与Z反应可生成一种有香味的物质W,若184 g X和120 g Z反应能生成106 g W,计算该反应的产率(要求写出计算过程)。
解析:(1)根据题意,X的分子中含碳原子数为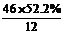 ≈2,含氢原子数为
≈2,含氢原子数为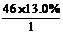 ≈6,含氧原子数为
≈6,含氧原子数为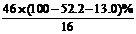 ≈1,所以X的分子式为C2H6O。
≈1,所以X的分子式为C2H6O。
(2)结合题意及上述分析可知X是乙醇。乙醇与钠反应的化学方程式为2Na+2CH3CH2OH 2CH3CH2ONa+H2↑。
2CH3CH2ONa+H2↑。
(3)X(乙醇)与空气中的O2在铜或银作催化剂的条件下反应生成Y(乙醛),其结构简式为CH3CHO。
(4)X(乙醇)与酸性高锰酸钾溶液反应可生成Z(乙酸)。乙酸与乙醇反应,生成乙酸乙酯(W),根据化学方程式:CH3COOH+CH3CH2OH CH3COOC2H5+H2O,可知184 g 乙醇过量,应用120 g Z计算所得的乙酸乙酯,设理论上可以生成乙酸乙
CH3COOC2H5+H2O,可知184 g 乙醇过量,应用120 g Z计算所得的乙酸乙酯,设理论上可以生成乙酸乙 酯的质量为a。则有
酯的质量为a。则有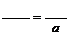 ,a=176 g。所以该反应的产率为
,a=176 g。所以该反应的产率为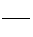 ×100%=60.2%。
×100%=60.2%。
答案:(1)C2H6O(2分)
(2)2Na+2CH3CH2OH 2CH3CH2ONa+H2↑(3分)
2CH3CH2ONa+H2↑(3分)
(3)CH3CHO(2分)
(4)60.2%(3分)
11.(10分)已知A是一种相 对分子质量为28的气态烃,现以A为主要原料合成一种具有果香味的物质E,其合成路线如下图所示。
对分子质量为28的气态烃,现以A为主要原料合成一种具有果香味的物质E,其合成路线如下图所示。
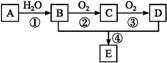
请回答下列问题:
(1)写出A的结构简式 。
(2)B、D分子中的官能团名称分别是 、 。
(3)物 质B可以被直接氧化为D,需要加入的试剂是 。
质B可以被直接氧化为D,需要加入的试剂是 。
(4)写出下列反应的化学方程式及其反应类型。
① ;反应类型: 。
④ ;反应类型: 。
解析:A是一种相对分子质量为28的气态烃,则最多含两个碳,所以是乙烯。乙烯与水发生加成反应生成乙醇(B),乙醇被氧化生成乙醛(C),乙醛进一步被氧化生成乙酸(D) ,乙醇与乙酸发生酯化反应,生成乙酸乙酯(E)。
,乙醇与乙酸发生酯化反应,生成乙酸乙酯(E)。
答案:(1)CH2 CH2(1分)
CH2(1分)
(2)羟基 羧基(各1分)
(3)酸 性高锰酸钾溶液或酸性重铬酸钾溶液(1分)
性高锰酸钾溶液或酸性重铬酸钾溶液(1分)
(4)CH2 CH2+H2O
CH2+H2O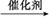 CH3CH2OH(1分) 加成反应(2分)
CH3CH2OH(1分) 加成反应(2分)
CH3COOH+CH 3CH2OH
3CH2OH
CH3COOCH2CH3+H2O(2分) 取代反应(1分)
10.(6分)(1)苯、四氯化碳、乙醇都是常见的有机溶剂。能与水互溶的是 ;难溶于水,且密度比水小的是 。
(2)一瓶无色气体,可能含有CH4和CH2 CH2,也可能是其中的一种,与一瓶Cl2混合后光照,观察到黄绿色逐渐褪去,瓶壁有无色油状小液滴。
CH2,也可能是其中的一种,与一瓶Cl2混合后光照,观察到黄绿色逐渐褪去,瓶壁有无色油状小液滴。
①由上述实验现象推断出该混合气体中一定含有CH4,你认为是否正确,说明理由。
。
②上述实验过程中可能涉及的反应类型有: 。
解析:熟悉常见有机 溶剂的应用,掌握简单烃的化学、物理性质,并能推知其同系物的性质。
溶剂的应用,掌握简单烃的化学、物理性质,并能推知其同系物的性质。
答案:(1)乙醇(1分) 苯(1分)
(2)①不正确。(1分)因为CH2 CH2也可以与Cl2发生加成反应,从而使黄绿色逐渐褪去,生成的CH2Cl—CH2Cl也是油状液体(2分)
CH2也可以与Cl2发生加成反应,从而使黄绿色逐渐褪去,生成的CH2Cl—CH2Cl也是油状液体(2分)
②取代反应和加成反应(1分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com