
27.工业制硫酸中的一步重要反应是SO2的催化氧化: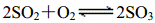 (正反应放热),下列有关说法正确的是
(正反应放热),下列有关说法正确的是
A.升高温度只提高逆反应速率 B.降低温度可提高正反应速率
C.使用催化剂能显著增大反应速率 D.达到化学平衡时正、逆反应速率相等
26. 下列有关试剂的保存方法中,不正确的是
A.漂白粉存放在敞口容器中
B.液溴应保存在棕色细口瓶,并加水液封
C.浓硝酸通常保存在棕色玻璃试剂瓶中
D.氢氧化钠溶液用带磨口玻璃塞的试剂瓶贮存
二、双项选择题
25.下列有关化学用语使用正确的是
A.硫酸的电离方程式: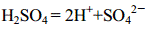
B.纯碱的化学式:NaHCO3
C.硫原子的原子结构示意图:
D.中子数为20的钙原子: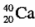
24.为了探究温度对化学反应速率的影响,下列实验方案可行的是
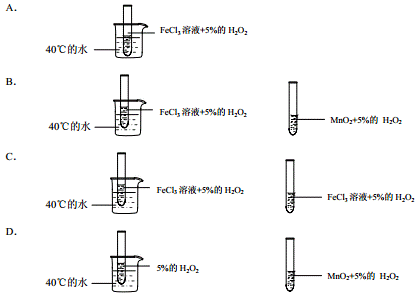
23.有一种银锌微型钮扣电池,其电极分别是Ag2O和Zn,电解质溶液为KOH,电极反应
为: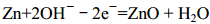 ,
, 。总反应为:Ag2O + Zn =2Ag + ZnO。根据上述反应式,判断下列叙述中,正确的是
。总反应为:Ag2O + Zn =2Ag + ZnO。根据上述反应式,判断下列叙述中,正确的是
A.在使用过程中,电池负极区溶液pH增大
B.在使用过程中,电子由Ag2O极经外电路流向Zn极
C.在使用过程中,Zn电极发生还原反应,Ag2O电极发生氧化反应
D.外电路中每通过0.2mol电子,正极的质量理论上减小1.6g
22.能够用于鉴别SO2和CO2两种无色气体的溶液是
A.品红溶液 B.BaCl2溶液 C.紫色石蕊试液 D.澄清石灰水
21.根据元素周期律判断,下列表述正确的是
A.酸性强弱:H3PO4>H2SO4 B.金属性:Na>Al
C.碱性强弱:NaOH<Mg(OH)2D. 原子半径:Cl>Na
20.元素周期表对工农业生产具有一定的指导作用,下列说法不正确的是
A. 用于制农药的元素通常位于周期表的右上角
B. 半导体材料在金属元素和非金属元素的分界线附近
C. 在过渡元素中可以找到新型催化剂
D. 在IA族元素中寻找新型耐高温、耐腐蚀的材料
19.一定条件下N2和H2在密闭容器中反应生成NH3。已知它们的起始浓度N2是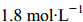 ;H2 是
;H2 是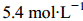 ,10min后测得N2的浓度是
,10min后测得N2的浓度是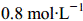 ,则在这10min内NH3的平均反应
,则在这10min内NH3的平均反应
速率是
A.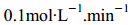 B.
B.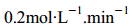
C.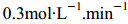 D.
D.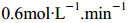
18.海水资源的利用包括海水的淡化,以下方法中,不能淡化海水的是
A.蒸馏法 B.过滤法
C.电渗析法 D.离子交换法
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com