
32. (18分)遗传学上,将同源染色体中有一个是易位染色体的生物个体称为易位杂合体,将同源染色体都含有相同易位片段的生物个体称为“易位纯合体”。下图甲、乙分别代表某种植物两个不同个体细胞的部分染色体与基因组成,其中高茎(A)对矮茎(a)显性,卷叶(B)对直叶(b)显性,红花(C)对白花(c)显性,请回答:
(18分)遗传学上,将同源染色体中有一个是易位染色体的生物个体称为易位杂合体,将同源染色体都含有相同易位片段的生物个体称为“易位纯合体”。下图甲、乙分别代表某种植物两个不同个体细胞的部分染色体与基因组成,其中高茎(A)对矮茎(a)显性,卷叶(B)对直叶(b)显性,红花(C)对白花(c)显性,请回答:
(1)从染色体组成看,两植株中,正常的植株是 植株,从变异来源看,另一植株发生了何种变异? 。
(2)若该种植物的配子失去图示三种基因中的任意一种,都会导致配子死亡。(不考虑同源染色体的交叉互换)
① 植株乙自交后代中易位纯合体占 。
② 为了区分某高茎卷叶红花植株是甲类型还是乙类型,工作人员选择若干未发生染色体易位的矮茎直叶白花植株对其进行测交。
预期结果与结论:
若测交后代有4种表现型,则该高茎卷叶红花植株是甲类型;
若 ,则该高茎卷叶红花植株是乙类型。
写出被测植株为乙类型时的遗传图解。
(3) 拟采用转基因技术培育抗虫植株。通常将抗虫基因和农杆菌的Ti 质粒连接,形成 ,再转移到该植株的培养细胞中,然后常根据质粒上的 进行筛选,再通过植物 获得转基因抗虫植株。
31.(12分)美国纽约大学生物研究所科研人员从苦瓜中提取到一种生物活性物质P,通过细胞培养实验证明:该活性物质能促进外周组织细胞吸收和利用葡萄糖;研究人员利用该活性物质研制了一种新型的天然降血糖药物X。已知药物使用的途径常用的有静脉注射和口服两种形式,为了进一步探究药物X的正确给药途径,研究人员设计了以下实验:
材料用具:实验小鼠200只,生理盐水,适宜浓度活性物质X溶液,注射器,血糖测定仪。
(说明:①实验小鼠的各项生理指标相同且符合实验要求;②将小鼠处理成高血糖小鼠和血糖测定的具体方法不要求)
(1)实验目的:_______________________________________________________________。
(2)实验思路:
①将实验小鼠均分为四组,编为A、B、C、D,其中将B、C、D处理成高血糖小鼠,用血糖测定仪分别测量各组小鼠空腹血糖浓度,统计处理并记录。
②_______________________________________________________________________
③在___________条件下培养一定时间后,再次用血糖测定仪分别测量各组小鼠空腹血糖浓度,统计处理并记录。分析比较各组小鼠前后血糖浓度变化。
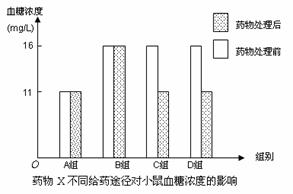 (3)结果与结论:研究人员在实验过程中用表格和直方图形式分别记录了实验结果,但记录表因故遗失,直方图如右图。
(3)结果与结论:研究人员在实验过程中用表格和直方图形式分别记录了实验结果,但记录表因故遗失,直方图如右图。
①请根据直方图还原实验结果记录表:
②根据图表分析,该实验的结论是______________________________________。
30.(14分)荔枝叶片在发育过程中,净光合速率及相关指标的变化如曲线所示。(说明:净光合速率是指在光照条件下,植物从外界环境吸收的CO2总量)

请分析回答:
(1)在发育过程中的BC阶段,净光合速率较低,推测原因可能是:①
;② 。在此阶段适当增加光照强度,荔枝叶片的净光合速率 (填“增大”、“减小”或“基本不变”)
(2)将处于A、D发育时期的两株荔枝分别置于光照、温度恒定的密闭容器中,一段时间后,A时期的叶肉细胞中开始积累 ,是由于 ,导致叶肉细胞进行厌氧呼吸;D时期的叶肉细胞中,短时间内3-磷酸甘油酸的含量将 。
(3)生产实践中,可适时喷洒植物激素中的 ,促进叶的生长,起到促进新叶展开的作用。
29.(15分)某课题组以甲苯为主要原料,采用以下路线合成7-氨基异喹啉:

已知: 。请回答下列问题:
。请回答下列问题:
(1)对于化合物E,下列说法正确的是 。
A.E的分子式为C9H10NO B.E可发生加成反应
C.E分子中含有醛基 D.E可发生水解反应
(2)A→B反应所需的试剂和反应条件为 ;B→C反应的反应类型是 。
(3)写出C→D反应的化学方程式 。
(4)化合物C在酸性条件下水解生成羧酸X,写出同时符合下列条件的X的所有同分异构体的结构简式 。
①分子中含有苯环;②分子中共有4种不同化学环境的氢原子;③能发生银镜反应。
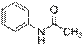 (5)以苯和乙酸乙酯为原料可合成乙酰苯胺(
),请设计合成路线(无机试剂及溶剂任选)。
(5)以苯和乙酸乙酯为原料可合成乙酰苯胺(
),请设计合成路线(无机试剂及溶剂任选)。
注:合成路线的书写格式参照如下实例流程图:
CH3CHO CH3COOH
CH3COOH CH3COOCH2CH3
CH3COOCH2CH3
28.(14分)高锰酸钾是一种用途广泛的强氧化剂,实验室制备高锰酸钾所涉及的化学方程式如下:MnO2熔融氧化:3MnO2+ KClO3+ 6KOH  3K2MnO4+ KCl+3H2O ;
3K2MnO4+ KCl+3H2O ;
K2MnO4歧化:3K2MnO4+ 2CO2=2KMnO4+ MnO2↓+2K2CO3 。
已知K2MnO4溶液显绿色。请回答下列问题:
(1)MnO2熔融氧化应放在 中加热(填仪器编号)。
①烧杯 ②瓷坩埚 ③蒸发皿 ④铁坩埚
(2)在MnO2熔融氧化所得产物的热浸取液中通入CO2气体,使K2MnO4歧化的过程在如图装置中进行,A、B、C、D、E为旋塞,F、G为气囊,H为带套管的玻璃棒。

①为了能充分利用CO2,装置中使用了两个气囊。当试管内依次加入块状碳酸钙和盐酸后,关闭旋塞B、E,微开旋塞A, 打开旋塞C、D,往热K2MnO4溶液中通入CO2气体,未反应的CO2被收集到气囊F中。待气囊F收集到较多气体时,关闭旋塞 ,打开旋塞 ,轻轻挤压气囊F,使CO2气体缓缓地压入K2MnO4溶液中再次反应,未反应的CO2气体又被收集在气囊G中。然后将气囊G中的气体挤压入气囊F中,如此反复,直至K2MnO4完全反应。
②检验K2MnO4歧化完全的实验操作是 。
(3)将三颈烧瓶中所得产物进行抽滤,将滤液倒入蒸发皿中,蒸发浓缩至 ,自然冷却结晶,抽滤,得到针状的高锰酸钾晶体。本实验应采用低温烘干的方法来干燥产品,原因是________________。
(4)利用氧化还原滴定法进行高锰酸钾纯度分析,原理为:
2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O
现称取制得的高锰酸钾产品7.245g,配成500mL溶液,用移液管量取25.00 mL待测液,用0.1000 mol·L-1草酸钠标准溶液液进行滴定,终点时消耗标准液体积为50.00mL(不考虑杂质的反应),则高锰酸钾产品的纯度为 (保留4位有效数字,已知M(KMnO4)=158g·mol-1)。若移液管用蒸馏水洗净后没有用待测液润洗或烘干,则测定结果将 。(填“偏大”、“偏小”、“不变”)
27. (14分)氢气是清洁的能源,也是重要的化工原料,有关氢气的制取研究是一个有趣的课题。根据提供两种制氢方法,完成下列各题:
(14分)氢气是清洁的能源,也是重要的化工原料,有关氢气的制取研究是一个有趣的课题。根据提供两种制氢方法,完成下列各题:
(1)方法一:H2S热分解法,反应式为:
2H2S(g)
 2H2(g)+S2(g) △H
2H2(g)+S2(g) △H
在恒容密闭容器中,控制不同温度进行H2S的分解实验。H2S的起始浓度均为c mol·L-1。不同温度下反应相同时间t后,测得如图所示H2S转化率曲线图。其中a为平衡转化率与温度关系曲线,b为未达到平衡时转化率与温度的关系曲线。
①△H 0(“>”、 “<”或“=”),
②若985℃时,反应经t min达到平衡,此时H2S的转化率为40%,则t min内反应速率v(H2)= (用含c、t的代数式表示)。
③请说明随温度的升高,曲线b向曲线a逼近的原因: 。
(2)方法二:以CaO为吸收体,将生物材质(以C计)与水蒸气反应制取H2。反应装置由气化炉和燃烧炉两个反应器组成,相关反应如下表所示:
|
流程1:气化炉中产生H2 |
流程2:燃烧炉中CaO再生 |
|
通入水蒸气,主要化学反应: I: C(s)+H2O(g)=CO(g)+H2(g) K1 II: CO(g)+ H2O(g) =CO2(g)+ H2(g) K2 III:CaO(s)+CO2(g)=CaCO3(s) K3 |
通入纯氧,主要化学反应: IV: C(s) +O2(g)= CO2(g) △H= -393.8 kJ·mol-1 V: CaCO3(s)=CaO(s) + CO2(g) |
①反应C(s)+2H2O(g)+CaO(s)=CaCO3(s)+2H2(g) K= 。(用K1、K2、K3表示)
 ②右图为反应I在一定温度下,平衡时各气 体体积百分含量随压强变化的关系图。若反应达某一平衡状态时,测得c(H2O)=2c(H2)=2c(CO)=2mol·L-1,试根据H2O的体积百分含量变化曲线,补充完整CO的变化曲线示意图。
②右图为反应I在一定温度下,平衡时各气 体体积百分含量随压强变化的关系图。若反应达某一平衡状态时,测得c(H2O)=2c(H2)=2c(CO)=2mol·L-1,试根据H2O的体积百分含量变化曲线,补充完整CO的变化曲线示意图。
③对于可逆反应C(s)+2H2O(g)+CaO(s)  CaCO3(s)
+2H2(g),△H= -87.9 kJ·mol-1;采取以下措施可以提高H2产量的是
。(填字母编号)
CaCO3(s)
+2H2(g),△H= -87.9 kJ·mol-1;采取以下措施可以提高H2产量的是
。(填字母编号)
A.降低体系的温度
B.使各气体组分浓度均加倍
C.适当增加水蒸气的通入量
D.增加CaO的量,提高CO2的吸收率?
(3)方法二与方法一相比其优点有 (写一个即可)。
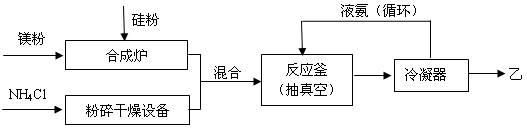
26.(15分)硅基太阳电池需用化合物甲作钝化材料,甲的摩尔质量为140 g·mol-1,其中硅元素的质量分数为60%。已知1 molNH3与足量的化合物乙充分反应后可得到35 g 甲与6 g H2。工业上制乙的流程如下:
请回答下列问题:
(1)乙的电子式是 ;比较热稳定性:乙_______NH3(填>,<或=)。
(2)NH3与足量的化合物乙反应制甲的化学方程式是 。
(3)合成炉内物质需在保护气氛下高温合成,下列气体可作保护气的有 (填字母编号)。
A.O2 B.H2 C.N2 D.CO2 E.Ar
(4)上述生产乙的过程中液氨的作用是_________________________________________。
(5)甲与少量H2SO4溶液反应只得到H2SiO3和盐M两种产物,写出该反应的离子方程式 。请设计验证产物盐M的实验方案 。
25. (22分) 如图所示,在平面直角坐标系O点处有一粒子源,该粒子源可向x ³ 0的范围内发射比荷 C/kg的带正电粒子,粒子速度范围为
C/kg的带正电粒子,粒子速度范围为 (c为真空中的光速), 在0£x< 1m的I区域存在垂直于坐标平面向外、磁感强度B1=1T的匀强磁场,在1m£x£3 m的II区域存在垂直坐标平面向里、磁感强度B2 =
0.5T的匀强磁场,不计粒子重力。
(c为真空中的光速), 在0£x< 1m的I区域存在垂直于坐标平面向外、磁感强度B1=1T的匀强磁场,在1m£x£3 m的II区域存在垂直坐标平面向里、磁感强度B2 =
0.5T的匀强磁场,不计粒子重力。
(1) 速度多大的粒子不可能进入II区域? 并指出这些粒子在y轴上射出的范围。
 (2) 对能从(1m, 0)点进入II区域的粒子, 它在O点发射速度的方向(用与x轴正向夹角q表示)与其大小满足的什么关系? 在O点发射的什么方向范围内的粒子才有可能经过(1m, 0)点?
(2) 对能从(1m, 0)点进入II区域的粒子, 它在O点发射速度的方向(用与x轴正向夹角q表示)与其大小满足的什么关系? 在O点发射的什么方向范围内的粒子才有可能经过(1m, 0)点?
(3) 对在O点与+y方向成45°角入射的粒子,在答题卡的图上用圆规和直尺作出它们在x=3m边界上射出的范围,并在各射出点标出速度矢量(要求你画的图能表明各速度的矢量长短关系及方向关系)。
(图中要留下清晰的作图痕迹, 使阅卷者能看得清你的作图过程, 不要求写出作图依据和作图过程)
24. (20分) 如图所示,在空间有两个磁感强度均为B的匀强磁场区域,上一个区域边界AA¢与BB¢的间距为H,方向垂直纸面向里,CC¢与BB¢的间距为h, CC¢下方是另一个磁场区域,方向垂直纸面向外。现有一质量为m,边长为L(0.5H < L < H;h < L)的正方形线框由AA¢上方某处竖直自由落下,线框总电阻为R,已知当线框cd边到达AA¢和BB¢正中间时加速度大小为g。
(20分) 如图所示,在空间有两个磁感强度均为B的匀强磁场区域,上一个区域边界AA¢与BB¢的间距为H,方向垂直纸面向里,CC¢与BB¢的间距为h, CC¢下方是另一个磁场区域,方向垂直纸面向外。现有一质量为m,边长为L(0.5H < L < H;h < L)的正方形线框由AA¢上方某处竖直自由落下,线框总电阻为R,已知当线框cd边到达AA¢和BB¢正中间时加速度大小为g。
(1) 判断线框穿入磁场至加速度大小为g的过程中是做加速还是减速运动,并说明判断依据。
(2) 求cd到达AA¢和BB¢正中间时线框速度。
(3) 若cd边进 入CC¢前的瞬间线框的加速度大小变为0.8g, 则线框进入CC¢后的瞬间线框的加速度多大?
(4) 求: cd边在AA¢和BB¢正中间位置到cd边刚穿进CC¢ 的过程中线框发热量。
23.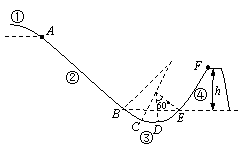 (16分)自由式滑雪空中技巧是一项有极大观赏性的运动,其场地由①出发区、②助滑坡、③过渡区(由两段不同半径的圆弧平滑相连,其中CDE弧的为半径3m,DE弧的圆心角60º)、④ 跳台(高度可选)组成。比赛时运动员由A点进入助滑区做匀加速直线运动,经过渡区后沿跳台的斜坡匀减速滑至跳台F处飞出,运动员的空中动作一般在54km/h到68km/h的速度下才能成功完成,不计摩擦和空气阻力,取g=10m/s2,求:
(16分)自由式滑雪空中技巧是一项有极大观赏性的运动,其场地由①出发区、②助滑坡、③过渡区(由两段不同半径的圆弧平滑相连,其中CDE弧的为半径3m,DE弧的圆心角60º)、④ 跳台(高度可选)组成。比赛时运动员由A点进入助滑区做匀加速直线运动,经过渡区后沿跳台的斜坡匀减速滑至跳台F处飞出,运动员的空中动作一般在54km/h到68km/h的速度下才能成功完成,不计摩擦和空气阻力,取g=10m/s2,求:
(1) 某运动员选择由A点无初速滑下,测得他在②、④两段运动时间之比为t1:t2=3:1,,且已知 ,则运动员在这两坡段运动平均速度之比及加速度之比各为多少?
,则运动员在这两坡段运动平均速度之比及加速度之比各为多少?
(2) 另一质量60kg的运动员,选择高h = 4 m的跳台,他要成功完成动作,在过渡区最低点D处至少要承受多大的支持力。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com