
19.在一个密闭容器中盛有N2和H2,它们的起始浓度分别是1.8 mol/L和5.4 mol/L,在一定的条件下它们反应生成NH3,10 min后测得N2的浓度是0.8 mol/L,则在这10 min内NH3的平均反应速率是( )。
A.0.1 mol/(L·min) B.0.2 mol/(L·min)
C.0.3 mol/(L·min) D.0.6 mol/(L·min)
18. 可逆反应2SO2+O2 2SO3达到平衡的标志是( )。
可逆反应2SO2+O2 2SO3达到平衡的标志是( )。
①消耗2 mol SO2的同时生成2 mol SO3
②SO2、O2与SO3的物质的量之比为2∶1∶2
③反应混合物中,SO3的质量分数不再改变
A.①② B.①③ C.只有③ D.全部
17.下列变化是因原电池反应而引起的是( )。
A.在空气中金属铝表面迅速氧化形成保护膜
B.常温下,铁被浓硫酸“钝化”形成保护膜
C.在潮湿的空气中钢铁易生锈
D.在潮湿的空气中过氧化钠易变质
16.已知:①能量越低的物质越稳定,②白磷转化成红磷放出热量。据此,下列判断或说法中正确的是( )。
A.在相同的条件下,红磷比白磷稳定 B.在相同的条件下,白磷比红磷稳定
C.红磷和白磷的结构相同 D.红磷容易发生自燃而白磷则不会自燃
15.下列实验中,反应速率的加快由催化剂引起的是( )。
A.在炭粉中加入KClO3,点燃时燃烧更为剧烈
B.锌与稀硫酸反应中加入少量CuSO4溶液而使反应放出H2的速率加快
C.固态FeCl3和固体NaOH混合后,加入水能迅速产生沉淀
D.双氧水中加入少量MnO2,即可迅速放出气体
14.下列说法中不正确的是( )。
A.用完的电池不可以随意地丢弃
B.增加炼铁高炉的高度不可以降低尾气中CO的含量
C.无论加入正催化剂还是加入负催化剂都能大大提高化学反应速率
D.把煤粉碎后再燃烧可以提高煤的燃烧效率
13.镍氢电池的总反应式是H2+2NiO(OH) 2Ni(OH)2,根据此反应式判断,此电池放电时,负极上发生反应的物质是( )。
A.NiO(OH) B.Ni(OH)2
C.H2 D.H2和NiO(OH)
12.在反应:C+CO2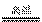 2CO中,可使反应速率增大的措施是( )。
2CO中,可使反应速率增大的措施是( )。
①增大压强 ②升高温度 ③通入CO2 ④增加碳的量 ⑤降低压强
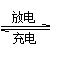 A.①②③④ B.②③④⑤ C.①②③ D.②③④
A.①②③④ B.②③④⑤ C.①②③ D.②③④
11.下列说法正确的是( )。
A.化学电池的放电过程就是电能转化为化学能的过程
B.化学电池中电子由正极流出,经外电路流向负极
C.燃料电池两极板均发生氧化还原反应
D.燃料电池工作时,通常是将空气通向正极
10.X、Y、Z都是金属,把X浸入Z的硝酸盐溶液中,X表面有Z析出,X与Y组成原电池时,Y为负极。X、Y、Z三种金属的活动性顺序为( )。
A.X>Y>Z B.X>Z>Y C.Y>X>Z D.Y>Z>X
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com