
二、非选择题
17. (9分)(2011·佛山高二检测)在一个U形管里盛有CuCl2溶液,并插入两块锌片作电极,按如图连接。
(9分)(2011·佛山高二检测)在一个U形管里盛有CuCl2溶液,并插入两块锌片作电极,按如图连接。
(1)如果把电键K接A,该装置应是电解装置,Zn①极是________极,电极反应式为____________________,Zn②极是________极,电极反应式为__________________________。
(2)上述反应进行5 min后,转换电键K到C,则这个装置是原电池装置,Zn①极是________极,电极反应式为________。
(3)上述装置进行2 min后,再转换电键K到B,则Zn①极发生的化学反应为________________________________________________________________________,
Zn②极发生的有关电化学的反应为_________________________________________。
解析:当电键K接触A点时,构成一个有外接直流电源的电解池装置,与电源正极相连的Zn①极是阳极,与电源负极相连的Zn②极是阴极。当工作5 min后,Zn②极上析出了Cu,此时,将电键K接触C点,构成一个原电池装置,表面覆盖铜的Zn②极是原电池的正极,Zn①极是原电池的负极。当把电键K接触B点时,形成断路,Zn①极发生Zn与CuCl2的置换反应,Zn②极由于在锌的表面有铜,又浸在CuCl2溶液中,发生电化学腐蚀。
答案:(1)阳 Zn-2e-===Zn2+
阴 Cu2++2e-===Cu (2)负 Zn-2e-===Zn2+
(3)Zn+CuCl2===ZnCl2+Cu
负极:Zn-2e-===Zn2+,
正极:Cu2++2e-===Cu
16. (2011·北京海淀区期末练习)已知在pH为4~5的溶液中,Cu2+几乎不水解,而Fe3+几乎完全水解。某学生拟用电解CuSO4溶液的方法测定铜的相对原子质量。该同学向pH=3.8的含有Fe2(SO4)3杂质的CuSO4溶液中加入适量的黑色粉末X,充分搅拌后过滤,将滤液用右图所示装置电解,其中某电极增重a g,另一电极上产生标准状况下的气体V mL。下列说法正确的是( )
(2011·北京海淀区期末练习)已知在pH为4~5的溶液中,Cu2+几乎不水解,而Fe3+几乎完全水解。某学生拟用电解CuSO4溶液的方法测定铜的相对原子质量。该同学向pH=3.8的含有Fe2(SO4)3杂质的CuSO4溶液中加入适量的黑色粉末X,充分搅拌后过滤,将滤液用右图所示装置电解,其中某电极增重a g,另一电极上产生标准状况下的气体V mL。下列说法正确的是( )
A.黑色粉末X是铁粉
B.铜电极连接电源正极
C.石墨电极上发生的反应是
4OH--4e-===O2↑+2H2O
D.铜的相对原子质量的计算式是
解析:利用Fe3+的水解,除去CuSO4溶液中Fe3+方法是向其中加入黑色的CuO,与Fe3+水解产生的H+反应,促进Fe3+水解,使Fe3+转化为Fe(OH)3沉淀而除去,A错误;电解时,石墨作阳极,电极反应式:
4OH--4e-===2H2O+O2↑,C正确;
铜作阴极,电极反应式为:2Cu2++4e-===2Cu,B错误;
据两极上转移电子的量相等可知:
×2=×4,
解得:M(Cu)=。
答案:C
15.按下图装置实验,若x轴表示流入阴极的电子的物质的量,则y轴可表示( )
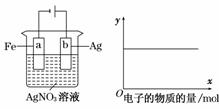
①c(Ag+) ②c(AgNO3) ③a棒的质量 ④b棒的质量
⑤溶液的pH
A.①③ B.③④
C.①②④ D.①②⑤
解析:该电解池,随着电解的进行,c(Ag+)不变,c(AgNO3)不变,溶液的pH不变。因为阳极反应式为Ag-e-===Ag+,阴极反应式为Ag++e-===Ag。
答案:D
14.(2011·安徽师大附中模拟)利用生活中常见的材料可以进行很多科学实验,甚至制作出一些有实际应用价值的装置来,如图就是一个用废旧材料制作的可用于驱动玩具的电池的示意图。该电池工作时,有关说法正确的是( )
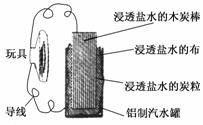
A.铝罐将逐渐被腐蚀
B.炭粒和炭棒上发生的反应为O2+4e-===2O2-
C.炭棒应与玩具电机的负极相连
D.该电池工作一段时间后炭棒和炭粒的质量会减轻
解析:该电池的反应原理是4Al+3O2===2Al2O3,所以Al作电源负极,与玩具电极的负极相连,逐渐被腐蚀,A项正确,C、D项错误;B项中正确的反应式为O2+2H2O+4e-===4OH-。
答案:A
13.[双选题]银锌蓄电池是一种高能电池,它的两极材料分别为锌和氧化银,电解质溶液为KOH溶液,放电时它的正、负两极的电极反应式如下:
Ag2O+H2O+2e-===2Ag+2OH-,
Zn+2OH--2e-===Zn(OH)2。
下列判断正确的是( )
A.锌为负极,氧化银为正极
B.锌为正极,氧化银为负极
C.原电池工作时,负极区溶液pH增大
D.原电池反应的化学方程式为Zn+Ag2O+H2O===Zn(OH)2+2Ag
解析:从电极反应式看,锌失电子被氧化,所以锌为负极;Ag2O得电子被还原,所以是正极。由电极反应式相加可得,总化学方程式:Zn+Ag2O+H2O===Zn(OH)2+2Ag。从负极电极反应式分析,OH-被消耗,所以负极区溶液的pH应减小,选A、D。
答案:AD
12.(2011·杭州师大附中月考)1 L某溶液中含有的离子如下表:
|
离子 |
Cu2+ |
Al3+ |
NO |
Cl- |
|
物质的量浓度(mol/L) |
1 |
1 |
a |
1 |
用惰性电极电解该溶液,当电路中有3 mol e-通过时(忽略电解时溶液体积的变化及电极产物可能存在的溶解现象),下列说法正确的是( )
A.电解后溶液的pH=0 B.a=3
C.阳极生成1.5 mol Cl2 D.阴极析出的金属是铜与铝
解析:根据电子守恒可知,该反应过程中涉及的反应有:阳极:2Cl--2e-===Cl2↑(产生氯气的体积,标准状况下为0.5 mol),4OH--4e-===2H2O+O2↑;阴极:Cu2++2e-===Cu,2H++2e-===H2↑。从电子守恒的角度知,电解后溶液的pH=0,A项正确;从电荷守恒的角度可知,a=4,B不正确。
答案:A
11.[双选题]将金属A和金属B分别放入稀H2SO4中有氢气生成。若将金属A和金属B相连后投入稀H2SO4中发现A被腐蚀,B未被腐蚀,关于A、B的叙述正确的是( )
A.金属活动性A>B
B.还原性B>A
C.在后者装置中金属A发生还原反应,金属B发生氧化反应
D.金属B的表面有明显的气泡产生
解析:金属A和金属B相连后投入稀H2SO4中,构成了原电池,负极腐蚀而损耗,正极被保护,即金属A为负极,金属B为正极。
答案:AD
10.(2011·山东省实验中学高二检测)氯碱工业的基本原理就是电解饱和食盐水。下列关于实验室电解饱和食盐水的说法中正确的是( )
A.可以选用石墨棒作为阴、阳极材料,但阳极材料也可以用铁棒
B.用湿润的淀粉KI试纸靠近阴极区域,试纸变蓝
C.电解过程中,在阳极区域溶液中滴加品红,品红褪色
D.实验结束后,将溶液搅拌,然后用pH试纸检验,溶液呈中性
解析:电解时阳极不能选用活泼的金属材料,故A错;电解饱和食盐水时阴极产物为还原产物H2,故B错;电解时阳极产物为氧化产物氯气,故C正确;电解饱和食盐水除生成氢气和氯气外,在阴极还有NaOH产生,所以电解实验结束后,搅拌溶液,溶液中有NaOH,显碱性,故D错。
答案:C
9.(2011·长春高二检测)用铜片、银片设计成如图所示的原电池。以下有关该原电池的叙述正确的是( )
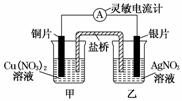
A.电子通过盐桥从乙池流向甲池
B.铜导线替换盐桥,原电池仍继续工作
C.开始时,银片上发生的反应是:Ag-e-===Ag+
D.将铜片浸入AgNO3溶液中发生的化学反应与该原电池总反应相同
解析:根据原电池工作原理,电子由负极(Cu)沿导线传递给正极(Ag),电解质溶液中阴离子沿盐桥从乙流向甲;正极(Ag):2Ag++2e-===2Ag,负极(Cu):Cu-2e-===Cu2+,总反应:Cu+2Ag+===Cu2++2Ag,与将Cu片浸入AgNO3溶液中发生的化学反应相同。故选D。
答案:D
8.如下图所示是某太空空间站能量转化系统的局部示意图,其中燃料电池采用KOH溶液为电解液,下列有关说法中正确的是( )
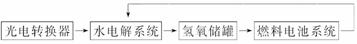
向日面时 背日面时
A.该能量转化系统工作时,需不断补充H2O
B.该转化系统的能量本质上来源于太阳能
C.水电解系统中的阴极反应:
O2+2H2O+4e-===4OH-
D.燃料电池放电时的负极反应:H2-2e-===2H+
解析:水电解时阴极为2H++2e-===H2↑,C项错误;燃料电池放电时负极为H2+2OH--2e-===2H2O,故D项错误;A项中H2O可以循环利用,错误;B项正确。
答案:B
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com