
2£®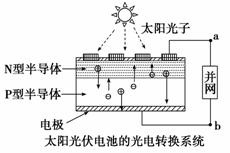 ŹĄ²©»įÖŠ¹ś¹Ż”¢Ö÷Ģā¹ŻµČ½ØÖžĖłŹ¹ÓĆµÄ¹ā·üµē³Ų£¬×ܹ¦ĀŹ“ļ4Õ×Ķߣ¬ŹĒĄś½ģŹĄ²©»įÖ®×ī”£ĻĀĮŠÓŠ¹ŲŠšŹöÕżČ·µÄŹĒ
ŹĄ²©»įÖŠ¹ś¹Ż”¢Ö÷Ģā¹ŻµČ½ØÖžĖłŹ¹ÓĆµÄ¹ā·üµē³Ų£¬×ܹ¦ĀŹ“ļ4Õ×Ķߣ¬ŹĒĄś½ģŹĄ²©»įÖ®×ī”£ĻĀĮŠÓŠ¹ŲŠšŹöÕżČ·µÄŹĒ
A£®¹ā·üµē³ŲŹĒ½«Ģ«ŃōÄÜ×Ŗ±äĪŖµēÄÜ
B£®¹ā·üµē³ŲŹĒ½«»ÆѧÄÜ×Ŗ±äĪŖµēÄÜ
C£®µēĮ÷“ÓaĮ÷Ļņb
D£®Ķ¼ÖŠNŠĶ°ėµ¼ĢåĪŖÕż¼«£¬PŠĶ°ėµ¼ĢåĪŖøŗ¼«
Ņ»”¢Ń”ŌńĢā
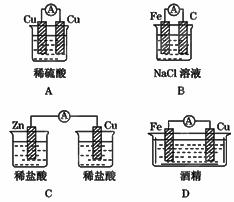
1£®ČēĶ¼ĖłŹ¾µÄ×°ÖĆÄܹ»×é³ÉŌµē ³Ų²śÉśµēĮ÷µÄŹĒ
³Ų²śÉśµēĮ÷µÄŹĒ
5. ŹµŃéŹŅ°“ĻĀĶ¼ĖłŹ¾×°ÖĆÖĘČ”CO2£¬²¢¼ģŃéCO2µÄŠŌÖŹ£®ŹŌ»Ų“šŅŌĻĀĪŹĢā£ŗ
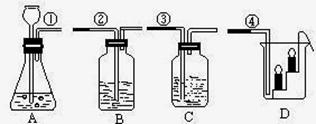
£Ø1£©ŹµŃéæŖŹ¼ Ē°£¬ĻČÓ¦¼ģ²é×°ÖĆAµÄ_____
Ē°£¬ĻČÓ¦¼ģ²é×°ÖĆAµÄ_____ _________”£
_________ӣ
£Ø2£©ÓĆ×°ÖĆAĄ“ÖĘČ”CO2£¬ĖłÓƵÄŅ©Ę·ŹĒ____________ŗĶ____________£ØŠ“»ÆѧŹ½£©
£Ø3£©ČōŅŖÓĆ×°ÖĆB¼ų¶ØCO2£¬ŌŚBÖŠÓ¦Ź¢·ÅµÄŹŌ¼ĮĆū³ĘŹĒ____________£¬µ±½«±ź¢ŁŗĶ¢ŚµÄµ¼¹ÜæŚĮ¬½ÓŹ±£¬B֊擵½µÄŹµŃéĻÖĻóŹĒ______________________”£
£Ø4£©ČōŅŖÓĆ×°ÖĆCÖ¤Ć÷CO2ÄÜÓėĖ®·“Ӧɜ³ÉĢ¼Ėį£¬CÖŠ³żÓŠÉŁĮæĖ®Ķā£¬Ó¦¼ÓČėµÄŹŌ¼ĮŹĒ_______________ __£¬µ±½«±ź¢ŁŗĶ¢ŪµÄµ¼¹ÜæŚĮ¬½ÓŹ±£¬C֊擵½µÄŹµŃéĻÖĻóŹĒ________________”£
__£¬µ±½«±ź¢ŁŗĶ¢ŪµÄµ¼¹ÜæŚĮ¬½ÓŹ±£¬C֊擵½µÄŹµŃéĻÖĻóŹĒ________________”£
£Ø5£©ÉÕ±DÖŠ·ÅÓŠČ¼×ÅµÄĄÆÖņČēĶ¼ĖłŹ¾£¬µ±½«±ź¢ŁŗĶ¢ÜµÄµ¼¹ÜæŚĮ¬½ÓŹ±£¬D֊擵½µÄŹµŃéĻÖĻóŹĒ____________________________________”£
£Ø6£©¼ĢŠųÉč¼Ę²¢½ųŠŠÓŠ¹ŲCO 2ŠŌÖŹµÄĢ½¾æŹµŃ飬Čē×°ÖĆE”¢F”£ĻČŌŚ×°ÖĆEÖŠ·ÅŅ»øöÓĆæÕĘų³äÕĶµÄĘųĒņ£¬ÖĘČ”Ņ»Ę涞Ńõ»ÆĢ¼µ¹ČėE×°ÖĆŗ󣬳öĻÖČēF×°ÖĆŹµŃéĻÖĻó”£Ēė»Ų“š£ŗøĆŹµŃéµÄÄæµÄŹĒĢ½¾æ____________________________________”£
2ŠŌÖŹµÄĢ½¾æŹµŃ飬Čē×°ÖĆE”¢F”£ĻČŌŚ×°ÖĆEÖŠ·ÅŅ»øöÓĆæÕĘų³äÕĶµÄĘųĒņ£¬ÖĘČ”Ņ»Ę涞Ńõ»ÆĢ¼µ¹ČėE×°ÖĆŗ󣬳öĻÖČēF×°ÖĆŹµŃéĻÖĻó”£Ēė»Ų“š£ŗøĆŹµŃéµÄÄæµÄŹĒĢ½¾æ____________________________________”£
4£®»ģŗĻĘųĢåæÉÄÜŗ¬ÓŠH2”¢N2”¢CO2”¢CO ĘäÖŠµÄŅ»ÖÖ»ņ¼øÖÖ£¬½«ĘäĶعżĻĀĶ¼µÄŹµŃé×°ÖĆ¼ģŃéĘä³É·Ö”£

ČōA “¦ĻÖĻóĪŖ³ĪĒåŹÆ»ŅĖ®±ä»ė×Ē£¬B “¦ŗŚÉ«·ŪÄ©±äŗģ£¬C “¦³ĪĒåŹÆ»ŅĖ®²»±ä”£ĶʶĻ“ĖĘųĢåÖŠŅ»¶Øŗ¬ÓŠ”””””””””” £¬Ņ»¶Ø²»ŗ¬ÓŠ”””””””””” £¬æÉÄÜŗ¬ÓŠ”””””””” ”£
3.ĻÖÓŠAŗĶB×é³ÉµÄŗŚÉ«»ģŗĻĪļ£¬°“ŅŌĻĀĶ¼Ź¾½ųŠŠŹµŃé£ŗ
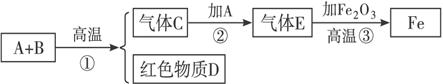
øł¾ŻŹµŃéĶʶĻ£¬²¢Š“³öĻĀĮŠĪļÖŹµÄ»ÆѧŹ½£ŗ
A._____________ £¬B. _____________ £¬C. _____________ £¬
D. _____________ £¬E. _____________ ”£
2.ĶعżŹµŃéĢ½¾æµÄ·½·Ø¶ŌĪ“ÖŖŹĀĪļ½ųŠŠĢ½Ė÷ŹĒ»ÆѧѧĻ°µÄŅ»ÖÖÖŲŅŖ·½Ź½”£ĪŖĮĖĢ½¾æ¶žŃõ»ÆĢ¼ÄÜÓėĖ®·¢Éś·“Ӧɜ³É¾ßÓŠĖįŠŌµÄĪļÖŹ£¬A”¢BĮ½Ķ¬Ń§·Ö±šÉč¼ĘĮĖĢ½¾æŹµŃéµÄ·½°ø”£AĶ¬Ń§µÄŹµŃé·½°øŹĒ½«¶žŃõ»ÆĢ¼ĶØČė×ĻÉ«ŹÆČļŹŌŅŗÖŠ£¬¹Ū²ģČÜŅŗµÄŃÕÉ«±ä»Æ£¬Čē ĻĀĶ¼¼×ĖłŹ¾”£BĶ¬Ń§µÄŹµŃé·½°øŹĒČ”ĖĶäÓĆŹÆČļŹŌŅŗČ¾³É×ĻÉ«µÄøÉŌļµÄŠ”»Ø£¬°“ĻĀĶ¼ŅŅ½ųŠŠŹµŃ飬¹Ū²ģŠ”»ØŃÕÉ«±ä»Æ£Ø×ĻÉ«ŹÆČļŹŌŅŗÓöĖįČÜŅŗ±äŗģÉ«£©”£
ĻĀĶ¼¼×ĖłŹ¾”£BĶ¬Ń§µÄŹµŃé·½°øŹĒČ”ĖĶäÓĆŹÆČļŹŌŅŗČ¾³É×ĻÉ«µÄøÉŌļµÄŠ”»Ø£¬°“ĻĀĶ¼ŅŅ½ųŠŠŹµŃ飬¹Ū²ģŠ”»ØŃÕÉ«±ä»Æ£Ø×ĻÉ«ŹÆČļŹŌŅŗÓöĖįČÜŅŗ±äŗģÉ«£©”£
ĒėÄć¶ŌA”¢BĮ½Ķ¬Ń§µÄŹµŃéĢ½¾æ·½°ø½ųŠŠĘĄ¼Ū£ŗ
£Ø1£©ÄÄøöĶ¬Ń§µÄ·½°øŗĻĄķ”£_________________________
£Ø2£©·½°øŗĻĄķµÄĄķÓÉŹĒ”£_______ ____________________
____________________

1.ČēĻĀĶ¼ĖłŹ¾ŹĒŹµŃéŹŅÖĘČ”²¢ŃéÖ¤¶žŃõ»ÆĢ¼ŠŌÖŹµÄŹµŃ飬Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
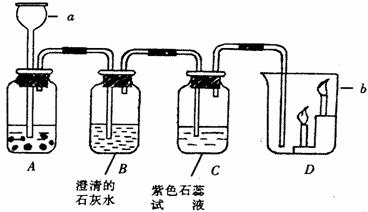
¢ŁŠ“³öŅĒĘ÷Ćū³Ę
a”””””””””””””””” £»b”””””””””””””””” £»
¢Ś¹ćæŚĘæAÖŠµÄŅ©Ę·£¬ŹōŅŗĢ¬µÄŹĒ””””””  ””””£¬æéד¹ĢĢåŹĒ””””””””””
””””£¬æéד¹ĢĢåŹĒ””””””””””
¢ŪŹµŃéÖŠ£¬¹Ū²ģµ½¹ćæŚĘæBÖŠ·¢ÉśµÄĻÖĻóŹĒ”””””””””””””””””” £¬Ęä·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ””””””””””””””””””””””””””””””””””””””””””””
¢ÜŌŚ¹ćæŚĘæCÖŠ¹Ū²ģµ½µÄĻÖĻóŹĒ”””””””””””””””””””””””””” £¬ĘäŌŅņŹĒ£ØÓĆ»Æѧ·½³ĢŹ½±ķŹ¾£©”””””””””””””””””””””””””””””””””””””” [Ą“Ō“:]
¢ŻDÖŠµÄĄÆÖņ£¬”””””””””” ĻČĻØĆš£¬ĖµĆ÷¶žŃõ»ÆĢ¼¾ßÓŠ”””””””””””””” ”¢””””
”””””””””””””” ĒŅ”””””””””””””” µÄŠŌÖŹ”£
Čż”¢·ĒŃ”ŌńĢā
16£®(9·Ö)æĘѧ¼Ņ·¢ĻÖ£ŗ¾ßÓŠ2”¢8”¢20”¢28”¢50”¢82”¢114”¢126µČŹżÄæµÄÖŹ×Ó»ņÖŠ×ÓµÄŌ×ÓŗĖ¾ßÓŠĢŲ±šµÄĪČ ¶ØŠŌ£¬²¢½«ÕāŠ©Å¼Źż³ĘĪŖ”°»ĆŹż”±£¬¶ų¾ßÓŠĖ«»ĆŹżµÄHe”¢Ni”¢Sn”¢PbµČÓČĪŖĪČ¶Ø”£øł¾Ż“ĖŠÅĻ¢»Ų“šĻĀĮŠĪŹĢā£ŗ
¶ØŠŌ£¬²¢½«ÕāŠ©Å¼Źż³ĘĪŖ”°»ĆŹż”±£¬¶ų¾ßÓŠĖ«»ĆŹżµÄHe”¢Ni”¢Sn”¢PbµČÓČĪŖĪČ¶Ø”£øł¾Ż“ĖŠÅĻ¢»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)Š“³öĒ°ČżÖÖÖŹ×ÓŹżĪŖ”°»ĆŹż”±Ź±µÄŌŖĖŲŌ×ӵĽį¹¹Ź¾ŅāĶ¼£¬²¢±źĆ÷ŌŖĖŲ·ūŗÅ£ŗ________________________________________________________________________
________________________________________________________________________ӣ
(2)ŅŃÖŖŃõÓŠČżÖÖĶ¬Ī»ĖŲO”¢O”¢O£¬øł¾ŻÉĻŹö”°»ĆŹż”±¹ęĀÉ£¬ŃõµÄĶ¬Ī»ĖŲÖŠŌ×ÓŗĖ×īĪČ¶ØµÄŹĒ________”£
(3)øł¾ŻĻÖÓŠŌŖĖŲÖÜĘŚĀÉĶĘĖć£¬RĪ»ÓŚŌŖĖŲÖÜĘŚ±ķµÄµŚ________ÖÜĘŚ________×壬ŗĖĪČ¶ØŠŌR________R(Ģī”°>”±”¢”°<”±»ņ”°£½”±)”£
½āĪö£ŗ(1)øł¾ŻĢāÄæŠÅĻ¢æÉÖŖ£¬2”¢8”¢20”¢28”¢50”¢82”¢114”¢126ÕāŃłµÄŹż³ĘĪŖ”°»ĆŹż”±£¬ĖłŅŌĒ°ČżÖÖÖŹ×ÓŹżĪŖ”°»ĆŹż”±µÄŌŖĖŲŹĒŗ¤”¢Ńõ”¢øĘ£»(2)ŅņĪŖ¾ßÓŠĖ«”°»ĆŹż”±(¼“ÖŹ×ÓŹżŗĶÖŠ×ÓŹż¶¼ŹĒ”°»ĆŹż”±)µÄŌ×ÓŗĖ×īĪČ¶Ø£¬øł¾ŻŃõµÄĶ¬Ī»ĖŲŌ×ÓÖŖ£¬Ö»ÓŠOµÄÖŹ×ÓŹżŗĶÖŠ×ÓŹż¶¼µČÓŚ»ĆŹż8£¬ĖłŅŌ×īĪČ¶Ø£»(3)øł¾ŻŌŖĖŲRµÄÖŹ×ÓŹżÖŖøĆŌŖĖŲĪ»ÓŚÖÜĘŚ±ķµÄµŚ7ÖÜĘŚ¢ōA×壬ÓÉÓŚRŌ×ÓµÄÖŹ×ÓŹżŹĒ”°»ĆŹż”±£¬ÖŠ×ÓŹżĪŖ298£114£½184£¬±¾Ģā°µŹ¾184ŹĒ»ĆŹż£¬ĖłŅŌRŌ×ÓĻą¶ŌĪČ¶Ø”£
15£®X”¢Y”¢Z”¢W¾łĪŖ¶ĢÖÜĘŚŌŖĖŲ£¬ĖüĆĒŌŚÖÜĘŚ±ķÖŠµÄĪ»ÖĆČēĻĀĶ¼ĖłŹ¾”£ČōYŌ×ÓµÄ×īĶā²ćµē×ÓŹżŹĒÄŚ²ćµē×ÓŹżµÄ3±¶£¬ĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ(””)

A£®Ō×Ó°ė¾¶£ŗW>Z>Y>X
B£®×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļµÄĖįŠŌ£ŗZ>W>X
C£®ĻąµČĪļÖŹµÄĮæÅØ¶ČµÄĘųĢ¬Ēā»ÆĪļČÜŅŗµÄpH£ŗX>Z>W
D£®ĖÄÖÖŌŖĖŲµÄµ„ÖŹÖŠ£¬Zµ„ÖŹµÄČŪ·Šµć×īøß
½āĪö£ŗŃ”CD”£ŅņYŌ×ÓµÄ×īĶā²ćµē×ÓŹżŹĒÄŚ²ćµē×ÓŹżµÄ3±¶£¬æÉÖŖYĪŖOŌŖĖŲ£¬ÓÉ“ĖæÉĶĘ³öXĪŖNŌŖĖŲ£¬ZĪŖSŌŖĖŲ£¬WĪŖClŌŖĖŲ”£Ō×Ó°ė¾¶X>Y”¢Z>W£¬Ń”ĻīA“ķĪó£»×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļµÄĖįŠŌÖŠW¶ŌÓ¦µÄĖį×īĒæ£¬Ń”ĻīB“ķĪó£»°±Ė®ĻŌ¼īŠŌ£¬ĒāĮņĖįĪŖČõĖį£¬ŃĪĖįĪŖĒæĖį£¬Ņņ“ĖŃ”ĻīCÕżČ·£»ĖÄÖÖŌŖĖŲµÄµ„ÖŹÖŠ£¬Sµ„ÖŹµÄČŪ·Šµć×īøߣ¬Ń”ĻīDÕżČ·”£
14£®ĻÖÓŠĮ½ÖÖ¶ĢÖÜĘŚÖ÷×åŌŖĖŲX”¢Y£¬ĒŅŌŚ³£ĪĀĻĀXµÄµ„ÖŹ³ŹĘųĢ¬£¬YµÄµ„ÖŹ³Ź¹ĢĢ¬”£ŌņĻĀĮŠĶʶĻ²»ÕżČ·µÄŹĒ(””)
A£®ČōX”¢YĪ»ÓŚ ¢ńA×壬ŌņX”¢YæÉÄÜÓėŃõŌŖĖŲŠĪ³ÉŌ×ÓøöŹż±ČĪŖ1”Ć1»ņ2”Ć1µÄ»ÆŗĻĪļ
¢ńA×壬ŌņX”¢YæÉÄÜÓėŃõŌŖĖŲŠĪ³ÉŌ×ÓøöŹż±ČĪŖ1”Ć1»ņ2”Ć1µÄ»ÆŗĻĪļ
B£®ČōX”¢YĪ»ÓŚµŚ3ÖÜĘŚ£¬ŌņX”¢YŠĪ³ÉµÄ»ÆŗĻĪļæÉÄÜŹĒĄė×Ó»ÆŗĻĪļ»ņ¹²¼Ū»ÆŗĻĪļ
C£®ČōĘųĢ¬HnXµÄ·ŠµćøßÓŚHnY£¬ŌņX”¢YÖ»ÄÜĪ»ÓŚÖÜĘŚ±ķ¢öA×å
D£®ČōX”¢YĪ»ÓŚÖÜĘŚ±ķµÄĶ¬Ņ»ÖÜĘŚ£¬Ōņ×īøß¼Ūŗ¬ŃõĖįµÄĖįŠŌæÉÄÜŹĒHnXOm<HaYOb
½āĪö£ŗŃ”CD”£·ūŗĻAŃ”ĻīµÄĪļÖŹĪŖH2O”¢H2O2ŗĶNa2O”¢Na2O2£»·ūŗĻBŃ”ĻīµÄĪļÖŹĪŖMgCl2”¢SiCl4£»·ūŗĻDŃ”ĻīµÄXµÄŌ×ӱȊņŹżYµÄŌ×ÓŠņŹż“󣬷Ē½šŹō»īĘĆŠŌX>Y£¬¹ŹĖįŠŌHnXOm>HaYOb”£·ūŗĻCŃ”ĻīµÄX”¢YĪŖSŗĶO»ņPŗĶN”£
¹ś¼ŹŃ§Š£ÓÅŃ” - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com