
12.(10分)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压。高铁电池的总反应为:
3Zn+2K2FeO4+8H2O放电充电3Zn(OH)2+2Fe(OH)3+4KOH。
请回答下列问题:
(1)高铁电池的负极材料是____________。
(2)放电时,正极发生________(填“氧化”或“还原”)反应;已知负极反应为Zn-2e-+2OH-===Zn(OH)2,则正极反应为__________________________________________________。
(3)放电时,________(填“正”或“负”)极附近溶液的碱性增强。
二、非选择题[
11.(8分)如下图,三个烧杯中盛足量的Cu Cl2溶液。
Cl2溶液。
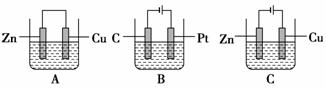
(1)A中Zn是________极,发生________反应(填“氧化”或“还原”,下同),电极反应式________________________________;
Cu是________极,发生________反应,电极反应式_______________________________________,总反应方程式__________________________________________________。
(2)B中C是________极,发生________反应,电极反应式____________________,Pt是________极,发生________反应,电极反应式_______________________________________;
总反应方程式__________________________________________________。
(3)C中Zn是________极,发生________反应,电极反应式________________,Cu是________极,发生________反应,电极反应式______________________________________________;
反应过程中c(Cu2+)____________(填“变大”、“变小”或“不变”)。
10.氢氧燃料电池以KOH溶液为电解质溶液,下列有关该电池的叙述不正确的是
A.正极反应式为:O2+2H2O+4e-===4OH-
B.工作一段时间后,电解液中KOH的物质的量浓度不变
C.该燃料电池的总反应方程式为:2H2+O2===2H2O
D.用该电池电解CuCl2溶液,产生2.24 L Cl2(标准状况)时,有0.2 mol电子转移
选择题答题栏
9.分析如图所示的四个原电池装置,其中结论正确的是
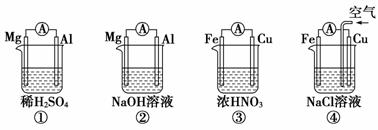
A.①②中Mg作负极,③④中Fe作负极
B.②中Mg作正极,电极反应式为:6H 2O+6e-===6OH-+3H2↑
2O+6e-===6OH-+3H2↑
C.③中Fe作负极,电极反应式为Fe-2e-===Fe2+
D.④中Cu作正极,电极反应式为2H++2e-===H2↑
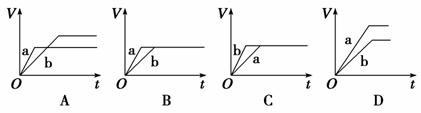
8.等质量的两份锌粉a、b分别加 入过量的稀硫酸,同时向a中加少量的CuSO4溶液,如各图中产生H2的体积V(L)与时间t(min)的关系,正确的是
入过量的稀硫酸,同时向a中加少量的CuSO4溶液,如各图中产生H2的体积V(L)与时间t(min)的关系,正确的是
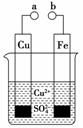
7.某小组为研究电化学原理,设计如图装置,下列叙述不正确的是
A.a和b不连接时,铁片上会有金属铜析出
B.a和b用导线连接时,铜片上发生的反应为:Cu2++2e-===Cu
C.无论a和b是否连接,铁片均会溶解,溶液均从蓝色逐渐变成浅绿色
D.a和b分别连接直流电源正、负极,电压足够大时,Cu2+向铜电极移动[
6.芬兰籍华人科学家张霞昌研制的“超薄型软电池”获2009年中国科技创业大赛最高奖,被称之为“软电池”的纸质电池总反应为Zn+2MnO2+H2O===ZnO+2MnOOH。下列说法正确的是
A.该电池中Zn作负极,发生还原反应
B.该电池反应中MnO2起催化作用
C.该电池工作时电流由Zn经导线流向MnO2
 D.该电池正极反应式为:2MnO2+2e-+2H2O===2MnOOH+2OH-
D.该电池正极反应式为:2MnO2+2e-+2H2O===2MnOOH+2OH-
5.如图是Zn和Cu组成的原电池示意图,某小组做完该实验后,在读书卡片上作了如下记录,其中合理的是
|
卡片:No.10
Date:2012-3-11,实验记录:①导线中电流方向:锌→铜。 ②铜极上有气泡产生。 ③锌片变薄。,实验结论:④Zn为正极,Cu为负极。 ⑤铜比锌活泼。 ⑥H+向铜片移动。 |
A.①②③ B.④⑤⑥
C.③④⑤ D.②③⑥
4.某原电池的电池反应为:Fe+2Fe3+===3Fe2+,与此电池反应不符的原电池是
A.铜片、铁片、FeCl3溶液组成的原电池
B.石墨、铁片、Fe(NO3)3溶液组成的原电池
C.铁片、锌片、Fe2(SO4)3溶液组成的原电池
D.铜片、铁片、Fe(NO3)3溶液组成的原电池
3.下图为一原电池装置,下列叙述中正确的是
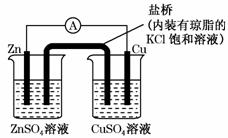 A.铜离子在铜片表面被还原
A.铜离子在铜片表面被还原
B.盐桥中的K+移向ZnSO4溶液
C.电流从锌片经导线流向铜片
D.铜是阳极,铜片上有气泡产生
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com