
18. X、Y、Z、W代表短周期的四种元素,有关它们的部分结构及性质信息如下表所示。
|
元素 |
部分结构信息 |
部分性质信息 |
|
X |
X的单质由双原子分子构成,分子中有14个电子 |
X有多种氧化物,如XO、XO2、X2O4等;通常情况下XO2与X2O4共存 |
|
Y |
Y原子的次外层电子数等于最外层电子数的一半 |
Y能形成多种气态氢化物 |
|
Z |
Z原子的最外层电子数多于4 |
Z元素的最高正化合价与最低负化合价代数和等于6 |
|
W |
W原子的最外层电子数等于2n-3(n为原子核外电子层数) |
化学反应中W原子易失去最外层电子形成Wn+ |
请按要求回答下列问题(注意不能用字母X、Y、Z、W作答):
(1)X的气态氢化物分子的电子式是______________,Z元素在周期表中的位置是________。
(2)X、Y、Z三元素的最高价氧化物对应水化物的酸性由强到弱的顺序是
(3)实验室用X的氢化物的水溶液制取W的氢氧化物的方法是(用离子方程式表示)_____________________________________
(4)25 ℃、101 kPa时,32 g Y的最低价气态氢化物完全燃烧生成稳定的氧化物时放出1 780.6 kJ的热量,写出该反应的热化学方程式:_______________________________________
二、非选择题
16、安全气囊是行车安全的重要设施。当车辆发生碰撞的瞬间,安全装置通电点火使其中的粉末分解释放出大量的氮气形成气囊,从而保护司机及乘客。为研究安全气囊工作的化学原理,取安全装置中的粉末进行研究。经实验分析,确定该粉末是一种混合物且只含Na、Fe、N、O四种元素。
(1)氧元素在元素周期表中的位置是________,Na原子结构示意图为________,混合物所含四种元素中三种主族元素的离子半径从大到小的顺序是________(用离子符号表示)。
(2)水溶性实验表明,安全气囊中固体粉末部分溶解。不溶物为一种红棕色固体,可溶于盐酸。已知该不溶物能发生铝热反应,写出反应的化学方程式________________________
(3)氮的最高价氧化物对应的水化物与其氢化物反应生成一种盐,该盐晶体中含有的化学键类型是________________
17如图是从元素周期表中截取的一个片断,其中X、Y、Z、W均属于短周期元素。请回答下列问题。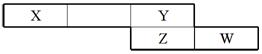
(1)若X的单质为空气中的主要成分之一,则W的原子结构示意图为________。
(2)若Y、W、Z的最高价氧化物对应的水化物依次为一元酸、二元酸、三元酸,这三种酸的正盐的含氧酸根离子中,有两种的电子数相等,这两种离子的离子符号是______、________ 。
。
(3)若Na与Y和Z的单质分别反应可以生成摩尔质量相同的两种化合物,其中Na与Y形成的化合物的电子式为________,所含化学键的类型为________________。
(4)Y元素在元素周期表中处于第_______________________纵行(写出所有可能纵行数)。
15、同周期的元素X、Y、Z形成的最高价氧化物对应水化物的酸性HXO4>H2YO4>H3ZO4,则下列说法正确的是( )
A、非金属性X< Y < Z B、阴离子还原性:X—< Y2—<Z3—
C、氢化物的稳定性:HX< H2Y < ZH3 D、原子序数:X< Y < Z
14.下列说法正确的是( )
A、同位素之间的性质几乎相同
B、H2、D+、T之间互为同位素
C、最外层有2个电子的元素一定是第ⅡA族的金属
D、同周期的元素,原子序数越大,其非金属性越强
12.(2012·浙江)X、Y、Z是原子序数依次增大的短周期元素,3种元素的原子核外电子数之和与 Ca2+的核外电子数相等,X
Ca2+的核外电子数相等,X 、Z分别得到一个电子后均形成稀有气体原子的稳定电子层结构。下列说法正确的是( )
、Z分别得到一个电子后均形成稀有气体原子的稳定电子层结构。下列说法正确的是( )
A.原子半径:Z > Y > X
B.Z与X形成化合物的沸点高于Z的同族元素与X形成化合物的沸点
C.CaY2与水发生氧化还原反应时,CaY2只作氧化剂
D.CaX2、CaY2和CaZ2等3种化合物中,阳离子与阴离子个数比均为1:2
13 X、Y、Z、W为四种短周期元素,它们在周期表中位于连续的四个主族,如图所示。Z元素原子核外K层与M层电子数相等。下列说法中正确的是( )。
|
|
|
X |
Y |
|
Z |
W |
|
|
A.Y元素最高价氧化物对应的水化物化学式为H3YO4
B.Y最简单气态氢化物的水溶液显弱碱性
C.原子半径由小到大的顺序为:X< Z< Y< W
D.X、Z两种元素的氧化物中所含化学键类型相同
11.(2012·四川)已知W、X、Y、Z为短周期元素,W、Z同主族,X、Y、Z同周期,W的气态氢化物的稳定性大于Z的气态氢化物的稳定性,X、Y为金属元素,X的阳离子的氧化性小于Y的阳离子的氧化性。下列说法正确的是( )
A.X、Y、Z、W的原子半径依次减小 B.W与X形成的化合物中只含离子键
C.W的气态氢化物的沸点一定高于Z的气态氢化物的沸点
D.若W与Y的原子序数相差5,则二者形成化合物的化学式一定为Y2W3
10. X、Y、Z、W为周期表中前20号元素中的四种,原子序数依次增大,W、Y为金属元素,X原子的最外层电子数是次外层电子数的3倍,Y、Z位于同周期,Z单质是一种良好的半导体。W能与冷水剧烈反应,Y、Z原子的最外层电子数之和与X、W原子的最外层电子数之和相等。下列说法正确的是( )
A.原子半径:W> Y> Z>X
B.气态氢 化物的稳定性:X<Z
化物的稳定性:X<Z
C.最高价氧化物对应水化物的碱性:Y>W D.Y、Z的氧化物都有酸性和碱性
9. X、Y、Z、W是原子序数依次增大的短周期主族元素,X、Z在周期表中的相对位置如表所示。已知X元素最低负化合价的绝对值与其原子最外层电子数相等,Y是地壳中含量最多的金属元素。下列说法错误的是( )
|
X |
|
|
|
|
|
Z |
A.X和氢组成的化合物分子中可能含有极性共价键和非极性共价键
B.工业上用电解Y和W组成的化合物来制备Y
C.Z、W两元素的气态氢化物中,W的气态氢化物更稳定
D.X、Y、Z、W元素最高价氧化物对应的水化 物中酸性最强的是HWO4
物中酸性最强的是HWO4
8.下列说法中,正确的是( )
A.前三周期元素形成的单质中,常温下呈气态的有5种
B.ⅦA族元素的原子随核电荷数 的增加,得电子能力逐渐减弱
的增加,得电子能力逐渐减弱
C.主族元素的阳离子与同周期稀有气体元素的原子具有相同的核外电子排布
D.所有主族元素的正化合价数,等于它 的族序数
的族序数
7. X、Y、Z、W为四种短周期元素,它们在周期表中位于连续的四个主族,如图所示。Z元素原子核外K层与M层电子数相等。下列说法中正确的是( )
|
|
|
X |
Y |
|
Z |
W |
|
|
A.Y元素最高价氧化物对应水化物的化学式为H3YO4
B.Y的最简单气态氢化物的水溶液显弱碱性
C.原子半径由小到大的顺序为X<Z<Y<W
D.X、Z两种元素的氧化物中所含化学键类型 相同
相同
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com