
8、 白磷
黑磷,黑磷比白磷稳定,结构与石墨相似,下列叙述正确的(
白磷
黑磷,黑磷比白磷稳定,结构与石墨相似,下列叙述正确的(  )
)
A.黑磷与白磷互为同分异构体
 B.黑磷和白磷均不能导电
B.黑磷和白磷均不能导电
C.白磷转化为黑磷 是氧化还原反应
D.白磷转化为黑磷是放热反应
是氧化还原反应
D.白磷转化为黑磷是放热反应
7、下列叙述正确的是( )
 A.海水中含有钾元素,只需经过物理变化就可得到钾单质
A.海水中含有钾元素,只需经过物理变化就可得到钾单质
B.石油分馏、煤的气化、海水制镁等过程都包含化学变化
C.在海水中加入硝酸银,滤掉生成的沉淀,可达到海水淡化的目的
D.铝热法还原铁的反应中,放出的热量能使铁熔化
6、下列鉴别方法可行的是( )
A.用氨水鉴 别Al3+、Mg2+和A
别Al3+、Mg2+和A g+ B.用溴水鉴别苯和正己烷
g+ B.用溴水鉴别苯和正己烷
C.用新制Cu(OH)2悬浊液鉴别乙醇、乙醛、乙酸 D.用Ca(OH)2溶液鉴别CO32-和HCO3-
5、下列化学用语正确的是( )
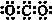 A.CO2的电子式:
B.乙烯的结构简式:CH2CH2
A.CO2的电子式:
B.乙烯的结构简式:CH2CH2
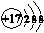
 C.CH4分子
C.CH4分子 的比例模型:
的比例模型:  D. Cl原子的结构示意图:
D. Cl原子的结构示意图:
4、某溶液中含有下列六种离子:①HCO3- ②SO32- ③Na+ ④CO32- ⑤NH4+ ⑥NO3-,向其中加入
一定量Na2O2后,溶液中离子浓度基本保持不变的是( )
A.只有⑥ B.④⑥ C.③④⑥ D.①②⑤
3、在通常条件下,下列各组物质的性质排列正确的是( )
A.熔点:CO2>KCl>SiO2 B. 沸点:乙烷>正丁烷>异丁烷
C.热稳定性:HF>NH3>H2O D.酸性:H2SO4>H2CO3>H2SiO3
2、下列设备工作时,将化学能转化为热能的是( )

一、选择题
1、化学已渗透到人类生活的各个方面。下列说法不正确的是( )
A.阿司匹林具有解热镇痛的作用
B.红宝石、珍珠、玛瑙、水晶、钻石等装饰品的主要成分都是硅酸盐
C.“84”消毒液的有效成分为NaClO,能杀菌消毒
D.绚丽缤纷的烟花中添加了含钾、钠、钙、铜等金属元素的化合物
12.(2012·大纲全国,29)(16分)氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质。为了提纯氯化钾,先将样品溶于适量水中,充分搅拌后过滤,再将滤液按下图所示步骤进行操作。
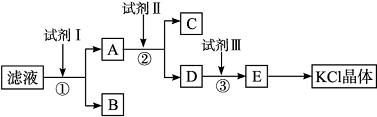
回答下列问题:
(1)起始滤液的pH__________7(填“大于”“小于”或“等于”),其原因是______________;
(2)试剂Ⅰ的化学式为__________,①中发生反应的离子方程式为__________________;
(3)试剂Ⅱ的化学式为_________,②中加入试剂Ⅱ的目的是___
 __________________;
__________________;
(4)试剂Ⅲ的名称是__________,③中发生反应的离子方程式为___________________;
(5)某同学称取提纯的产品0. 775 9 g,溶解后定容在100
mL容量瓶中,每次取25.00 mL溶液,用0.100 0 mol·L-1的硝酸银标准溶液滴定,三次滴定消耗标准溶液的平均体积为25.62 mL,该产品的纯度为__________。(列式并计算结果)
775 9 g,溶解后定容在100
mL容量瓶中,每次取25.00 mL溶液,用0.100 0 mol·L-1的硝酸银标准溶液滴定,三次滴定消耗标准溶液的平均体积为25.62 mL,该产品的纯度为__________。(列式并计算结果)
11.(10分)以下是25 ℃时几种难溶电解质的溶解度:
|
难溶电解质 |
Mg(OH)2 |
Cu(OH)2 |
Fe(OH)2 |
Fe(OH)3 |
|
溶解度/g |
9×10-4 |
1.7×10-6 |
1.5×10-4 |
3.0×10-9 |
在无机化合物的提纯中,常利用难溶电解质的溶解平衡原理除去某些杂质离子。例如:
①为了除去氯化铵中的杂质Fe3+,先将混合物溶于水,再加入一定量的试剂反应,过滤结晶即可;
②为了除去氯化镁晶体中的杂质Fe3+,先将混合物溶于水,加入足量的氢氧化镁,充分反应,过滤结晶即可;
③为了除去硫酸铜晶体中的杂质Fe2+,先将混合物溶于水,加入一定量的H2O2,将Fe2+氧化成Fe3+,调节溶液的pH=4,过滤结晶即可。
请回答下列问题:
(1)上述三种除杂方案都能够达到很好的效果,Fe3+、Fe2+都被转化为________(填化学式)而除去。
(2)①中加入的试剂应该选择________为宜,其原因是_____ ______________________。
______________________。
(3)②中除去Fe3+所发生的总反应的离子方程式为________________________________。
(4)下列与方案③相关的叙述中,正确的是____(填字母)。
A.H2O2是绿色氧化剂,在氧化过程中不引进杂质,不产生污染
B.将Fe2+氧化为Fe3+的主要原因是Fe(OH)2沉淀比Fe(OH)3沉淀较难过滤
C.调节溶液pH=4可选择的试剂是氢氧化铜或碱式碳酸铜
D.Cu2+可以大量存在于pH=4的溶液中
E.在pH>4的溶液中Fe3+一定不能大量存在
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com