
18.(12分)某铝合金中含有铝、镁、铜、硅。为了测定该合金中铝的含量,现设计了如下实验:
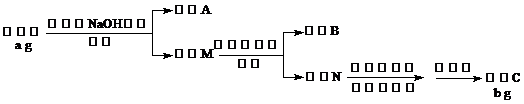
已知:Si+2NaOH=Na2 Si O3+H2↑,H2Si O3是不溶于水的弱酸。
(1)固体A的成分是:________,溶液M中的阴离子有:____________________
(2)步骤③中生成沉淀的离子方程式为:_____________________________________
(3)步骤④中,用到的仪器有三脚架、酒精灯以及
(4)该样品中铝的质量分数是:_______________________________(用a、b表示)。
(5)下列因操作不当,会使测定结果偏大的是___________
A.第①步中加入NaOH溶液不足 B.第②步中加入盐酸不足时
C.第④步中的沉淀未用蒸馏水洗涤 D.第④步对沉淀灼烧不充分
17.(11分)某无色透明溶液,可能含有下列离子:Mg2+、Al3+、Fe2+、Ba2+、SO42-、Cl-、AlO2-,现取该溶液实验如下:
|
实验步骤 |
实验现象 |
|
①取少量该溶液,加几滴石蕊试剂 |
溶液变成红色 |
|
②取少量原溶液,加BaCl2溶液 |
有白色沉淀生成 |
|
③取②中上层清液,加AgNO3溶液 |
有白色沉淀生成,且不溶于稀HNO3 |
|
④取少量原溶液,加NaOH溶液至过量 |
有白色沉淀生成,当NaOH过量时有部分沉淀溶解 |
(1)该溶液中一定存在的离子有______________,一定不存在的离子有________________;可能存在的离子有_______________。
(2)写出下列反应的离子方程式:
操作②: 。
操作④中沉淀溶解: 。
16.(10分) 在实验室中
(1)烧碱溶液因保存不慎会变质,涉及的离子方程式为:________________________。
(2)向NaCO3逐滴加入稀盐酸,现象是:_____________ _____________。
涉及的离子方程式为:_______________________ ; _______________________。
(3)向分液漏斗中先加入10mL溴水,再加入4mLCCI4溶液,振荡静置,现象是:________________
_________________________________________。
二、填空题
15.(8分)焊接铜件时常用的焊药为氯化铵,其作用是消除焊接处的氧化铜。其反应式为:
NH4C1 + CuO→ Cu + CuC12 + N2↑+ H2O
(1)配平,并用双线桥法标出电子转移情况。
(2)该反应中,氧化剂和还原剂的物质的量之比为:___________。
(3)若反应中电子转移了0.3mol,则产生的气体在标准状况下的体积为_______L。
14.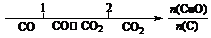 研究反应物的化学计量数与产物之间的关系时,使用类似数轴的方法可以收到的直观形象的效果。下列表达不正确的是( )
研究反应物的化学计量数与产物之间的关系时,使用类似数轴的方法可以收到的直观形象的效果。下列表达不正确的是( )
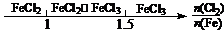 A.密闭容器中CuO和C高温反应的气体产物:
A.密闭容器中CuO和C高温反应的气体产物:
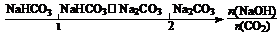 B.Fe在Cl2中的燃烧产物:
B.Fe在Cl2中的燃烧产物:
C.NaOH溶液中通入一定量的CO2的产物:
D.AlCl3溶液中滴加NaOH溶液后体系中铝元素的存在形式:
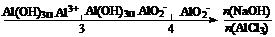
第II卷 非选择题(共48分)
13.下列关于物质的检验说法不正确的是( )
A.向某物质中滴加盐酸后,有能使澄清石灰水变浑浊的无色无味气体产生,证明含CO32-
B.将某化合物进行焰色实验,透过蓝色钴玻璃观察,焰色为紫色,证明含K+
C.待检液逐滴加入NaOH溶液,有白色胶状沉淀产生后来沉淀逐渐消失,则原溶液中可能含有Al3+
D.待检液中先加入KSCN溶液,无明显现象,再加入氯水溶液显血红色,则待检液中一定含有Fe2+
12.下列各组物质的无色溶液,不用其它试剂即可鉴别的是( )
①KOH、Na2SO4、AlCl3 ②NaAlO2、HCl、H2SO4 ③Na2CO3、NaHCO3、H2SO4 ④AgNO3、Na2CO3、KCl
A.①②④ B.②③ C.①② D.①③
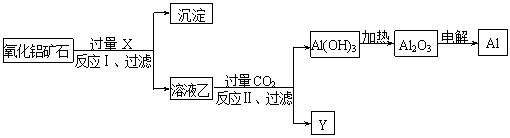
11. 工业上用某种氧化铝矿石(含Fe2O3杂质)为原料冶炼铝的工艺流程如下:
工业上用某种氧化铝矿石(含Fe2O3杂质)为原料冶炼铝的工艺流程如下:




 对上述流程中的判断正确的是( )
对上述流程中的判断正确的是( )
 A.试剂X可以为氨水,沉淀中含有铁的化合物
A.试剂X可以为氨水,沉淀中含有铁的化合物
B.CO2可以用H2SO4溶液或稀盐酸代替
 C.反应II中的反应为:CO2 + AlO2-+ 2H2O=Al(OH)3↓+ HCO3-
C.反应II中的反应为:CO2 + AlO2-+ 2H2O=Al(OH)3↓+ HCO3-
 D.工业上还可采用Fe还原Al2O3的方法制Al,成本更低
D.工业上还可采用Fe还原Al2O3的方法制Al,成本更低
10.某CuSO4、Fe2(SO4)3、H2SO4的混合溶液100 mL,
已知溶液中阳离子的浓度相同(不考虑水电离的少量H+),
且SO42-的物质的量浓度为6 mol/L,则此溶液最多溶解铁粉的质量为( )
A.11.2 g B.16.8 g C.19.6 g D.22.4 g
9.在右图点滴板上有四组溶液间反应的小实验,其对应的离子方程式书写正确的是( )
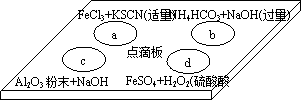 A.a反应:Fe3+ + 3SCN-=Fe(SCN)3↓
A.a反应:Fe3+ + 3SCN-=Fe(SCN)3↓
B.b反应:HCO3-+ OH-=CO32-+ H2O
C.c反应:Al2O3+2OH-=2AlO2-+H2O
D.d反应:Fe2++ 2H++ H2O2=Fe3++ 2H2O
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com