
(2) 当X=0.5时,平衡后右室SO2的体积分数为a;X=1时,平衡后右室SO2的体积分数为b,则a和b的关系是 ▲ ;
A、a>b B、a=b C、a<b D、无法确定
(3) 若平衡时隔板在中央,则X= ▲ , 左室吸收的热量为Q1 kJ,右室放出的热量为Q2 kJ,则Q1、Q2间满足的关系是 ▲ ;

左室:2SO3(g) 2SO2(g) + O2(g) 右室:2SO2(g) + O2(g) 2SO3(g) △H=-197kJ/mol
回答下列问题:
(1) 能说明反应达到平衡的是 ▲ ;
A、隔板不再移动 B、左右二室SO2和O2物质的量之比相等
C、左右两边SO2的物质的量相等 D、左右二边SO3的体积分数相等
17.(10分)如下图所示,在一定温度下,在一个容积为
请填写下列空白:
(1)简述B形成的酸雨对环境的危害 ▲ ; ▲ (至少二点);
(2)配制F的溶液时要加 ▲ ;
(3)写出B+H→F+G的离子方程式 ▲ ;
(4)若A分解产生的B、C、D、E的质量比为16∶20∶63∶40,则A的化学式为 ▲ 。
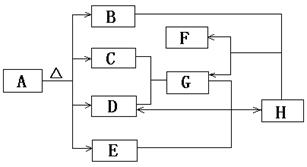
16.(8分)下图是无机物A~H在一定条件下的转化关系(部分反应中参加反应的水未列出)。其中,A是一种带有结晶水的正盐,B是形成酸雨的主要物质,G是一种常见的二元强酸,E是一种红棕色粉末。

(3)B装置中试剂的化学式是 ▲ , C装置中试剂的名称是 ▲ 。
(4)能证明乙同学观点正确的实验现象是 ▲ 。
(5) 若丙同学的观点正确,用上述装置通过B、C中质量的增加来定量测定沉淀的组成,请你说说该装置主要存在的缺点 ▲ (至少二点)
15.某研究性学习小组将一定浓度Na2CO3溶液滴入CuSO4溶液中得到蓝色沉淀。
甲同学认为沉淀可能是CuCO3;
乙同学认为沉淀可能是Cu(OH)2;
丙同学认为沉淀可能是CuCO3和Cu(OH)2的混合物。(查阅资料知:CuCO3和Cu(OH)2均不带结晶水)
Ⅰ.(1)乙同学的观点,你认为其原理是 ▲ ;
(2)在探究沉淀成分前,须将沉淀从溶液中过滤、洗涤、低温干燥,检验沉淀是否洗涤干净的方法是 ▲ 。
Ⅱ.请用下图所示装置,选择必要的试剂,定性探究生成物的成分。
14.一定质量的Fe2O3、ZnO、CuO的固体混合粉末,在加热条件下用足量CO还原,得到金属混合物4.
A.50 mL B.100 mL C.200 mL D.缺少数据,无法计算
B.将标准状况下1.
2Fe2++4Br-+3Cl2 =2Fe3++6Cl-+2Br2
C.向NaOH溶液中滴加同浓度的少量Ca(HCO3)2溶液:
Ca2++ HCO3- +OH- =CaCO3↓+H2O
D.向Ba(OH)2溶液中逐滴加入NH4HSO4溶液至刚好沉淀完全:
Ba2++2OH-+H++ SO42- + NH4+ =BaSO4↓+ NH3?H2O +H2O
13.下列离子方程式的书写正确的是
A.实验室用浓盐酸与MnO2反应制Cl2:
MnO2 +4HCl(浓) Cl2↑+Mn2+ +2Cl-+2H2O
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com