
2、下列液体中,PH >7的是 ( )
A. 食醋 B.人体血液 C.人体胃液 D.柠檬汁
1、下列变化属于化学变化的是 ( )
A.工业制氧气 B.大米酿酒 C.干冰升华 D.电灯通电发光
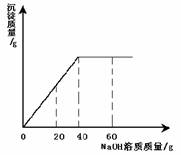
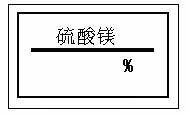
18.(4分) 某同学在实验室发现一瓶标签残缺(如图1所示)的溶液。为了测定此溶液的溶质质量分数,他取出25g该溶液,向其中逐滴加入溶质质量分数为10%的NaOH溶液。反应过程中生成沉淀的质量与所用NaOH溶液质量的关系如图2所示(有关化学方程式为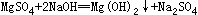 )。请列式计算此溶液的溶质质量分数。
)。请列式计算此溶液的溶质质量分数。
17.(2分) 水果中含有柠檬酸,可促进消化,柠檬酸的化学式为C6H8O7。
求:⑴柠檬酸的相对分子量;
⑵柠檬酸中碳原子的质量分数为。
16.(6分)氢氧化铜固体受热分解能得到两种产物,其中一种为固定。某学生小组为确定这种固体产物是什么,进行了如下探究活动。
假设:生成的固体产物可能是氧化亚铜(Cu2O),也可能是__________、________。
资料:Cu2O是红色固体。
实验:将新制的氢氧化铜粉末放入试管中,使其在加热条件下分解

(如右图),观察到蓝色粉末逐渐变成黑色。
推测结论:该黑色粉末是氧化铜,推测的依据是________________________________;
_____________________________________________。
验证结论:设计一个简单的实验,证明这种推断是正确的。(填写下列实验报告)
|
实验步骤 |
可能出现的实验现象 |
实验结论 |
|
|
|
黑色粉末是氧化铜 |
15.(5分)我国青海湖地区素有“夏天晒盐,冬天捞碱”之说,其中捞出的碱主要是碳酸钠和少量氯化钠的混合物。小王同学以捞出的碱作为样品,并用以下一套装置对样品进行分析,根据量筒中收集到的液体的体积(相当于二氧化碳的体积)来计算样品中碳酸钠的含量。(已知:HCl+NaHCO3===NaCl+CO2↑+H2O;CO2在饱和NaHCO3溶液中溶解度很小)
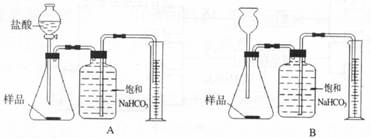
(1)在A和B 两套装置中,哪一套装置更合理________(选填“A”或“B”)。
(2)准确读取量筒内液体体积的方法是_______________________。
(3)锥形瓶中原有的空气对实验结果是否有明显影响? ______(填“有”或“没有”)。
(4)若实验中用的盐酸是浓盐酸,则测得的样品中碳酸钠的含量与实际值相比会________(填“偏大”或“偏小”或“不变”)。
14.(4分)“有其他物质生成”是判断物质发生化学变化的依据,但在实际化学反应中,常常根据反应伴随的现象来确定化学反应是否发生。请你根据对化学变化的理解,仿照实例填写下表:(表中内容不得重复)
|
实验内容 |
主要实验现象 |
|
例如:铜丝与硝酸银溶液反应 |
铜丝表面覆着一层银白色的物质,溶液变成蓝色 |
|
⑴ |
|
|
⑵ |
|
13.(3分)某工厂用硫化铜(CuS)制硫酸铜,现有两个方案:
方案一:让CuS在硫杆菌(催化剂)的作用下跟空气中的O2反应生成CuSO4。
方案二: ,
,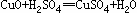 。
。
从保护环境的角度看,⑴上述万案_____________较为合理。
⑵理由是:________________________、__________________。
12.(4分) 经过一年的学习,我们初步认识了身边的一些简单物质,如木炭、氧气、氢气、一氧化碳、二氧化碳、甲烷、水等。
(1)请从上述物质中选出适当的物质写出两个燃烧的化学方程式:
①_______________________________;②______________________________。
(2)二氧化碳能与上述物质中的一种反应,生成一种酸,试写出反应的化学方程式:
___________________________________________。
(3)含硫煤的燃烧排放到空气中的有毒气体主要是SO2,它遇到雨水后形成酸雨降落到地面上会带来很大危害。这减少环境污染,对工厂排放的废气可用烧碱溶液吸收处理,其化学方程式为_______________________________。
11.(2分)请从H(+1)、C(+4)、O(-2)、K(+1)中选择合适的元素,按下列要求写出化学式(各写一例):
⑴非金属氧化物_______;⑵由三种元素组成的酸_________;
⑶可溶于水的碱_________;⑷由三种元素组成的盐__________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com