
⒒(2分)从氢气、盐酸、干冰、氢氧化钠,选出适当的物质,按要求填空(用化学式表示)。
⑴可用于人工降雨的物质是 ;
⑵可用作理想的高能燃料的气体是 ;
⑶可用于除铁锈的酸是 ;
⑷化工生产中的一种重要原料,其水溶液能使酚酞试液变红的是 ;
12.(4分)请从Mg、O2、稀HCl、NaOH溶液、KClO3五种物质中,选择适当的物质作反应物,写出符合下列要求的化学方程式并注明条件。
⑴化合反应: ;
⑵分解反应: ;
⑶置换反应: ;
⑷复分解反应: 。
⒈下列俗语与物质的化学性质无关的是 ( )
A.真金不怕火炼 B.百炼方能成钢
C.纸里包不住火 D.玉不琢不成器
⒉下列有关实验基本操作或有关实验现象的描述错误的是 ( )
A.点燃可燃性气体前,先检验气体的纯度
B.用胶头滴管吸取液体后,将滴管平放或倒置,以免试液污染
C.铁丝在氧气中燃烧时,火星四射,有黑色固体生成
D.酒精灯打翻着火,用湿抹布扑盖
⒊空气污染给人类和大自然带来严重危害。下列措施中,对减少空气污染没有直接作用的是 ( )
A.减少煤、石油等化石燃料的使用
B.工厂的废气经净化处理后排放
C.提倡使用无磷洗衣粉
D.更多地利用太阳能、风能等清洁能源
⒋下列对物质世界的认识中,不正确的是 ( )
A.为提高粮食产量,应大量使用化肥和农药
B.废旧金属的回收利用是保护金属资源的有效途径
C.海洋中蕴藏着丰富的资源
D.通过化学反应,人类不仅可以获得所需物质,还可以获得能量
⒌钛和钛的合金被认为是21世纪的重要材料,它们具有很多优良的性能,如熔点高、密度小、可塑性好、易于加工,钛合金与人体有很好的“相容性”。根据它们的主要性能,下列用途不切合实际的是 ( )
A.用来做保险丝 B.用于制造航天飞机
C.用来制造人造骨 D.用于制造船舶
⒍右图中M、N分别表示二种固体物质(不含结晶水)的溶解度曲线,试根据图中曲线判断下列说法正确的是 ( )
A.图中A点表示M、N二种物质在t1℃时均达到饱和
B.M、N二种饱和溶液,当温度从t1降至t2时,一定析出相同质量的晶体
C.同处A点的相同质量的M、N二种溶液,当温度从t1降至t2后,剩余溶液的质量分数相等
D.0℃时,M、N具有相同的溶解度
⒎生活中可能遇到的下列混合物,能按“溶解-过滤-蒸发”的步骤加以分离的是 ( )
A.食盐(NaCl)和细砂 B.水和酒精
C.石灰石(CaCO3)和生石灰(CaO) D.蔗糖和味精
⒏下列哪种试剂最适合用来除去NaCl溶液中混有的少量Na2CO3 ( )
A.NaOH溶液 B.H2SO4溶液 C.HCl溶液 D.Ca(OH)2溶液
⒐现有铁、铜、银三种金属,限用一种试剂一次性就可验证他们的金属活动性强弱,则该试剂是 ( )
A.ZnSO4溶液 B.CuSO4溶液 C.KNO3溶液 D.稀硫酸
10.人体口腔内唾液的pH通常约为7,在进食过程的最初10分钟,酸性逐渐增强,之后酸性逐渐减弱,至40分钟趋于正常。与上述事实最接近的图象是 ( )

第二卷
12.(6分)镁是重要的金属材料,广泛应用于合金、火箭和飞机制造业,世界上大部分镁是从海水中提取的。威海是一座滨海城市,海岸线长达1000 km,海水资源丰富。某校学习小组的同学对家乡附近海水中镁元素的含量进行测定。称取海水100kg,然后再加入足量的氢氧化钠溶液,过滤、干燥、称量后得到沉淀质量见下表。(重复实验三次)。
|
|
第一次实验 |
第二次实验 |
第三次实验 |
|
所取海水质量/kg |
100 |
100 |
100 |
|
生成沉淀质量/kg |
0.28 |
0.29 |
0.30 |
试计算海水中镁元素的质量分数。
(假定海水中镁元素全部以氯化镁的形式存在,不考虑沉淀中杂质的干扰)。
11.(18分)实验与探究:追踪氧气和二氧化碳的足迹
据科学家估计,全世界生物的呼吸和燃烧所消耗的氧气,每秒钟可达l万吨左右。但
是我们生活中并没有明显感到环境中氧气不足,这是什么原因呢?
事实上,把地球作为一个整体,一些化学变化在消耗氧气的同时,另一些变化又在产
生氧气,并且维持一种动态平衡。科学研究发现,地球的再生氧气主要来源于地球臭氧层
电场电流对水分子的电解和绿色植物的光合作用。
下图是自然界中碳、氧循环的主要途径:
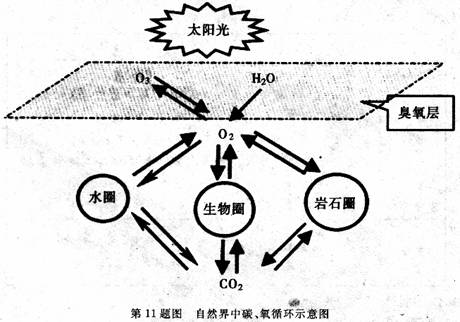
根据上图,运用你学过的有关知识,回答下列问题。
(1)试写出自然界中两种不同类型的消耗氧气的途径
①
②
(2)请你设计一个实验,模拟(1)中消耗氧气的一种变化。将实验方案写在下面。
(3)在实验中,为了获得少量氧气,可以根据物质的性质,选择含有 元素的物质,通过控制反应条件来实现。请你用化学方程式表示在实验室里产生氧气的一个变化
(4)另外有一种实验室产生少量氧气的简易方法:用过氧化氢的水溶液做反应物,反应条件是常温和二氧化锰做催化剂,反应的化学方程式为
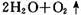 。
。
若根据该反应制取氧气,则发生装置跟制取 气体的发生装置相同,需要的仪器有 。与实验室用氯酸钾制取氧气比较,该反应的优点是
。现用溶质质量分数为30%、密度为1.1g/ml的过氧化氢溶液制取氧气。实验中,发现二氧化锰与过氧化氢溶液混合后,装置中产生氧气的速度太快,你认为可能的原因有
。
(5)从图中可以看出,碳和氧的循环过程是紧密联系在一起的一种自然过程。事实上,地球上的碳只有0.9%参与循环,99.1%都固定在岩石圈中,然而,人类对能源和资源的过度开发利用,已经影响到自然界中碳、氧循环。
①在上面叙述中所说中碳、氧循环是指 的循环。
A.碳和氧的单质 B.氧气和二氧化碳 C.碳元素和氧元素
②根据自然界中碳、氧循环示意图,试分别写出一个自然界中产生和消耗二氧化碳气体的化学方程式。
产生二氧化碳的反应
消耗二氧化碳的反应 。
③为了遏制大气中二氧化碳不断增加的趋势,维护好自然界中碳、氧循环,请你提出两点措施 ;
。
10.(4分)下表是不同溶质质量分数的硫酸溶液和氨水与其相应密度的对照表
|
溶液中溶质的质量分数 |
4% |
2% |
16% |
24% |
28 |
|
硫酸溶液的密度(20℃)/g·ml |
1.02 |
1.08 |
1.11 |
1.17 |
1.20 |
|
氨水的密度(20~C)/g·ml |
0.98 |
0.95 |
0.94 |
0.91 |
0.90 |
请你仔细分析上表中的数据,回答下列问题:
(1)从上表可以看出,硫酸溶液的密度大于水的密度,而氨水的密度则小于水的密
度。除此以外,你还能够总结出溶液密度与其溶质的质量分数的变化规律是
。
(2)试从物质定量组成(氨水的溶质为NH3)的角度分析,为什么这两种溶液密度与其溶质的质量分数之间存在这种变化规律?
。
8. (8分)人类对原子结构的认识是逐渐深入的。右图是不同时期科学家提出的原子结构模型。
(8分)人类对原子结构的认识是逐渐深入的。右图是不同时期科学家提出的原子结构模型。
1808年,英国科学家道尔顿提出了原子论。他认为物质都是由原子直接构成的;原子是一个实心球体,不可再分割;同一类原子性质相同;不同的原子是以简单的整数比相结合。
1897年,英国科学家汤姆生发现原子中存在电子。1904年汤姆生提出了一个被称为
“西瓜式”结构的原子结构模型,电子就像“西瓜子”一样镶嵌在带正电的“西瓜瓤”中。
电子的发现使人们认识到原子是由更小的粒子构成的。
1911年英国科学家卢瑟福做了一个实验:用一束质量比电子大很多的带正电的高速运
动的。粒子轰击金箔,结果是大多数。粒子能穿过金箔且不改变原来的前进方向,但也有
一小部分改变了原来的方向,还有极少数的。粒子被反弹了回来。据此他提出了带核的原
子结构模型:原子是由原子核和核外电子构成。
……
根据以上材料,请回答:
(1)道尔顿提出了原子论,汤姆生发现了原子中的电子,这在当时是件很了不起的事,但由于受到那时科学技术水平的限制,他们的理论中存在一些缺陷甚至错误,按照目前初中阶段你学的原子结构的理论,你认为道尔顿的原子论存在的缺陷是
;
汤姆生原子结构模型的缺陷是
。
(2)根据卢瑟福的实验所产生的现象,不能够获得的结论是 。
A.原子核体积很小 B.原子核质量较大 C.原子核带有正电 D.核外电子带有负电
(3)通过人类认识原子结构的历史,你对科学的发展有哪些感想?
。
7.(8分)某化工厂用石灰石制取碳酸钙,流程图为:

(1)请写出上述方案中所依据反应的化学方程式。
① ___________________________________________________________________ ;
② ___________________________________________________________________ ;
③ ___________________________________________________________________ 。
(2)请你仍然用石灰石为原料,其他试剂任选,设计另外一种制备碳酸钙的实验方
案,将你的实验方案用流程图的形式表示出来:

6.(5分)为了获得人类生活和发展需要的各种物质,并更好地利用这些物质,化学家们通常按照某种标准,将众多的化学物质进行分类。根据你学过的初中化学知识,按照物质的组成,将空气、硫酸铵、石墨、铜、氢气、纯碱、氧化镁、烧碱、乙醇、食盐水进行分类。(要求用框图的形式表示,层次分明,分类精细。
5.下面是小李同学用连线方式对某一主题知识进行归纳的情况,其中有错误的是
A .物质与微观构成 B .能量的获取与物质的变化
|
|
||||
|
|
第二卷
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com