
6.下列实验操作错误的是 ( )

5.英国伦敦大学的科学家发明一种“智能玻璃”--不用空调,冬暖夏凉。秘密在于其表面的超薄层物质二氧化矾(VO2)和钨(W)的混合物。VO2中V的化合价为 ( )
A.+l B.+2 C.+3 D.+4
4.美国火星探测车在火星大气层中检测到COS气体。该物质属于 ( )
A.单质 B.酸 C.化合物 D.氧化物
3.图示材料属于合金的是 ( )

2.下图为自来水生产的一种流程示意图,其中属于化学变化的步骤是 ( )

1.央视经济频道“CCTV倾国倾城”中国名城全球网络推介活动正在进行中,2006年获“联合国最佳人居奖”的扬州已升至第三名。下列做法对保护古城环境无益的是 ( )
A.大力提倡市民使用小汽车,提高生活质量
B.加强工业用水系统的环保改造,提高水的重复利用率
C.研究开发“绿色化学”工艺,使原料完全转化为产物
D.推广垃圾的分类存放、回放、处理
0. 48g比正确值0.44g偏大的原因(假设操作均正确)
。
(4)数据计算
根据正确值0.44g可求得粗产品中Na2CO3的质量分数为 %。
NaOH含量的测定:
该小组同学又另取10.0g粗产品,逐滴加入20%的盐酸至恰好完全反应时,消耗盐酸的质量为36. 5g.放出CO2 0.44g(不考虑二氧化碳气体的溶解)。求原粗产品中NaOH的质量分数。(写出计算过程)
30.(18分)课外化学兴趣小组的同学利用某化工厂的废碱液(主要成分为Na2CO3,还含有少量NaCl,其它杂质不计)和石灰乳为原料制备烧碱,并对所得的烧碱粗产品的成分进行分析和测定。
[粗产品制备]
(1)将废碱液加热蒸发浓缩,形成较浓的溶液,冷却后与石灰乳混合,发生反应的化学方程式为 。
(2)将反应后的混合物过滤,得到的滤液进行蒸发结晶,制得NaOH粗产品。
[粗产品成分分析]
(1)取适量粗产品溶于水,滴加Ba(NO3)2溶液出现白色浑浊,发生反应的化学方程式为 ,该粗产品中一定不含有 ,理由是 。
(2)该小组同学通过对粗产品成分的实验分析,确定该粗产品中含有三种物质。
[粗产品含量测定]
Na2CO3含量的测定:
(1)该兴趣小组的同学设计了下图所示的实验装置。取10.0g粗产品,进行实验。
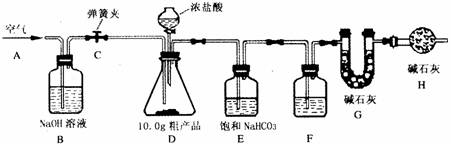
[说明]碱石灰是CaO与NaOH 的固体混合物。E装置中的饱和NaHCO3溶液是为了除去二氧化碳气体中的氯化氢,发生的反应为NaHCO3 十HC1 = NaCl十CO2↑十H2O。
(2)操作步骤
①连接好装置,检查气密性;
②打开弹簧夹C,在A处缓缓通入一段时间空气;
③称量G的质量;
④关闭弹簧夹C,慢慢滴加浓盐酸至过量,直至D中无气泡冒出;
⑤打开弹簧夹C,再次缓缓通入一段时间空气;
⑥再次称量G的质量,得前后两次质量差为0. 48g。
(3)问题探究
F中的试剂应为 ,B装置的作用是 ,
H装置的作用是 。
若没有H装置,则测定的Na2CO3的质量分数会 (填“偏大”、“偏小”、“不变”)。
事实上10.0g粗产品只能产生0.44g CO2。请你仔细分析上述实验,解释实验值
29.(5分)小兵同学在化学实验室发现一瓶盛有无色溶液的试剂瓶,其标签严重破损(如下图所示)。老师告诉他,这瓶试剂可能是硫酸、硫酸钠、硫酸镁溶液中的一种。
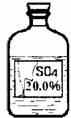
小兵同学通过查阅资料得知,常温下这三种物质的溶解度如下表:
|
物质 |
H2SO4 |
Na2SO4 |
MgSO4 |
|
溶解度/g |
与水任意比互溶 |
19.0 |
39.0 |
小兵同学根据上述信息.分析认为此溶液一定不是 溶液。为确定其成分,该同学对此溶液进行如下实验探究:
[提出假设]该溶液可能是 。
[实验验证]
|
实
验 步
骤 |
实
验 现
象 |
实
验 结
论 |
|
|
|
|
28.(7分)现有一包白色粉末,可能由NaCl、Na2SO4、Na2CO3、CuSO4中的一种或几种组成。现做如下实验:①取少量粉末,加水溶解得无色溶液;②另取少量粉末,滴加稀盐酸,无明显现象。请回答:
(1)由实验①可确定原粉末中一定没有 ;
由实验②可确定原粉末中一定没有 。
(2)根据上述实验现象,得出原粉末中可能含有的物质是 、 。
(3)为进一步确定原粉末的组成,另取少量粉末按下图所示进行实验:[在AgNO3、Ba(NO3)2、BaCl2溶液中选择两种作为A、B试剂,且A、B的阳离子不同]

原粉末的成分是 ;试剂A为 ;试剂B为 。
(若有多种情况,只需写出其中一种)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com