
2、空气中含量最多的气体是 ( )
A、氧气 B、二氧化碳 C、氮气 D、稀有气体
1、下列变化中,属于物理变化的是( )
A、木板做成书桌 B、汽油燃烧 C、食物腐败 D、火药爆炸
36.5 40

解得:ω=0.1825=18.25%
现请你参与探究并完成相关问题。(可能用到的相对分子质量:H2SO4-98 BaSO4-233 BaCl2-208 )
(1)[实验1]中发生反应的化学方程式为 。
(2)小忻测出原混合酸中H2SO4的质量分数为 (保留三位有效数字)。
(3)小燕计算出混合酸中HCl的质量分数会 (填“偏高”、“偏低”或“无影响”),理由是
(如“无影响”,本空不作答)。
28.(7分)
小忻和小燕合作测定盐酸、硫酸组成的混合酸中溶质的质量分数,设计并进行了如下两个探究实验:
[实验1] 取20g该混合酸并分成4等份,然后分别加入一定量未知质量分数的BaCl2溶液,实验记录如下:
|
|
第1份 |
第2份 |
第3份 |
第4份 |
|
加入BaCl2溶液的质量 / g |
15 |
20 |
25 |
30 |
|
反应得到的沉淀的质量 / g |
1.398 |
1.864 |
2.330 |
2.330 |
[实验2] 将[实验1]中的第4份反应液过滤,再向滤液中逐滴加入10%的NaOH溶液,通过pH测定仪打印出加入NaOH溶液的质量与烧杯中溶液pH的关系如下图:

[数据处理]
小忻依据[实验1]沉淀的质量计算出混合酸中H2SO4的质量分数。
小燕依据[实验2]求混合酸中HCl的质量分数,过程如下:
[解]设混合酸中HCl的质量分数为ω。
HCl + NaOH = NaCl + H2O
27.(3分)
为使食品在较长的时间内保持色、香、味和口感,人们常在食品或食品包装中加入化学防腐剂。请根据下图回答:

苯甲酸中C、H、O元素的原子个数比为 ,C、H元素的质量比为 ,
相对分子质量为 。
26.(7分)
小亮对课本中C和CuO反应的产物进行了进一步的探究,以下是他进行实验的部分流程(装置气密性良好):
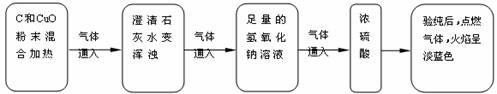
(1)通过以上实验,可知产物中有 气体。
(2)取出反应后的固体,观察呈红色。
[查阅资料] ① C也能将CuO还原为红色固体Cu2O(氧化亚铜)
② Cu2O + H2SO4(稀)= Cu + CuSO4 + H2O
[猜 想] (a)红色固体只是Cu
(b)
(c)红色固体是Cu和Cu2O的混合物
[实验探究]
|
实验操作 |
实验现象 |
实验结论 |
|
取7.2g红色固体,置于烧杯中,向其中加入足量稀硫酸,充分搅拌,静置。 |
若无现象。 |
证明红色固体 。 |
|
若
。 |
证明红色固体肯定含有 ,可能含有 。 |
|
|
取上述反应液过滤、洗涤、干燥和称量,得固体 6.8g 。 |
|
确认红色固体是
。 |
25.(10分)
下图A与B是实验室常用来制取气体的装置,根据所学知识回答以下问题:

(1) 装置B表示正在用高锰酸钾制取氧气,其中还缺少的仪器是________(填名称),并将其画到相应的位置,图中棉花的作用是_________________________,该反应的化学方程式为__________________________________________,实验完毕,为防止水倒吸,应_______
___________________________________。
(2)若想制取CO2,应选择图中的_______(填“A”或“B”)装置;若想用装置A来制取干燥的氧气,使用的药品是MnO2和___________(填化学式),并在瓶________(填“①”或“②”)中加浓硫酸。
(3)A装置气密性的检验:先关闭分液漏斗活塞,__________________________,用热毛巾捂住瓶①,若__________________________,则该装置漏气。
24.(4分)
盐的水溶液是否都呈中性呢?小松在老师的合作下进行了探究。
[实验试剂]10%的Na2CO3溶液、10%的Na2SO4溶液、10%的CuSO4溶液、蒸馏水、pH试纸
[信息资料]Na2CO3 、Na2SO4和CuSO4固体溶于水分别会解离出Na+ 与CO32-、Na+与
SO42-、Cu2+与SO42-
[实验记录]
|
|
10%的Na2CO3溶液 |
10%的Na2SO4溶液 |
10%的CuSO4溶液 |
蒸馏水 |
|
pH |
>7 |
=7 |
<7 |
=7 |
[结论]不同的盐溶于水形成的溶液,有呈中性、碱性或 性。
[推理]Na2CO3溶液呈碱性的原因除了与水有关外,还与该盐中的 (填离子符号,下同)有关,而CuSO4溶液呈酸性的原因除了与水有关外,还与该盐中的 有关。
[反思与评价]小松在上述实验探究中,采用了实验 的方法。
23.(6分)
有A、B、C、D、E五种化合物,A为白色固体,B为无色无味的气体,E为不溶于稀硝酸的白色沉淀,它们的关系如下图:
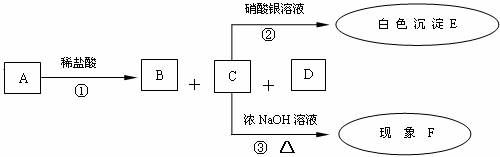
请填空:
(1)白色沉淀E为 。
(2)若现象F为“无明显变化”,则A的化学式可能为 (填字母)。
a. Na2CO3 b. MgCO3 c. KHCO3
(3)若现象F为“无色有刺激性气味的气体”,则A可能为 (填化学式),反应③的化学方程式为 。
22.(5分)
制豆腐是中国古代的一项重要发明,现豆腐在全球已成为颇受欢迎的食品,其制作的主要工艺流程通常如下:

[资料] 下表是豆腐中主要成分的平均质量分数:
|
成 分 |
水 |
蛋白质 |
脂肪 |
糖类 |
钙 |
磷 |
铁 |
维生素B1 |
维生素B2 |
|
质量分数/
% |
89.3 |
4.7 |
1.3 |
2.8 |
0.24 |
0.064 |
1.4 |
0.00006 |
0.00003 |
(1)上述工艺流程中,磨浆属于 变化,由豆腐花制豆腐的过程就是将豆腐与水分离,该设计利用的操作是 。
(2)除水、无机盐和维生素外,豆腐中还含的营养素有 ,含人体所需的微量元素是 。
(3)除大豆外,很多食物也能提供丰富的蛋白质。下列能提供丰富蛋白质的食物有
(填字母)。
A.萝卜 B. 鱼 C. 大米 D. 奶制品 E. 花生油 F. 苹果
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com