
2.据报道:某地一名5岁的女孩子把涂改液当饮料吸食,食道被严重烧伤。经医院检测后发现,涂改液中含有苯、甲基环已烷等多种有毒物质。由此可知,涂改液是( )
A.混合物 B.纯净物 C.单质 D.化合物
1.下列成语或俗语涉及化学变化的是( )
A.花香四溢 B.百炼成钢 C.滴水成冰 D.积沙成塔
30.(18分)课外化学兴趣小组的同学利用某化工厂的废碱液(主要成分为Na2CO3,还含有少量NaCl,其它杂质不计)和石灰乳为原料制备烧碱,并对所得的烧碱粗产品的成分进行分析和测定。
[粗产品制备]
(1)将废碱液加热蒸发浓缩,形成较浓的溶液,冷却后与石灰乳混合,发生反应的化学方程式为 。
(2)将反应后的混合物过滤,得到的滤液进行蒸发结晶,制得NaOH粗产品。
[粗产品成分分析]
(1)取适量粗产品溶于水,滴加Ba(NO3)2溶液出现白色浑浊,发生反应的化学方程式为 ,该粗产品中一定不含有 ,理由是
。
(2)该小组同学通过对粗产品成分的实验分析,确定该粗产品中含有三种物质。
[粗产品含量测定]
Na2CO3含量的测定:
(1)该兴趣小组的同学设计了下图所示的实验装置。取10.0g粗产品,进行实验。
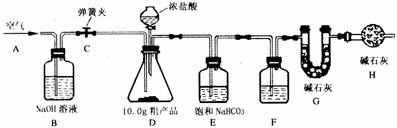
[说明]碱石灰是CaO与NaOH 的固体混合物。E装置中的饱和NaHCO3溶液是为了除
去二氧化碳气体中的氯化氢,发生的反应为NaHCO3 十HC1 = NaCl十CO2↑十H2O。
(2)操作步骤
①连接好装置,检查气密性;②打开弹簧夹C,在A处缓缓通入一段时间空气;③称量G
的质量;④关闭弹簧夹C,慢慢滴加浓盐酸至过量,直至D中无气泡冒出;⑤打开弹簧夹C,再次缓缓通入一段时间空气;⑥再次称量G的质量,得前后两次质量差为0. 48g。
(3)问题探究
F中的试剂应为 ,B装置的作用是 ,
H装置的作用是 。
若没有H装置,则测定的Na2CO3的质量分数会 (填“偏大”、“偏小”、“不变”)。
事实上10.0g粗产品只能产生0.44g CO2。请你仔细分析上述实验,解释实验值0. 48g比正确值0.44g偏大的原因(假设操作均正确)
。
(4)数据计算
根据正确值0.44g可求得粗产品中Na2CO3的质量分数为 %。
NaOH含量的测定:
该小组同学又另取10.0g粗产品,逐滴加入20%的盐酸至恰好完全反应时,消耗盐酸的质量为36. 5g.放出CO2 0.44g(不考虑二氧化碳气体的溶解)。求原粗产品中NaOH的质量分数。(写出计算过程)
29.(5分)小兵同学在化学实验室发现一瓶盛有无色溶液的试剂瓶,其标签严重破损(如下图所示)。老师告诉他,这瓶试剂可能是硫酸、硫酸钠、硫酸镁溶液中的一种。小兵同学通过查阅资料得知,常温下这三种物质的溶解度如下表:

|
物质 |
H2SO4 |
Na2SO4 |
MgSO4 |
|
溶解度/g |
与水任意比互溶 |
19.0 |
39.0 |
小兵同学根据上述信息.分析认为此溶液一定不是 溶液。为确定其成分,该同学对此溶液进行如下实验探究:
[提出假设]该溶液可能是 。
[实验验证]
|
实验步骤 |
实验现象 |
实验结论 |
|
|
|
|
28.(7分)现有一包白色粉末,可能由NaCl、Na2SO4、Na2CO3、CuSO4中的一种或几种组成。现做如下实验:①取少量粉末,加水溶解得无色溶液;②另取少量粉末,滴加稀盐酸,无明显现象。请回答:
(1)由实验①可确定原粉末中一定没有 ;
由实验②可确定原粉末中一定没有 。
(2)根据上述实验现象,得出原粉末中可能含有的物质是 、 。
(3)为进一步确定原粉末的组成,另取少量粉末按下图所示进行实验:
[在AgNO3、Ba(NO3)2、BaCl2溶液中选择两种作为A、B试剂,且A、B的阳离子不同]

原粉末的成分是 ;试剂A为 ;试剂B为 。
(若有多种情况,只需写出其中一种)
27.(7分)下图是化学实验中常用的几种装置。

请回答下列问题:
(1)指出有编号的仪器名称:① ,② 。
(2)利用上述A、D装置的组合可以制取的一种气体是 ,写出实验室制取该气
体的化学反应方程式 。
(3)某同学欲收集一种难溶性气体,认为E装置可以代替B装置。请简述该同学应如何使
用E装置? 。
26.(6分)已知A~G七种物质都是初中化学课本中出现过的化合物,其中F是常用的建筑材料;H为常见的单质。各物质之间存在如下转化关系(反应条件如下图所示)。
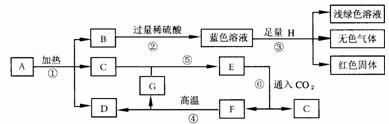
(1)请写出物质A的化学式 。
上述蓝色溶液中的溶质有 、 。
(2)在①~⑥反应中属于化合反应的是 (填序号)。
(3)上述转化过程中,有能够反映我国古代人民在化学方面对人类作出伟大贡献的变化。
请举出其中一例,用化学方程式表示 。
25.(3分)草酸钙(CaC2O4)是不能被人体吸收的沉积物。豆腐中含有较多的钙盐[如硫酸钙(CaSO4)等],菠菜、洋葱、竹笋中含有丰富的草酸(H2C2O4)、草酸钠(Na2C2O4)豆腐和上述几种蔬菜混合食用,可能诱发“结石”症。
(1)由草酸的化学式可知其中碳元素的化合价是 ;
(2)草酸与硫酸钙反应的化学方程式为H2C2O4十CaSO4== CaC2O4↓十H2SO4请写出草酸钠与硫酸钙反应的化学方程式 。
24.(4分)小李同学在学习了有关维生素的知识后,自制了一张《维生素C》知识小卡片,但不完整,请你帮他填写表中空格的内容。
|
《维生素C》知识小卡片 |
|||
|
分子结构 |
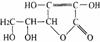 |
化学式 |
|
|
相对分子质量 |
|
||
|
Vc的性质 |
能溶于水,在加热或碱性环境中易被氧化而破坏 |
||
|
Vc的存在 |
绿色蔬菜(如黄瓜、生菜)、水果(如柑橘) |
||
|
食用黄瓜时注意事项 |
|
||
|
保存Vc片注意事项 |
|
23.(4分)将下列各操作名称的序号填在后面的横线上(每个序号只填写一次):
①搅拌 ②蒸发 ③过滤 ④加热
(1)由饱和的食盐水得到食盐晶体 ;
(2)将饱和的硝酸钾溶液变为不饱和溶液 ;
(3)除去食盐中的泥沙,先溶解,再 ;
(4)将浓硫酸注入水中,为使热量迅速散发 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com